- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Теория строения органических веществ А.М. Бутлерова(10 класс)
Содержание
- 1. Презентация по химии на тему Теория строения органических веществ А.М. Бутлерова(10 класс)
- 2. Основные «противоречия»
- 3. Теория радикалов(30 гг. XIX в Й.Берцелиус, Ю.Либих,
- 4. Теория типов(40-50 гг. XIX в. Ш.Жерар, А.Кекуле
- 5. «Органическая химия может сейчас кого угодно свести
- 6. Научные предпосылки возникновения теорииРазвитие и утверждение атомистических
- 7. Основные положения теории строения органических веществ (А.М.
- 8. 2. Свойства веществ определяются не только их
- 9. ЗАДАНИЕ:Составьте структурные формулы для молекул состава С4Н10
- 10. Трансформация изомеров пентана
- 11. 4. Зная строение вещества, можно предположить его
- 12. 1. Развитие представлений о строении молекул: свойства
- 13. 3. Превращение органической химии из описательной науки
- 14. Значение теории химического строения А. М. Бутлерова
- 15. Подведем итоги:1) Что такое изомерия? Изомеры?2) Что
- 16. Домашнее задание:Базовый: §2, упр.2,8,11 письменно; вопросы
- 17. К стартовой работе необходимо:ЗНАТЬ 1.Формулировку 1-го и
- 18. ВАЛЕНТНОСТЬ* - (понятие введено К.Э.Франклендом в 1853
- 19. СТЕПЕНЬ ОКИСЛЕНИЯ* - это условный заряд
- 20. ?? Вопрос на засыпкуЧто общего в смысле
- 21. Проверьте себя:Метан СН4С-4Н+4Вал-ть С=4Вал-ть Н=1 Азот N02 Вал-ть N=3Вода Н2ОН+2О-2 Вал-ть О=2Вал-ть Н=1
- 22. Вещества, которые имеют один и тот же
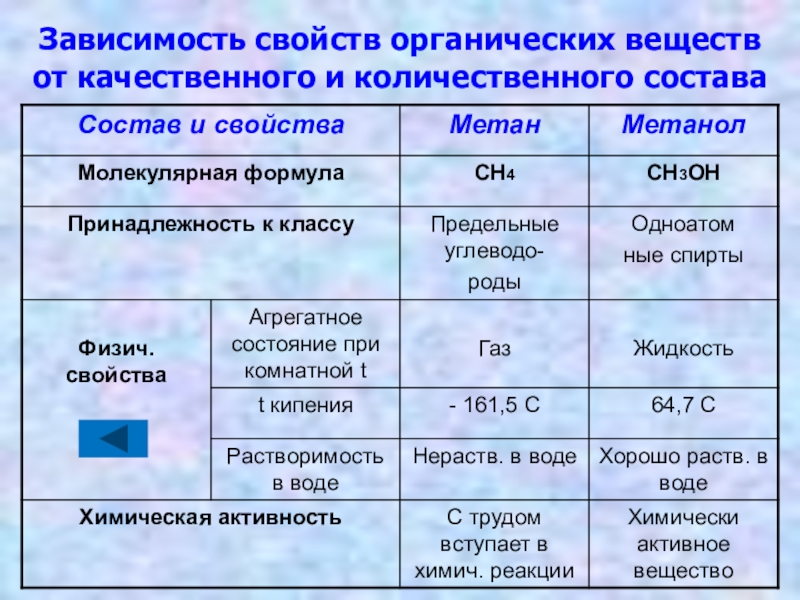
- 23. Зависимость свойств органических веществ от качественного и количественного состава
- 24. Франкленд (Frankland) Эдуард (1825-99), английский химик-органик, иностранный член-корреспондент Петербургской АН (1876). Ввел термин «валентность» (1853).
- 25. Бутлеров Александр Михайлович (1828-86), российский химик-органик, академик
- 26. Кстати… Создатель теории химического строения Александр Бутлеров стал
- 27. Берцелиус (Berzelius) Йенс Якоб (1779-1848), шведский химик
- 28. Кекуле (Kekule) Фридрих Август (1829-96), немецкий химик-органик,
- 29. Велер Фридрих (1800-82), немецкий химик, иностранный член-корреспондент
- 30. Атомы четырехвалентного углерода могут
- 31. 1. Структурная изомерия – молекулы
- 32. 2. Пространственная (стереоизомерия) – молекулы
Слайд 2Основные «противоречия»
Многообразие веществ, которые образованы небольшим числом элементов;
Кажущееся несоответствие понятий валентности и степени окисления в органических веществах – С3Н8;
Различные физические и химические свойства соединений, имеющих одинаковую молекулярную формулу:
С6Н12О6 – глюкоза, фруктоза;
С2Н6О – этиловый спирт, диметиловый эфир
Слайд 3Теория радикалов
(30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма)
В состав органических
Радикалы всегда постоянны, не подвергаются изменениям, переходят из одной молекулы в другую;
Радикалы могут существовать в свободном виде.
Понятие «радикал» прочно вошло в химию
Слайд 4Теория типов
(40-50 гг. XIX в. Ш.Жерар, А.Кекуле и др.)
Все органические
Формулы выражают не внутреннее строение молекулы, а способы образования, свойства определяют все атомы молекулы;
Недостатки: Теория позволила классифицировать орг. вещества, но зашла в тупик по мере накопления экспериментального материала. Невозможно предсказать свойства вещества на основе строения его молекулы. У каждого вещества столько формул, сколько его превращений существует.
Слайд 5«Органическая химия может сейчас кого угодно свести с ума. Она представляется
(из письма Ф.Велера к Й.Берцелиусу 1835г.)
Слайд 6Научные предпосылки возникновения теории
Развитие и утверждение атомистических представлений (съезд в Карслруэ,
Установление понятия «валентность» (Э. Франкленд, 1853г.);
Понятие четырехвалентности углерода (А. Кекуле, 1858г.);
Идеи о соединении атомов углерода в цепи (А. Кекуле, А. Купер, 1857г.)
Т.о. до Бутлерова целостной теории, подтвержденной экспериментом, не существовало.
Слайд 7Основные положения теории строения органических веществ
(А.М. Бутлеров 1861 – 1864
1. Атомы в молекулах органический веществ соединены в определенной последовательности согласно их валентности. Эту последовательность Бутлеров назвал ХИМИЧЕСКИМ СТРОЕНИЕМ.
Углерод в органических соединениях всегда ЧЕТЫРЕХВАЛЕНТЕН, а его атомы способны соединяться друг с другом, образуя различные цепи. Углерод в органических соединениях всегда ЧЕТЫРЕХВАЛЕНТЕН, а его атомы способны соединяться друг с другом, образуя различные цепи. Химическое строение молекул может быть отображено при помощи структурных формул.
Слайд 82. Свойства веществ определяются не только их качественным и количественным составом,
3. Свойства органических соединений зависят от взаимного влияния атомов и групп атомов в молекуле друг на друга. Наибольшее влияние оказывают атомы, непосредственно связанные друг с другом. Влияние атомов или групп атомов, не связанных непосредственно, ослабевает по мере их удаления друг от друга.
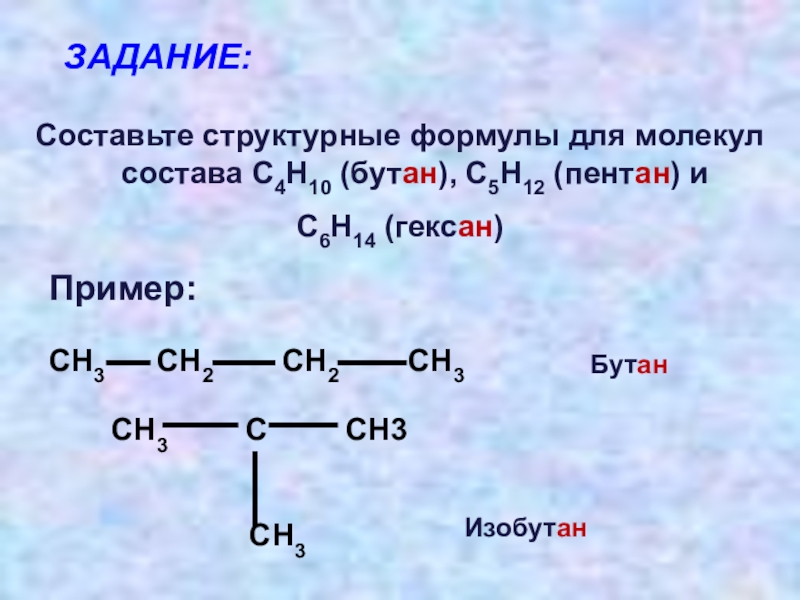
Слайд 9ЗАДАНИЕ:
Составьте структурные формулы для молекул состава С4Н10 (бутан), С5Н12 (пентан) и
С6Н14 (гексан)
СН3 СН2 СН2 СН3
СН3 С СН3
СН3
Бутан
Изобутан
Пример:
Слайд 114. Зная строение вещества, можно предположить его свойства. И наоборот, зная
СН3 СН2 ОН этиловый спирт
С2Н6О
СН3 О СН3 диметиловый эфир
Если известно, что вещество, имеющее молекулярную формулу С2Н6О, вступает в химические реакции, характерные для спиртов (выделяет водород в реакции с металлическим натрием), то можно сделать вывод, что мы говорим об этиловом спирте С2Н5ОН.
Слайд 121. Развитие представлений о строении молекул: свойства вещества можно объяснить на
Направления современного развития теории Бутлерова
2. Развитие представлений об изомерии: современная органическая химия различает 2 основных типа изомерии : структурную Развитие представлений об изомерии: современная органическая химия различает 2 основных типа изомерии : структурную (изомерия цепи, положения кратных связей, функциональных групп, гомологических рядов) и стереоизомерию (геометрическую, или цис-транс-изомерию и оптическую, или зеркальную).
Слайд 133. Превращение органической химии из описательной науки в созидательную, прогнозирующую; возможно
Направления современного развития теории Бутлерова
4. Создание искусственных аналогов природных веществ, которые могут даже превосходить природные по свойствам (синтетические красители, каучуки, пластмассы, волокна).
Слайд 14Значение теории химического строения А. М. Бутлерова для органической химии
Слайд 15Подведем итоги:
1) Что такое изомерия? Изомеры?
2) Что такое гомология? Гомологи?
3) Что
4) Сформулируйте положение теории строения, которое объясняет различие в свойствах изомеров.
5) Назовите причины многообразия органических веществ.
Слайд 16Домашнее задание:
Базовый: §2, упр.2,8,11 письменно;
вопросы 1,3- 6 устно
Профильный: §2,
презентации
Подготовиться к стартовой работе!
Слайд 17К стартовой работе необходимо:
ЗНАТЬ
1.Формулировку 1-го и 2-го положений теории Бутлерова;
2.
УМЕТЬ
Изображать структурные формулы органических соединений согласно валентности элементов;
Объяснять причины многообразие органических соединений.
ПОВТОРИТЬ
Типы химических связей, основные типы реакций;
Строение атомов 1-3 периодов;
Простейшие расчеты по уравнению.
ТЕСТЫ: 3.20,3.22,3.24,3.26 (эл. приложение проф.)
Слайд 18
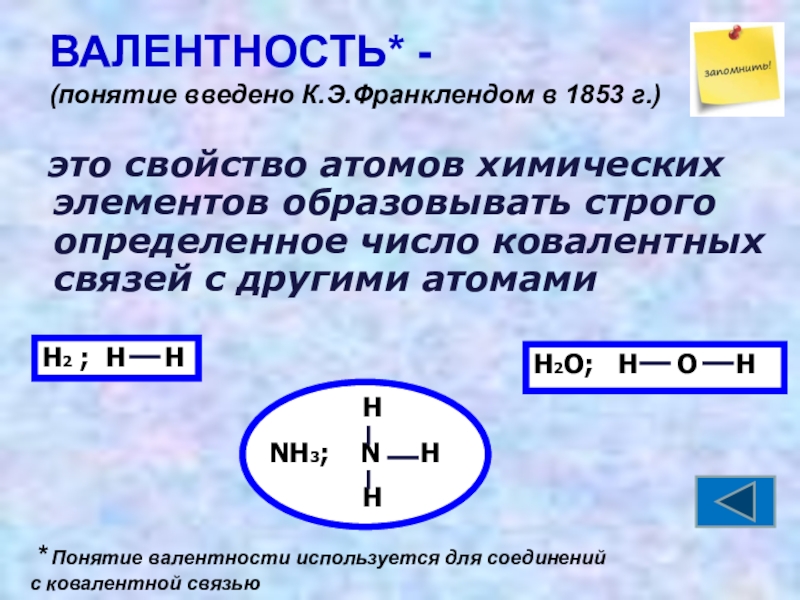
ВАЛЕНТНОСТЬ* -
(понятие введено К.Э.Франклендом в 1853 г.)
это свойство атомов химических
* Понятие валентности используется для соединений
с ковалентной связью
Н2 ; Н Н
H
NH3; N H
H
Н2О; Н О Н
Слайд 19СТЕПЕНЬ ОКИСЛЕНИЯ* -
это условный заряд атома в соединении,
что вещество состоит из ионов
* Понятие степени окисления более
характерно для соединений с ионной связью
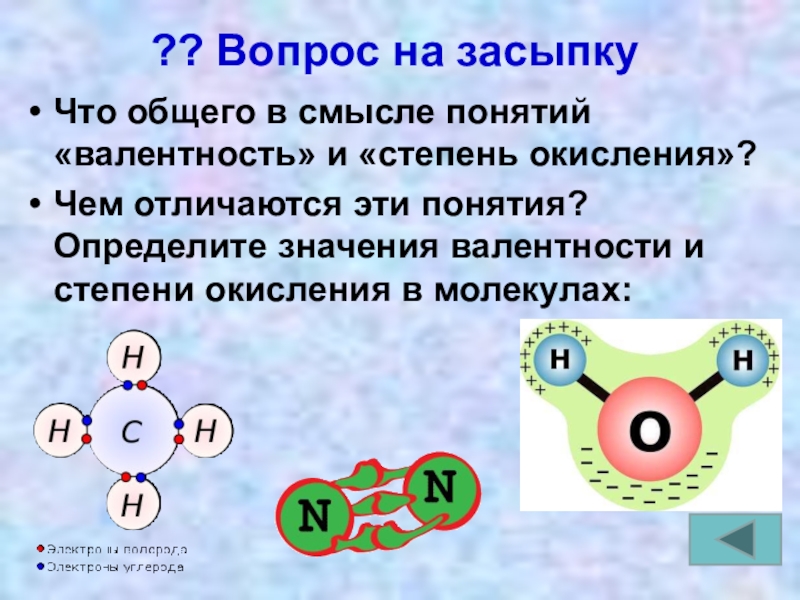
Слайд 20?? Вопрос на засыпку
Что общего в смысле понятий «валентность» и «степень
Чем отличаются эти понятия? Определите значения валентности и степени окисления в молекулах:
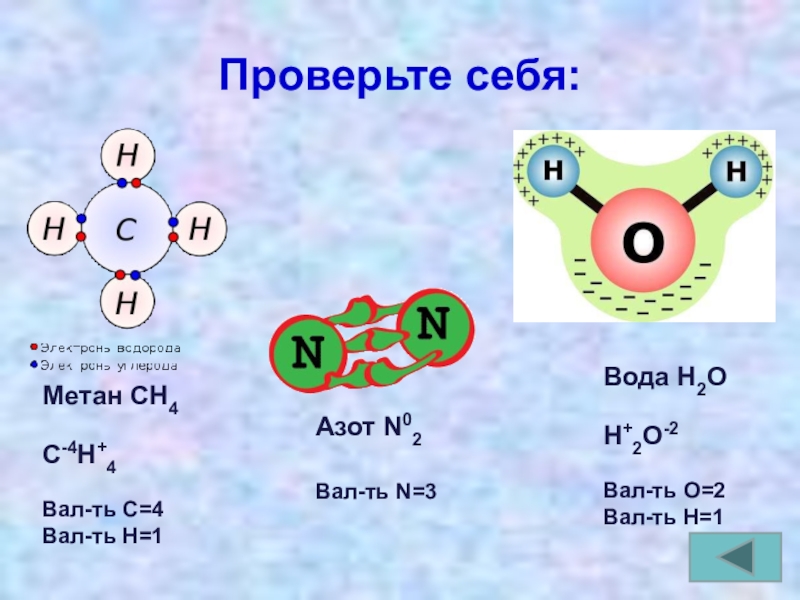
Слайд 21Проверьте себя:
Метан СН4
С-4Н+4
Вал-ть С=4
Вал-ть Н=1
Азот N02
Вал-ть N=3
Вода Н2О
Н+2О-2
Вал-ть О=2
Вал-ть Н=1
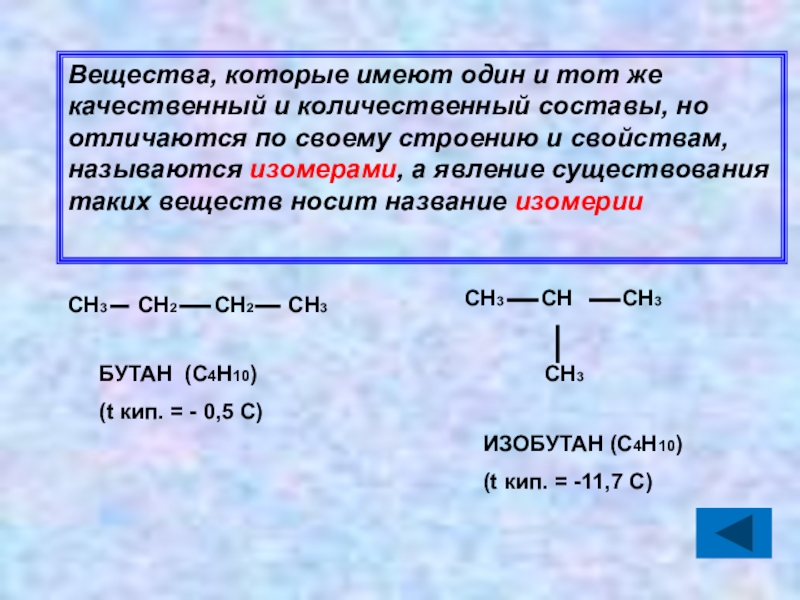
Слайд 22Вещества, которые имеют один и тот же качественный и количественный составы,
СН3 СН2 СН2 СН3
СН3 СН СН3
СН3
БУТАН (С4Н10)
(t кип. = - 0,5 С)
ИЗОБУТАН (С4Н10)
(t кип. = -11,7 С)
Слайд 24Франкленд (Frankland) Эдуард (1825-99), английский химик-органик, иностранный член-корреспондент Петербургской АН (1876).
Слайд 25Бутлеров Александр Михайлович (1828-86), российский химик-органик, академик Петербургской АН (1874). Создал
Слайд 26Кстати…
Создатель теории химического строения Александр Бутлеров стал виновником пожара в Казанском
Слайд 27Берцелиус (Berzelius) Йенс Якоб (1779-1848), шведский химик и минералог, иностранный почетный
Слайд 28Кекуле (Kekule) Фридрих Август (1829-96), немецкий химик-органик, иностранный член-корреспондент Петербургской АН
Слайд 29Велер Фридрих (1800-82), немецкий химик, иностранный член-корреспондент Петербургской АН (1853). Впервые
Слайд 30
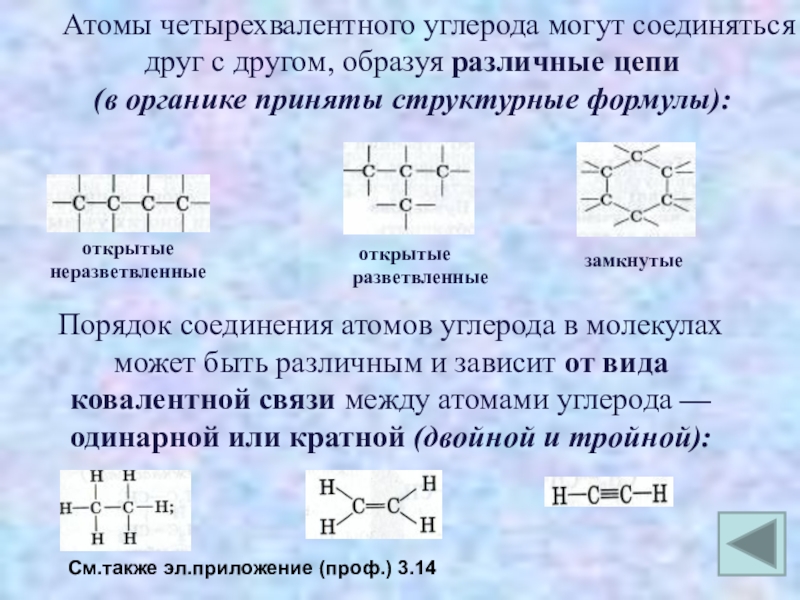
Атомы четырехвалентного углерода могут соединяться друг с другом,
(в органике приняты структурные формулы):
открытые неразветвленные
замкнутые
Порядок соединения атомов углерода в молекулах может быть различным и зависит от вида ковалентной связи между атомами углерода — одинарной или кратной (двойной и тройной):
См.также эл.приложение (проф.) 3.14
Слайд 31
1. Структурная изомерия – молекулы веществ различаются порядком
ВИДЫ ИЗОМЕРИИ
1) изомерия углеродной цепи (скелета)
2) изомерия положения
бутен-1
б) заместителей
1-хлорпропан
2-хлорпропан
в) изомерия положения функциональных групп
3) изомерия гомологических рядов (межклассовая)
бутен-2
Слайд 32
2. Пространственная (стереоизомерия) – молекулы веществ различаются не порядком
ВИДЫ ИЗОМЕРИИ