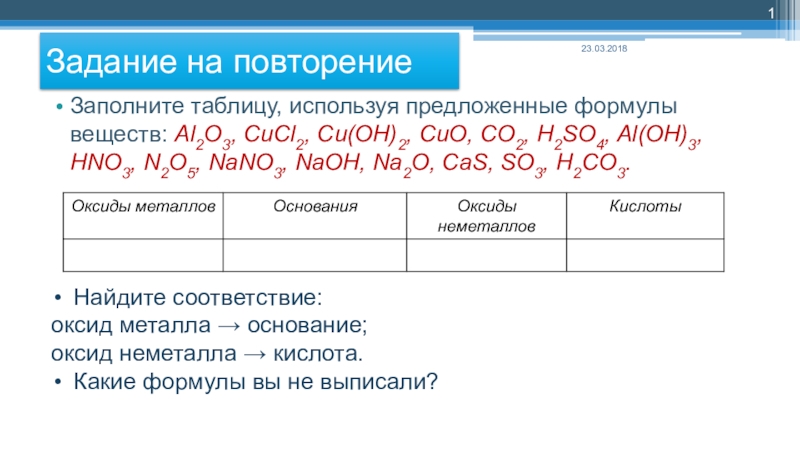
Найдите соответствие:
оксид металла → основание;
оксид неметалла → кислота.
Какие формулы вы не выписали?
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Соли (8 класс)
Содержание
- 1. ПРезентация по химии на тему Соли (8 класс)
- 2. Соли8 классАвтор: Кунова Галина Васильевна – учитель химии ЦДО г. Липецк.
- 3. Соли по составу похожи на кислоты, только
- 4. Как составить формулу соли?1. Обозначают заряды ионов, из
- 5. Аналогично выводят формулы солей кислородсодержащих кислот, имеющих
- 6. Как образуют названия солей?Соли бескислородных кислот: соли
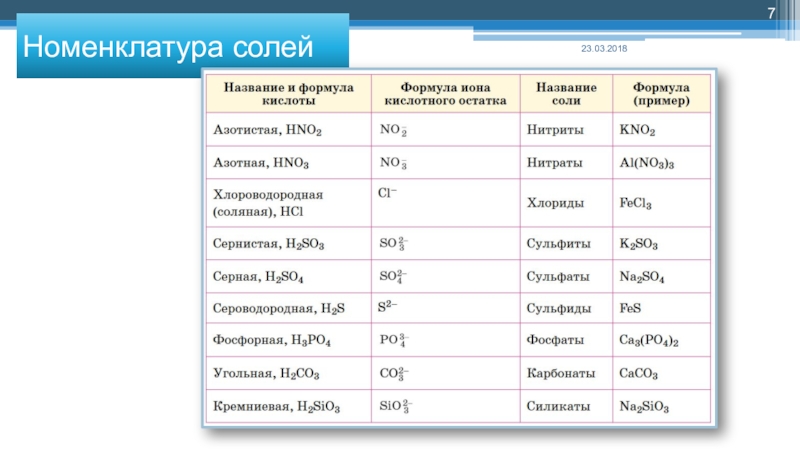
- 7. Номенклатура солей
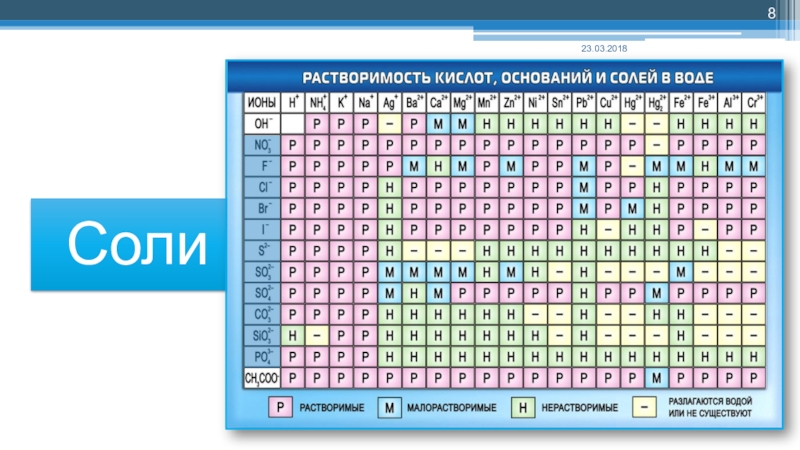
- 8. Слайд 8
- 9. Хлорид натрия NaCl - хорошо растворимая в воде
- 10. Карбонат кальция CaCO3 - нерастворимая в воде соль,
- 11. Из карбоната кальция наземные животные «строят» свои
- 12. Фосфат кальция Ca3(PO4)2, нерастворимый в воде, - это
- 13. Мы изучилиЗадание:из перечисленных формул: H2S, K2SO3, KOH,
- 14. Домашнее задание§21.
- 15. Источники:Габриелян, О. С. Химия. 8 класс: учеб.
Соли8 классАвтор: Кунова Галина Васильевна – учитель химии ЦДО г. Липецк.
Слайд 1Задание на повторение
Заполните таблицу, используя предложенные формулы веществ: Al2O3, CuCl2, Cu(OH)2,
CuO, CO2, H2SO4, Al(OH)3, HNO3, N2O5, NaNO3, NaOH, Na2O, CaS, SO3, H2CO3.
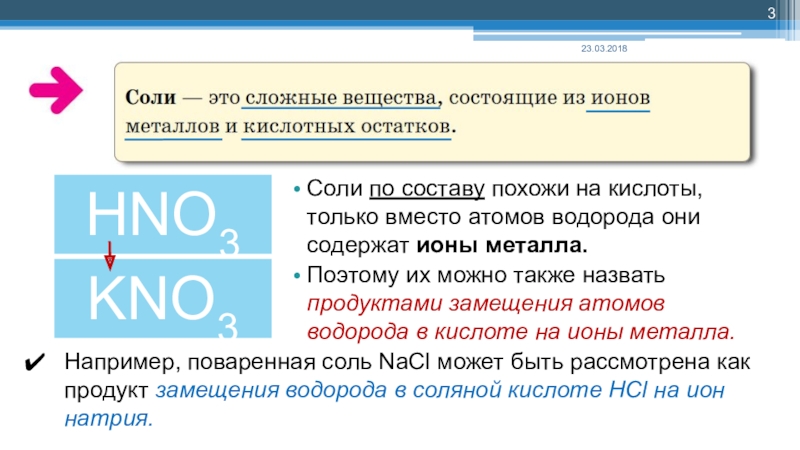
Слайд 3Соли по составу похожи на кислоты, только вместо атомов водорода они
содержат ионы металла.
Поэтому их можно также назвать продуктами замещения атомов водорода в кислоте на ионы металла.
Поэтому их можно также назвать продуктами замещения атомов водорода в кислоте на ионы металла.
KNO3
HNO3
Например, поваренная соль NaCl может быть рассмотрена как продукт замещения водорода в соляной кислоте HCl на ион натрия.
Слайд 4Как составить формулу соли?
1. Обозначают заряды ионов, из которых состоит соединение: Al3+S2–.
Заряд иона алюминия 3+, а заряд иона серы можно определить по формуле соответствующей сероводородной кислоты H2S, он равен 2–.
2. Находят наименьшее общее кратное числовых значений зарядов ионов алюминия и серы (3 и 2), оно равно 6.
3. Находят индексы, разделив наименьшее общее кратное на величины зарядов, и записывают формулу:
2. Находят наименьшее общее кратное числовых значений зарядов ионов алюминия и серы (3 и 2), оно равно 6.
3. Находят индексы, разделив наименьшее общее кратное на величины зарядов, и записывают формулу:
Слайд 5Аналогично выводят формулы солей кислородсодержащих кислот, имеющих сложные ионы.
Выведем, например,
формулу кальциевой соли фосфорной кислоты − фосфата кальция.
По таблице Менделеева определим заряд иона кальция как элемента главной подгруппы II группы (IIА группы): 2+.
По формуле фосфорной кислоты H3PO4 определим заряд иона, образованного кислотным остатком: РО43-.
Отсюда формула фосфата кальция имеет вид:
По таблице Менделеева определим заряд иона кальция как элемента главной подгруппы II группы (IIА группы): 2+.
По формуле фосфорной кислоты H3PO4 определим заряд иона, образованного кислотным остатком: РО43-.
Отсюда формула фосфата кальция имеет вид:
Слайд 6Как образуют названия солей?
Соли бескислородных кислот:
соли HCl - хлориды;
соли
H2S - сульфиды.
Названия солей кислородсодержащих кислот составляют из двух слов:
названия иона, образованного кислотным остатком (в именительном падеже) + названия иона металла (в родительном падеже).
Примеры:
KNO3 - нитрат калия;
Ca(NO2)2 - нитрит кальция;
Fe2+SO3 - сульфит железа (II).
Названия солей кислородсодержащих кислот составляют из двух слов:
названия иона, образованного кислотным остатком (в именительном падеже) + названия иона металла (в родительном падеже).
Примеры:
KNO3 - нитрат калия;
Ca(NO2)2 - нитрит кальция;
Fe2+SO3 - сульфит железа (II).
Слайд 9Хлорид натрия NaCl - хорошо растворимая в воде соль, известна под названием
поваренная соль.
Без этой соли невозможна жизнь растений, животных и человека, так как она обеспечивает важнейшие физиологические процессы в организмах: в крови соль создаёт необходимые условия для существования красных кровяных телец, в мышцах обусловливает способность к возбудимости, в желудке образует соляную кислоту, без которой было бы невозможным переваривание и усвоение пищи.
Хлорид натрия широко используют в химической промышленности для получения натрия, хлора, соляной кислоты, в медицине, для приготовления пищи, для консервирования продуктов питания (соление и квашение овощей) и т. д.
Без этой соли невозможна жизнь растений, животных и человека, так как она обеспечивает важнейшие физиологические процессы в организмах: в крови соль создаёт необходимые условия для существования красных кровяных телец, в мышцах обусловливает способность к возбудимости, в желудке образует соляную кислоту, без которой было бы невозможным переваривание и усвоение пищи.
Хлорид натрия широко используют в химической промышленности для получения натрия, хлора, соляной кислоты, в медицине, для приготовления пищи, для консервирования продуктов питания (соление и квашение овощей) и т. д.
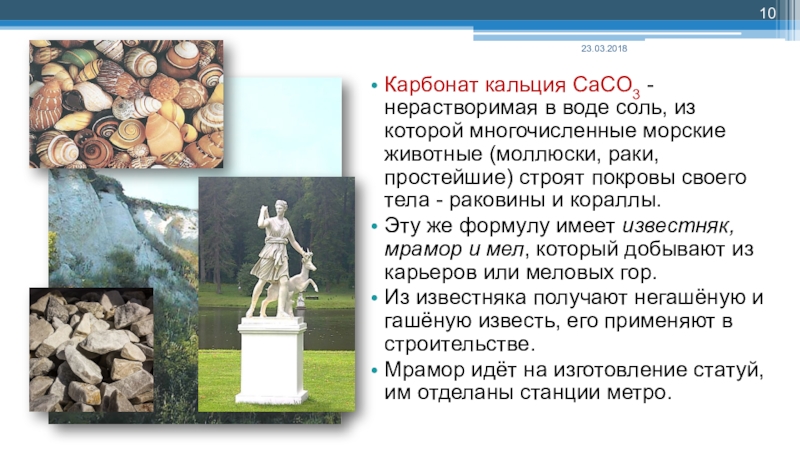
Слайд 10Карбонат кальция CaCO3 - нерастворимая в воде соль, из которой многочисленные морские
животные (моллюски, раки, простейшие) строят покровы своего тела - раковины и кораллы.
Эту же формулу имеет известняк, мрамор и мел, который добывают из карьеров или меловых гор.
Из известняка получают негашёную и гашёную известь, его применяют в строительстве.
Мрамор идёт на изготовление статуй, им отделаны станции метро.
Эту же формулу имеет известняк, мрамор и мел, который добывают из карьеров или меловых гор.
Из известняка получают негашёную и гашёную известь, его применяют в строительстве.
Мрамор идёт на изготовление статуй, им отделаны станции метро.
Слайд 11Из карбоната кальция наземные животные «строят» свои скелеты - внутреннюю опору для
мягких тканей, которые в десятки раз превышают вес самой опоры.
Слайд 12Фосфат кальция Ca3(PO4)2, нерастворимый в воде, - это основа минералов фосфоритов и
апатитов.
Из них производят фосфорные удобрения, без которых было бы невозможно получение высоких урожаев в сельском хозяйстве.
Фосфат кальция также входит в состав костей животных.
Из них производят фосфорные удобрения, без которых было бы невозможно получение высоких урожаев в сельском хозяйстве.
Фосфат кальция также входит в состав костей животных.
Слайд 13Мы изучили
Задание:
из перечисленных формул: H2S, K2SO3, KOH, SO3, Fe(OH)3, FeO, N2O3,
Cu3(PO4)2, Cu2O, P2O5, H3PO4 - выпишите формулы: а) оксидов; б) кислот; в) оснований; г) солей.
Дайте названия веществ.
Дайте названия веществ.
Слайд 15Источники:
Габриелян, О. С. Химия. 8 класс: учеб. для общеобразоват. учреждений /
О. С. Габриелян. 2-е изд., М. : Дрофа, 2013.
Габриелян, О. С. Химия. 8 класс: рабочая тетрадь к учебнику О.С. Габриеляна «Химия. 8 класс» / О. С. Габриелян, С.А. Сладков.- М. : Дрофа, 2013.
Интернет-ресурсы: рисунки, схемы.
Габриелян, О. С. Химия. 8 класс: рабочая тетрадь к учебнику О.С. Габриеляна «Химия. 8 класс» / О. С. Габриелян, С.А. Сладков.- М. : Дрофа, 2013.
Интернет-ресурсы: рисунки, схемы.