- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Семейство углерода, 9 класс.
Содержание
- 1. Презентация по химии на тему Семейство углерода, 9 класс.
- 2. НАХОЖДЕНИЕ В ПРИРОДЕ
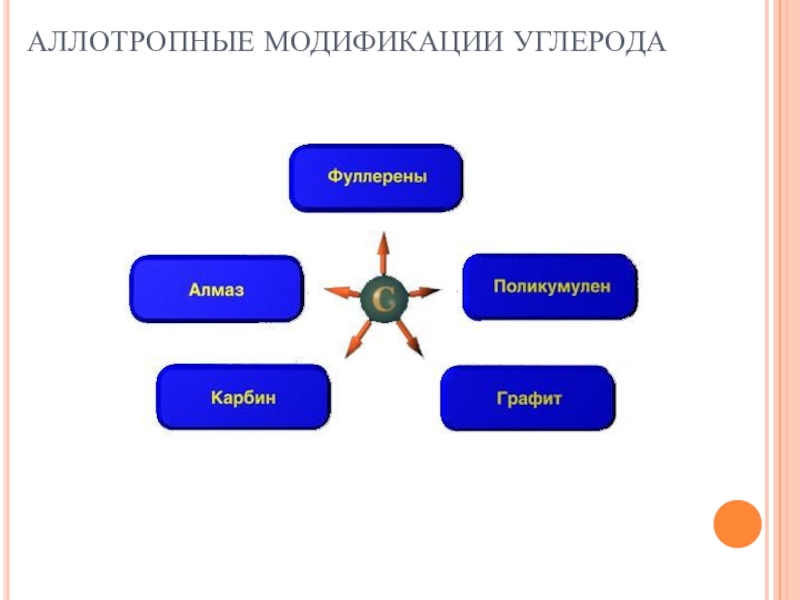
- 3. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ УГЛЕРОДА
- 4. ГРАФИТ Графит – это чёрные
- 5. КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА ГРАФИТА
- 6. ФИЗИЧЕСКИЕ СВОЙСТВАГрафит – тугоплавкое вещество, t горения
- 7. УГОЛЬУголь – тот же графит, только очень мелкокристаллический.
- 8. Уголь – твёрдое вещество, образовавшееся в
- 9. АДСОРБЦИЯРусский химик Т. Е. Ловиц в 1785г.
- 10. Слайд 10
- 11. АЛМАЗВ кристалле алмаза каждый атом углерода связан
- 12. ФИЗИЧЕСКИЕ СВОЙСТВА АЛМАЗА Алмаз – тугоплавкое химически
- 13. Слайд 13
- 14. БРИЛЛИАНТЫБриллианты – это огранённые алмазы.
- 15. КАРБИНМалокристаллический порошок чёрного цвета. По твёрдости занимает промежуточное положение между алмазом и графитом и является полупроводником.
- 16. ФУЛЛЕРЕН Жёлтые кристаллы диаметром 5 – 6
- 17. Слайд 17
- 18. ВОПРОСЫ ПОКУПАТЕЛЯМКакое аллотропное видоизменение углерода вы, как
НАХОЖДЕНИЕ В ПРИРОДЕ
Слайд 4ГРАФИТ
Графит – это чёрные звёздчатые кристаллы с металлическим
блеском.
Достаточно большие пласты графита тёмно – серого цвета.
Достаточно большие пласты графита тёмно – серого цвета.
Слайд 6ФИЗИЧЕСКИЕ СВОЙСТВА
Графит – тугоплавкое вещество, t горения = 800о C, «жирный»
на ощупь. При t = 1200 – 1600о C и давлении 104 Мпа графит способен превращаться в алмаз. Хорошо проводит электрический ток.
Слайд 8
Уголь – твёрдое вещество, образовавшееся в недрах Земли при разложении
органических остатков растений за многие миллионы лет.
Слайд 9АДСОРБЦИЯ
Русский химик Т. Е. Ловиц в 1785г. открыл свойство угля поглощать
и удерживать на поверхности некоторые газообразные и растворимые вещества.
Это явление называется адсорбцией.
Это явление называется адсорбцией.
Слайд 11АЛМАЗ
В кристалле алмаза каждый атом углерода связан с четырьмя соседними атомами
прочными ковалентными связями.
Все четыре связи углерода одинаковые и направлены от центра тетраэдра к его вершинам.
Все четыре связи углерода одинаковые и направлены от центра тетраэдра к его вершинам.
Слайд 12ФИЗИЧЕСКИЕ СВОЙСТВА АЛМАЗА
Алмаз – тугоплавкое химически стойкое вещество. Он не
проводит электрического тока, прозрачен, обладает высокой твёрдостью.
Алмаз при нагревании без доступа воздуха выше 1000о C превращается в графит.
Алмаз при нагревании без доступа воздуха выше 1000о C превращается в графит.
Слайд 15КАРБИН
Малокристаллический порошок чёрного цвета. По твёрдости занимает промежуточное положение между алмазом
и графитом и является полупроводником.
Слайд 16ФУЛЛЕРЕН
Жёлтые кристаллы диаметром 5 – 6 мм. Отдельные ячейки пяти
– и шестиугольники – собраны в сферу. Расстояние между атомами, как и у алмаза, по всем направлениям равны.
Слайд 18ВОПРОСЫ
ПОКУПАТЕЛЯМ
Какое аллотропное видоизменение углерода вы, как представитель компании, выберете?
Какие свойства этого
вещества будут использованы компанией?
Какое применение найдет в компании выбранное вами вещество?
Какое применение найдет в компании выбранное вами вещество?