- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Растворение. Растворы. Кристаллогидраты ( 8 класс)
Содержание
- 1. Презентация по химии на тему Растворение. Растворы. Кристаллогидраты ( 8 класс)
- 2. 2.Показать зависимость растворимости твёрдых веществ от температуры.Цель:1.Познакомиться
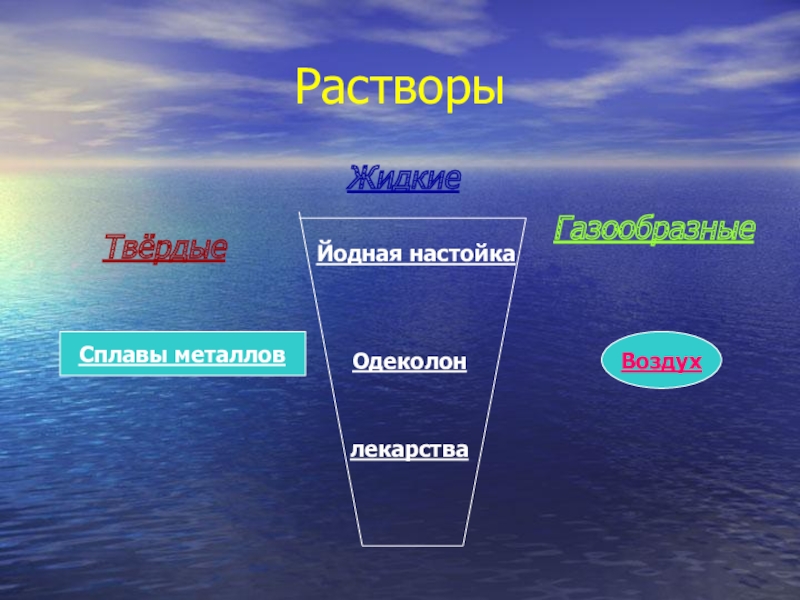
- 3. РастворыЖидкиеТвёрдыеГазообразныеЙодная настойкаОдеколонлекарстваСплавы металловВоздух
- 4. Сванте АвгустФизическая теория растворов1859-1927Растворение-процесс диффузии(взаимное проникновение частиц растворённого вещества между молекулами растворителя)Растворы-однородные системы.Растворы . Растворение.Аррениус1883 г.
- 5. Менделеев Дмитрий ИвановичХимическая теория растворовРастворы. Растворение.1834-1907Растворение -процесс
- 6. Правило смешивания серной кислоты с водой.Сначала- вода,потом -кислота, иначе случится большая беда.
- 7. Тепловые явления при растворенииЭкзотермическиеЭндотермическиеВЫДЕЛЕНИЕ ТЕПЛОТЫ ПРИ РАСТВОРЕНИИ ЩЕЛОЧЕЙ:NaOH,KOH,H2SO4ПОГЛОЩЕНИЕ ТЕПЛОТЫ ПРИ РАСТВОРЕНИИ СОЛЕЙ:NH4NO3,NaCl,KCNS,CH3COONaCЕРНОЙ КИСЛОТЫ(КОНЦ.)
- 8. Каблуков Иван Алексеевич (1857-1942)Современная теория растворов.Кистяковский Владимир
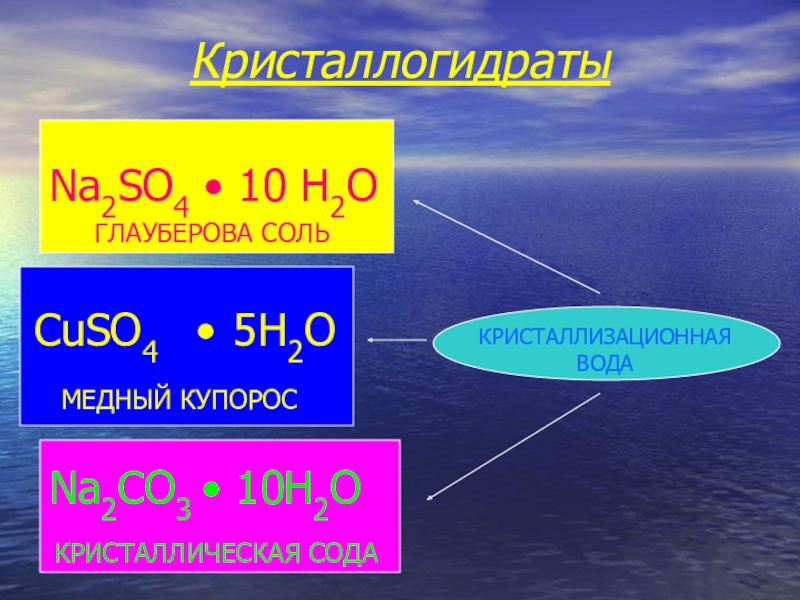
- 9. КристаллогидратыКРИСТАЛЛИЗАЦИОННАЯ ВОДАCuSO4 • 5H2ONa2CO3 • 10H2OКРИСТАЛЛИЧЕСКАЯ СОДАМЕДНЫЙ КУПОРОСГЛАУБЕРОВА СОЛЬNa2SO4 • 10 H2O
- 10. CuSO4•5H2O=CuSO4+5H2OСиний кристаллогидратБелый безводныйРазложение медного купороса.Признак реакции : изменение цветаУсловие реакции : нагревание
- 11. Растворимость веществ в воде
- 12. От каких факторов зависит растворимость?1.От природы веществ.(Растворение
- 13. Слайд 13
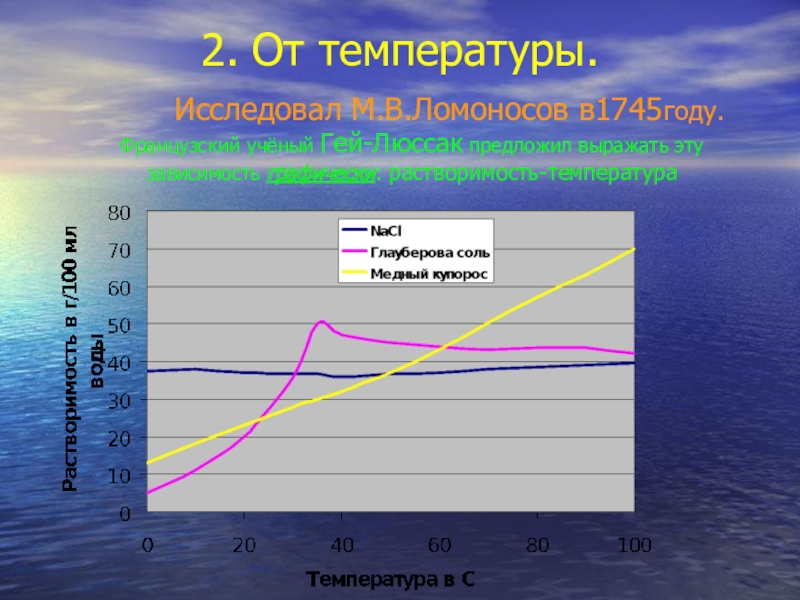
- 14. 2. От температуры.Исследовал М.В.Ломоносов в1745году.Французский учёный Гей-Люссак предложил выражать эту зависимость графически: растворимость-температура
- 15. Взаимодействие иодида калия с нитратом свинца2 K+I- + Pb 2+(NO3)2=2K+NO3-+Pb2+I-2ИСХОДНЫЕ ВЕЩЕСТВАПРОДУКТЫ РЕАКЦИИТип реакции-реакция обмена
- 16. Признаки реакции:2.Изменение цвета на ярко-желтый1.Выпадение осадка PbI2
- 17. Типы растворов по содержанию растворенного вещества.ненасыщенныенасыщенныепересыщенныеВ100г воды
- 18. «голодный»«сытый»«Аппетит растворов»
- 19. Залив Каспийского моря- Кара-Богаз-Гол
- 20. Глауберова соль-мирабилит
- 21. Кристалл поваренной соли
- 22. Кристаллы нитрата кобальта (II)
- 23. Кристаллы сульфата никеля(II)
- 24. Кристаллы сульфата меди(II)
- 25. Домашний эксперимент:Выращивание кристаллов – с.133,§ 34, № 1-4.Домашний эксперимент:Выращивание кристаллов – с.133,§ 34, № 1-4.
Слайд 1Растворы. Растворимость. Кристаллогидраты.
Учитель химии: Шишкова Любовь Викторовна
Ново-Харитоновская СОШ №10 с УИОП
Слайд 22.Показать зависимость растворимости твёрдых веществ от температуры.
Цель:
1.Познакомиться с растворением как физико-химическим
2.Показать зависимость растворимости твёрдых веществ от температуры.
3.Дать классификацию растворов по растворимости.
Слайд 4
Сванте Август
Физическая теория растворов
1859-1927
Растворение-процесс диффузии(взаимное проникновение частиц растворённого вещества между молекулами
Растворы-однородные системы.
Растворы . Растворение.
Аррениус
1883 г.
Слайд 5Менделеев
Дмитрий Иванович
Химическая теория растворов
Растворы. Растворение.
1834-1907
Растворение -процесс химического взаимодействия частиц
Растворы-химические соединения-гидраты.
Слайд 6Правило смешивания серной кислоты с водой.
Сначала- вода,потом -кислота, иначе случится большая
Слайд 7
Тепловые явления при растворении
Экзотермические
Эндотермические
ВЫДЕЛЕНИЕ ТЕПЛОТЫ ПРИ РАСТВОРЕНИИ ЩЕЛОЧЕЙ:
NaOH,KOH,
H2SO4
ПОГЛОЩЕНИЕ ТЕПЛОТЫ ПРИ РАСТВОРЕНИИ
NH4NO3,NaCl,KCNS,
CH3COONa
CЕРНОЙ КИСЛОТЫ(КОНЦ.)
Слайд 8Каблуков Иван
Алексеевич (1857-1942)
Современная теория растворов.
Кистяковский
Владимир
Александрович
(1865-1952)
Растворение - это физико-химический
Раствор -это однородная (гомогенная) система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия-
Имеют непостоянный состав
в растворах: H2SO4•H2O, H2SO4•2H2O
Постоянный состав в кристаллогидратах:
CuSO4•5H2O
гидратов
Слайд 9
Кристаллогидраты
КРИСТАЛЛИЗАЦИОННАЯ ВОДА
CuSO4 • 5H2O
Na2CO3 • 10H2O
КРИСТАЛЛИЧЕСКАЯ СОДА
МЕДНЫЙ КУПОРОС
ГЛАУБЕРОВА СОЛЬ
Na2SO4 •
Слайд 10CuSO4•5H2O=CuSO4+5H2O
Синий кристаллогидрат
Белый безводный
Разложение медного купороса.
Признак реакции : изменение цвета
Условие реакции :
Слайд 12
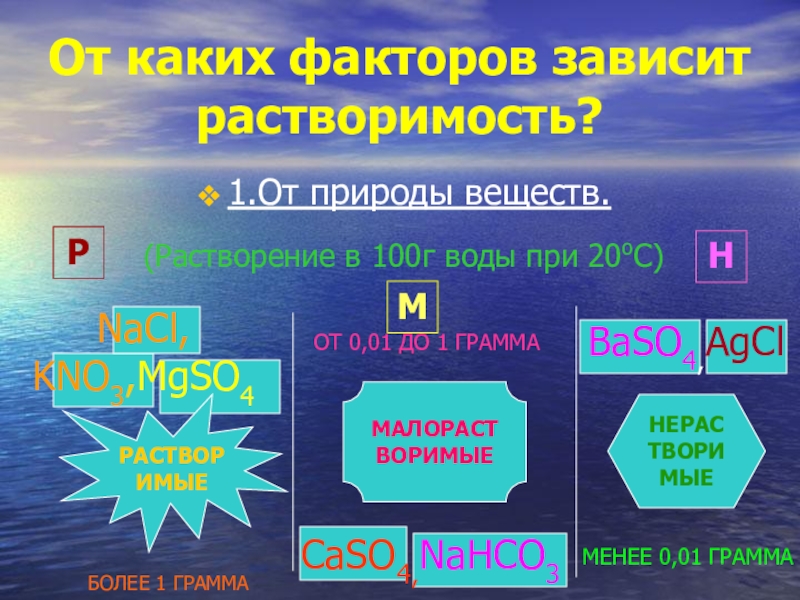
От каких факторов зависит растворимость?
1.От природы веществ.
(Растворение в 100г воды при
РАСТВОРИМЫЕ
МАЛОРАСТВОРИМЫЕ
НЕРАСТВОРИМЫЕ
БОЛЕЕ 1 ГРАММА
МЕНЕЕ 0,01 ГРАММА
NaCl,
KNO3,MgSO4
ОТ 0,01 ДО 1 ГРАММА
CaSO4,NaHCO3
BaSO4,AgCl
Р
М
Н
Слайд 142. От температуры.
Исследовал М.В.Ломоносов в1745году.
Французский учёный Гей-Люссак предложил выражать эту зависимость
Слайд 15
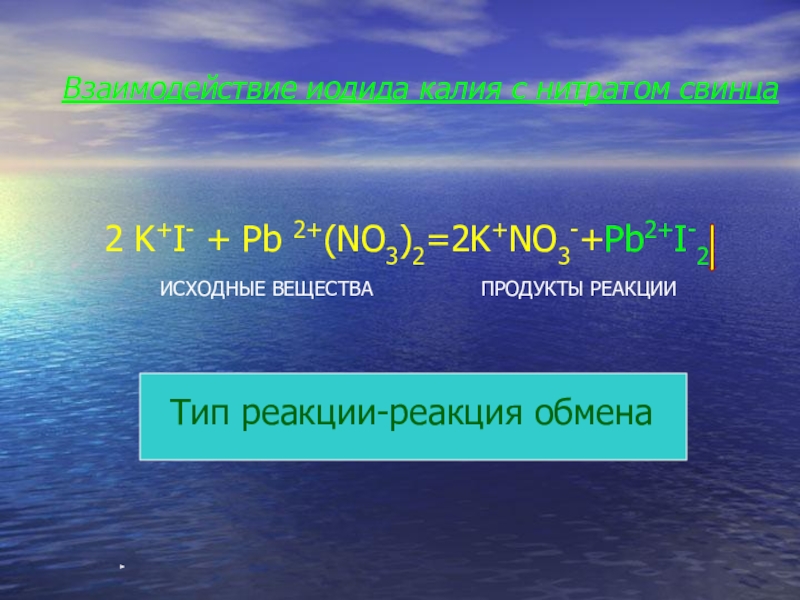
Взаимодействие иодида калия с нитратом свинца
2 K+I- + Pb 2+(NO3)2=2K+NO3-+Pb2+I-2
ИСХОДНЫЕ ВЕЩЕСТВА
ПРОДУКТЫ
Тип реакции-реакция обмена
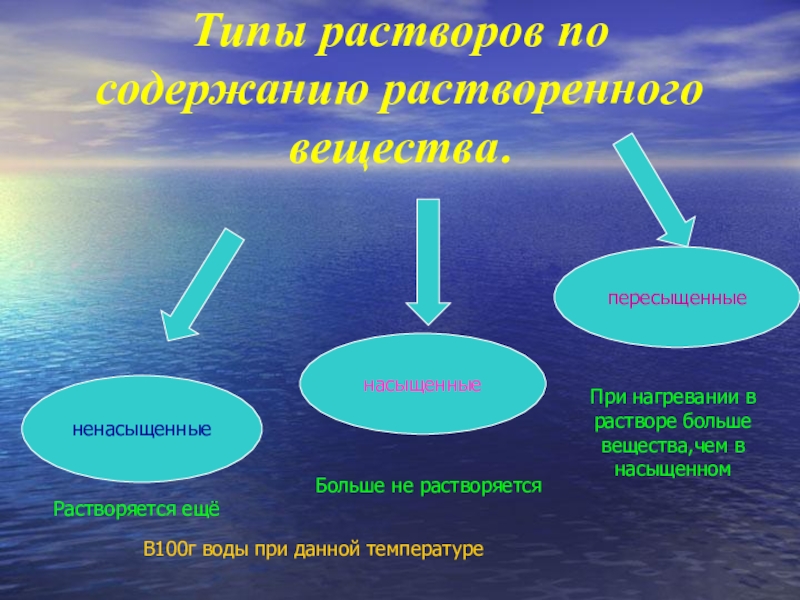
Слайд 17Типы растворов по содержанию растворенного вещества.
ненасыщенные
насыщенные
пересыщенные
В100г воды при данной температуре
Растворяется ещё
Больше
При нагревании в растворе больше вещества,чем в насыщенном
Слайд 25
Домашний эксперимент:
Выращивание кристаллов – с.133,
§ 34, № 1-4.
Домашний эксперимент:
Выращивание кристаллов –
§ 34, № 1-4.