- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему “Неметаллы”
Содержание
- 1. Презентация по химии на тему “Неметаллы”
- 2. Содержание1. Вступление2. Положение в ПСХЭ3. Общие физические свойства4. Общие химические свойства
- 3. ВступлениеВсе элементы делятся на металлы и неметаллы.
- 4. Бор
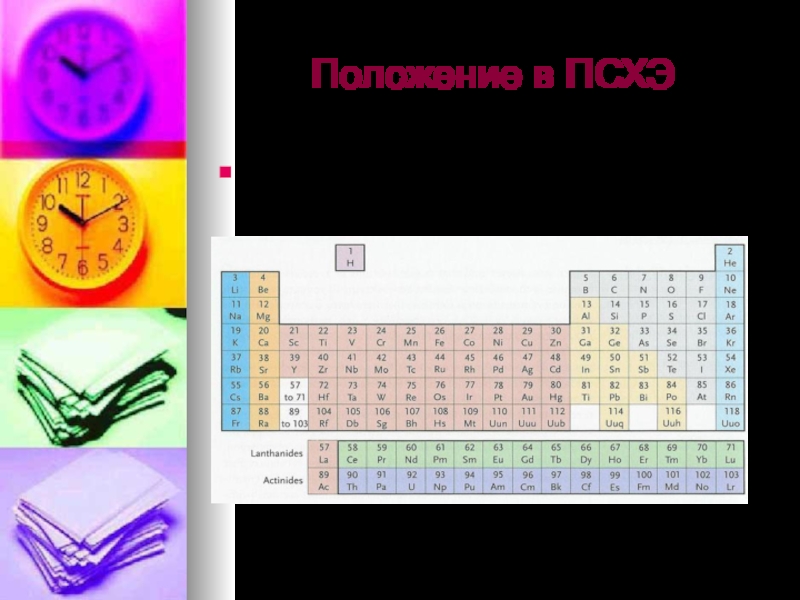
- 5. Положение в ПСХЭнеметаллические элементы в основном расположены в правой верхней части периодической системы.
- 6. Положение в ПСХЭнеметаллы выделены серым цветом
- 7. Общие физические свойстваНеметаллы в виде простых тел
- 8. Бром
- 9. Общие химические свойства. Реакции с О2С кислородом
- 10. Общие химические свойства. Реакции с водородом.С водородом
- 11. Общие химические свойства. Реакции с металлами и
Содержание1. Вступление2. Положение в ПСХЭ3. Общие физические свойства4. Общие химические свойства
Слайд 2Содержание
1. Вступление
2. Положение в ПСХЭ
3. Общие физические свойства
4. Общие химические свойства
Слайд 3Вступление
Все элементы делятся на металлы и неметаллы. Из 107 элементов 85
относятся к металлам. К неметаллам относят следующие элементы: гелий, неон, аргон, криптон, ксенон, радон, фтор, хлор, бром, йод, астат, кислород, сера, селен, теллур, азот, фосфор, мышьяк, углерод, кремний, бор, водород.
Однако это деление условное. При определенных условиях некоторые металлы могут проявлять неметаллические свойства, а некоторые неметаллы – металлические свойства.
Слайд 5Положение в ПСХЭ
неметаллические элементы в основном расположены в правой верхней части
периодической системы.
Слайд 7Общие физические свойства
Неметаллы в виде простых тел находятся в твердом или
газообразном состоянии (исключая бром – жидкость). Они не имеют физических свойств, присущих металлам. Твердые неметаллы не обладают характерным для металлов блеском, они обычно хрупки, плохо проводят электрический ток и тепло (за исключением графита).
Слайд 9Общие химические свойства.
Реакции с О2
С кислородом неметаллы образуют кислотные оксиды. В
одних оксидах они проявляют максимальную степень окисления, равную номеру группы (например,
SO2, N2O5), а других – более низкую (например, SO2, N2O3). Кислотным оксидам соответствуют кислоты, причем из двух кислородных кислот одного неметалла сильнее та, в которой он проявляет более высокую степень окисления. Например, азотная кислота HNO3 сильнее азотистой HNO2, а серная кислотаH2SO4 сильнее сернистой H2SO3.
S+O2=SO2
2N2+5O2=2N2O5
S+O2=SO2
2N2+5O2=2N2O5
Слайд 10Общие химические свойства.
Реакции с водородом.
С водородом неметаллы образуют летучие соединения, как,
например, фтороводород HF, сероводород H2S, аммиак NH3, метан CH4. При растворении в воде водородные соединения галогенов, серы, селена и теллура образуют кислоты той же формулы, что и сами водородные соединения: HF, HCl,HBr, HI, H2S, H2Se, H2Te.
Слайд 11Общие химические свойства.
Реакции с металлами и с другими неметаллами.
С металлами типичные
неметаллы дают соединения с ионной связью (например, NaCl). Неметаллы могут при определенных условиях между собой реагировать, образуя соединения с ковалентной полярной (H2O, HCl) и неполярной связями (CO2).