- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Классификация химических рекций
Содержание
- 1. Презентация по химии на тему Классификация химических рекций
- 2. Эпиграф«О, сколько нам открытий чудныхГотовят просвещенья дух,
- 3. Цели урокаЗначение закона сохранения массы веществКоличественное и качественное выражение закона – уравнения химических реакцийКлассификация химических реакций
- 4. Блеф-играВерите ли Вы, что …Химические явления называют
- 5. Блеф-играВерите ли Вы, что …Химические явления называют
- 6. Закон сохранения массы веществ. Эксперимент: в
- 7. Основоположники закона сохранения массы веществМ.В.Ломоносов, 1748г. А. Лавуазье, 1789г.
- 8. Закон сохранения массы веществ.Масса веществ, вступивших в
- 9. Химические уравнения.Уравнения реакции составляют на основе закона
- 10. Типы химических реакций ( по числу исходных и образующихся веществ)Реакция соединенияРеакция разложенияРеакция замещенияРеакция обмена
- 11. Реакция соединенияПолучение воды:2H2 + O2 =
- 12. Реакция разложенияРазложение воды :2H2O =
- 13. Реакция замещения Вытеснение углеродом атомов
- 14. Реакция обмена
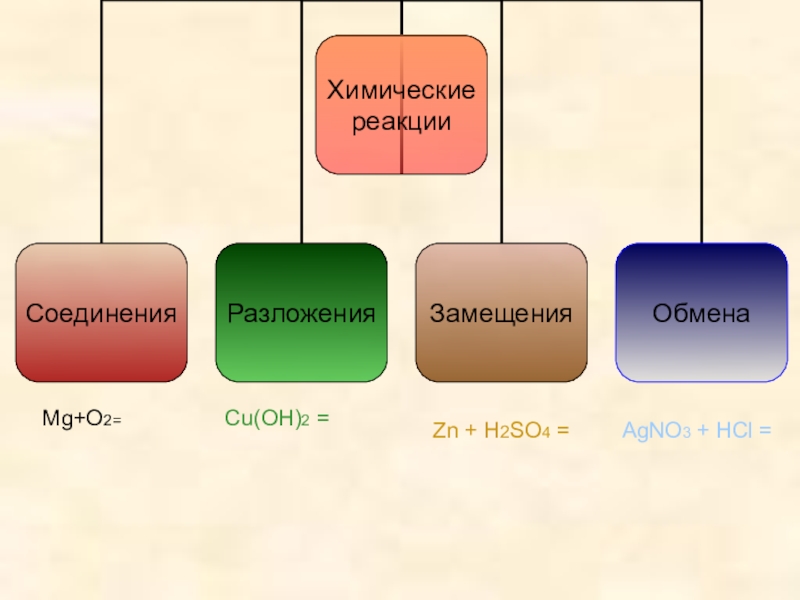
- 15. AgNO3 + HCl = Zn + H2SO4 =Cu(OH)2 = Mg+O2=
- 16. Расставьте коэффициенты и укажите тип реакции:_Zn +_H3PO4
- 17. Расставьте коэффициенты и укажите тип реакции:3Zn +2H3PO4
- 18. …Al +… O2 → …Al2O3 …P +
- 19. …Fe(OH)3 → Fe2O3 +… H2O …HgO →
- 20. CuCl2 + Fe → Cu + FeCl2
- 21. CuO + …HCl → CuCl2 + H2ОBaCl2
- 22. N2+ O2 = 2NO - Q2Mg+O2= 2MgO +Q
- 23. Типы химических реакций (по тепловому эффекту)
Слайд 2Эпиграф
«О, сколько нам открытий чудных
Готовят просвещенья дух,
И опыт, сын ошибок
И гений парадоксов друг…»
А.С.Пушкин
Девиз: «Per aspera ad astra» -
«Через тернии к звёздам».
Слайд 3Цели урока
Значение закона сохранения массы веществ
Количественное и качественное выражение закона –
Классификация химических реакций
Слайд 4Блеф-игра
Верите ли Вы, что …
Химические явления называют химическими превращениями или химическими
При химических реакциях исходные вещества превращаются в другие вещества, обладающие новыми свойствами. (_____).
Алхимики, внося вклад в развитие химии, создали философский камень. (_____).
В результате химических реакций масса веществ меняется, так как происходит соединение с «огненной материей». (____).
В результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка. (_____).
Условную запись химической реакции посредством химических знаков и формул называют химическим уравнением. (______).
Слайд 5Блеф-игра
Верите ли Вы, что …
Химические явления называют химическими превращениями или химическими
При химических реакциях исходные вещества превращаются в другие вещества, обладающие новыми свойствами. (Да).
Алхимики, внося вклад в развитие химии, создали философский камень. (Нет).
В результате химических реакций масса веществ меняется, так как происходит соединение с «огненной материей». (Нет).
В результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка. (Да).
Условную запись химической реакции посредством химических знаков и формул называют химическим уравнением. (Да).
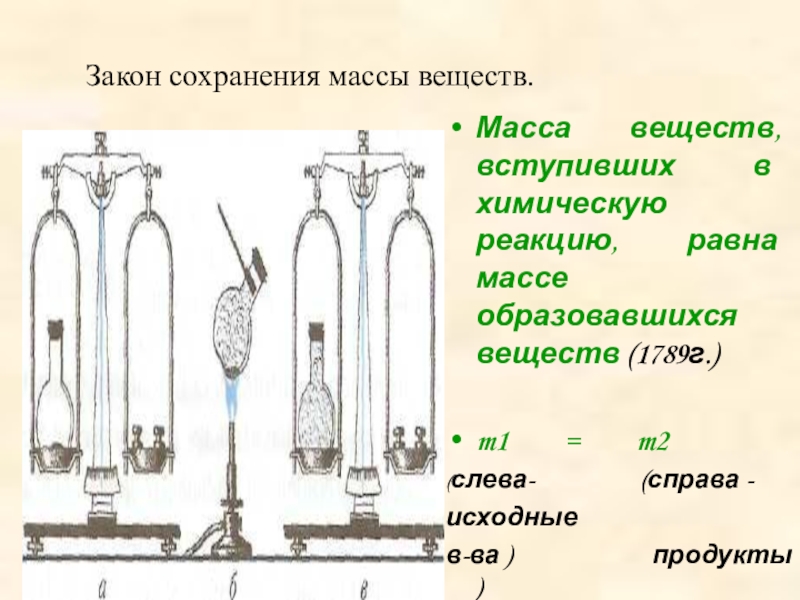
Слайд 6Закон сохранения массы веществ.
Эксперимент: в сосуде Ландольта (раздвоенная пробирка с
Слайд 8Закон сохранения массы веществ.
Масса веществ, вступивших в химическую реакцию, равна массе
m1 = m2
(слева- (справа -
исходные
в-ва ) продукты )
Слайд 9Химические уравнения.
Уравнения реакции составляют на основе закона сохранения массы веществ.
4P +
При составлении уравнения реакции слева и справа должно быть одинаковое число атомов.
Это достигается расстановкой коэффициентов перед формулами веществ.
Слайд 10Типы химических реакций
( по числу исходных и образующихся веществ)
Реакция соединения
Реакция разложения
Реакция
Реакция обмена
Слайд 11Реакция соединения
Получение воды:
2H2 + O2 = 2H2O
Реакция соединения – это
А + В = АВ
Слайд 12 Реакция разложения
Разложение воды :
2H2O = 2H2↑ + O2↑
Реакция
АВ → А + В
Слайд 13Реакция замещения
Вытеснение углеродом атомов водорода в молекуле воды:
Реакция замещения - это когда атомы простого вещества замещают атомы одного химического элемента в сложном веществе
АВ + С → СВ + А
Слайд 14Реакция обмена
Н2SО4 + 2NaOH
Реакция обмена – это реакция между двумя сложными веществами, при протекании которых они обмениваются своими составными частями
АВ + СD → СВ + АD
Слайд 16Расставьте коэффициенты и укажите тип реакции:
_Zn +_H3PO4 = Zn3(PO4)2 +_H2↑ р.
__H2 + N2 = __NH3 р. ____________
__NH3 = __H2↑ + N2↑ р. ____________
Слайд 17Расставьте коэффициенты и укажите тип реакции:
3Zn +2H3PO4 = Zn3(PO4)2 +3H2↑ р.замещения
3H2 + N2 = 2NH3 р. соединения
2NH3 = 3H2↑ + N2↑ р. разложения
Слайд 18…Al +… O2 → …Al2O3
…P + …O2 → …P2O5
Na2O
Li2O + H2O →… LiOH
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать процесс, который протекает?
Реакции соединения
Слайд 19…Fe(OH)3 → Fe2O3 +… H2O
…HgO → …Hg + O2
CaCO3
…NO → N2 + O2
Реакции разложения
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать процесс, который протекает?
Слайд 21CuO + …HCl → CuCl2 + H2О
BaCl2 + K2SO4 → BaSO4
Реакции обмена
Что объединяет все эти реакции?
В чём их отличие?
Как одним словом мы можем назвать процесс, который протекает?
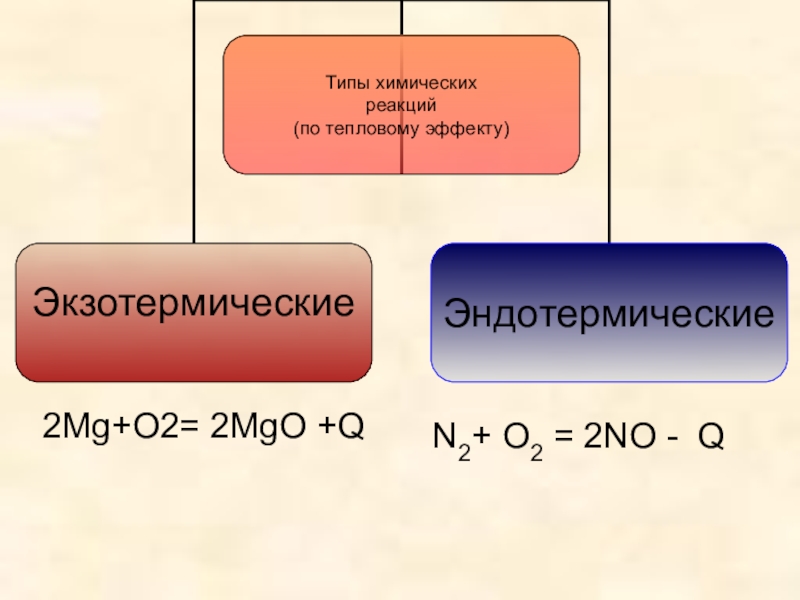
Слайд 23Типы химических реакций
(по тепловому эффекту)
Экзотермические - протекающие с выделением
2Mg + O2 = 2MgO + Q
Эндотермические - протекающие с поглощением теплоты
N2+ O2 = 2NO - 181кDж
N2+ O2 = 2NO - Q