- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Кислоты , соли и другие
Содержание
- 1. Презентация по химии на тему: Кислоты , соли и другие
- 2. КИСЛОТЫ
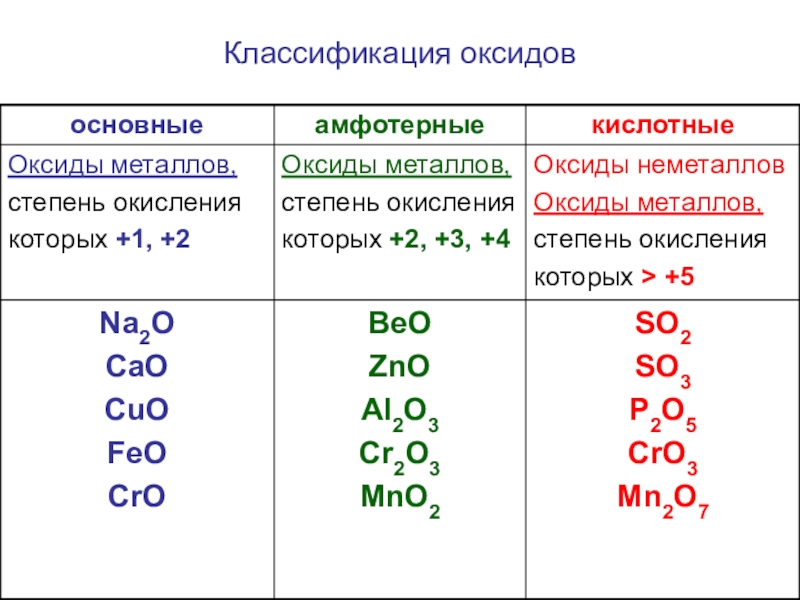
- 3. Классификация оксидов
- 4. 1. Кислотные свойства проявляет оксид:1) SiO2
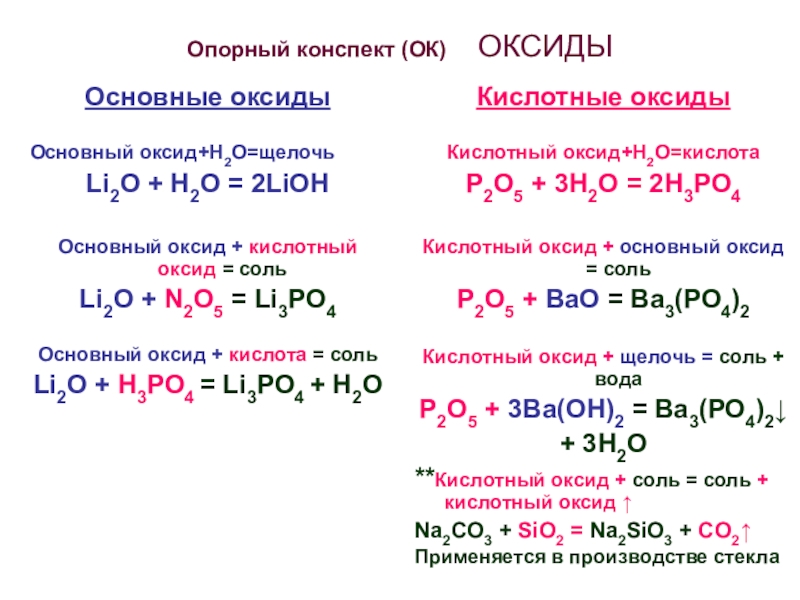
- 5. Опорный конспект (ОК) ОКСИДЫОсновные оксидыОсновный
- 6. Выберите из перечня веществ основный оксид.
- 7. Выберите из перечня веществ кислотный оксид.
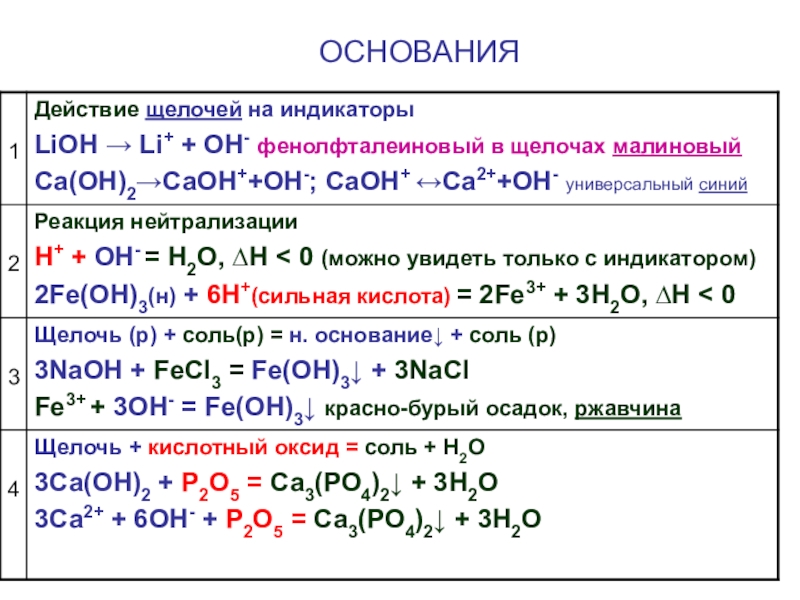
- 8. ОСНОВАНИЯ
- 9. Выберите из перечня веществ основание (щелочь).
- 10. Выберите из перечня веществ кислоту Напишите
- 11. 1. Наиболее сильные основные свойства проявляет гидроксид:1)
- 12. СОЛИ Все соли – ионные соединения, сильные электролиты
- 13. Выберите из перечня веществ соль Напишите
- 14. Генетическая связь неорганических веществМеталлОсновный оксидОснованиеСольНеметаллКислотный оксидКислотаСоль
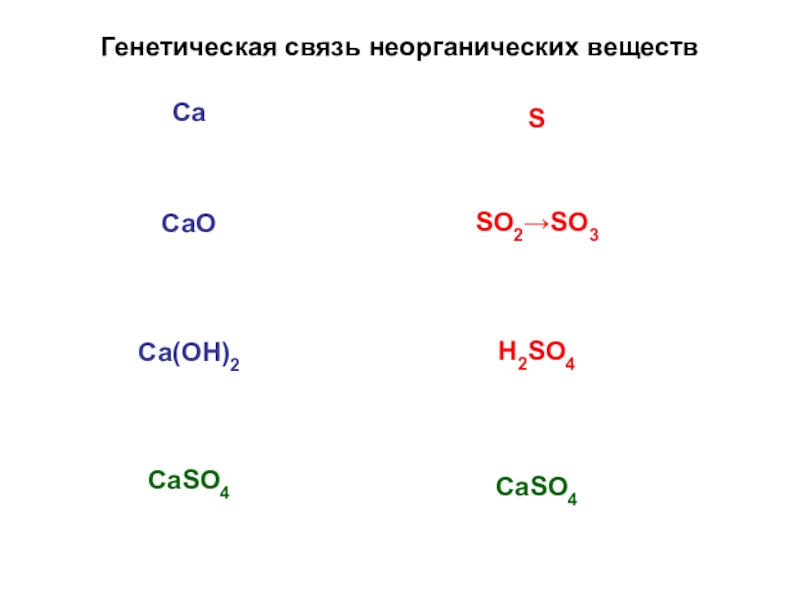
- 15. Генетическая связь неорганических веществСаСаОСа(ОН)2СаSО4SSO2→SO3H2SO4CaSO4
- 16. Реакции ионного обмена идут без изменения
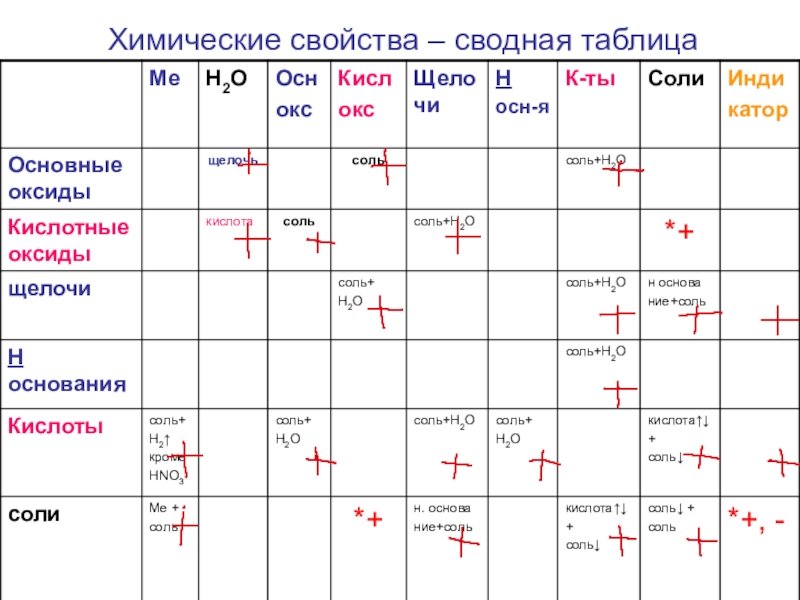
- 17. Химические свойства – сводная таблица
Слайд 1Химические свойства
опорные конспекты
Оксиды, основания, кислоты и соли
Выполнила учительница химии МБОУ СОШ
Талипова И.М.
Слайд 41. Кислотные свойства проявляет оксид:
1) SiO2
3. Установите соответствие между формулой вещества и классом соединений, к которому это вещество принадлежит:
А) оксид азота (II) 1) кислотный оксид
Б) оксид кальция 2) основный оксид
В) оксид серы (IV) 3) несолеобразующий оксид
Г) оксид углерода (II) 4) амфотерный оксид
2. Оксид с наиболее выраженными основными свойствами образует:
1) Be 2) Mg 3) Ba 4) Zn
Слайд 5Опорный конспект (ОК) ОКСИДЫ
Основные оксиды
Основный оксид+Н2О=щелочь
Li2O + H2O =
Основный оксид + кислотный оксид = соль
Li2O + N2O5 = Li3PO4
Основный оксид + кислота = соль
Li2O + Н3РО4 = Li3PO4 + Н2О
Кислотные оксиды
Кислотный оксид+Н2О=кислота
Р2О5 + 3Н2О = 2Н3РО4
Кислотный оксид + основный оксид = соль
Р2О5 + ВаО = Ва3(РО4)2
Кислотный оксид + щелочь = соль + вода
Р2О5 + 3Ва(ОН)2 = Ва3(РО4)2↓
+ 3Н2О
**Кислотный оксид + соль = соль + кислотный оксид ↑
Na2CO3 + SiO2 = Na2SiO3 + CO2↑
Применяется в производстве стекла
Слайд 6Выберите из перечня веществ основный оксид. Напишите для него уравнения возможных
Слайд 7Выберите из перечня веществ кислотный оксид. Напишите для него уравнения возможных
Слайд 9Выберите из перечня веществ основание (щелочь). Напишите для него уравнения возможных
Слайд 10Выберите из перечня веществ кислоту Напишите для нее уравнения возможных реакций с
Слайд 111. Наиболее сильные основные свойства проявляет гидроксид:
1) LiOH
2. Амфотерные свойства проявляют кислородные соединения:
1) бария 2) магния 3) кальция 4) бериллия
3.К двухосновным слабым кислородсодержащим кислотам относится:
1) HNO3 2) H2S 3) H2CO3 4) H2SO4
4. К слабым кислородсодержащим кислотам относится:
1) HNО3 2) HClO4 3) H2SiO3 4)H2S
Слайд 13Выберите из перечня веществ соль Напишите для нее уравнения возможных реакций с
Слайд 14Генетическая связь неорганических веществ
Металл
Основный оксид
Основание
Соль
Неметалл
Кислотный оксид
Кислота
Соль
Слайд 16Реакции ионного обмена идут
без изменения заряда ионов
В ионном виде не
слабые электролиты: Н2О, Н2СО3, HF, H2S, HNO2, H2SiO3, СН3СООН, NH4OH
Н2СО3 в продуктах записывают как Н2О + СО2↑
H2SO3 в продуктах Н2О+SО2↑
NH4OH в продуктах NH3↑+H2O
нерастворимые вещества (н)
малорастворимые вещества (м), если они – продукты, исключение Са(ОН)2 -щелочь
Оксиды – не электролиты
В ионном виде записывают:
растворимые вещества (р)
малорастворимые вещества (м), если они – реагенты