- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Кислоты (8 класс)
Содержание
- 1. Презентация по химии на тему Кислоты (8 класс)
- 2. Н NP S O C CI
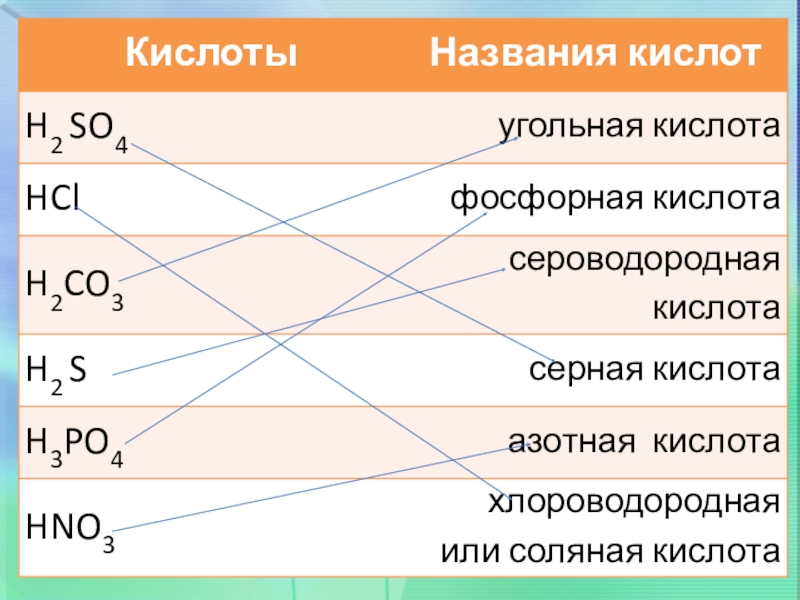
- 3. MgOCaOСа(OH)2K2ONa2OKOHNaOHLiOHHNO3 HClH2CO3 H3PO4 H2S H2SO4 Подумайте, к какой группе может относиться эти формулы
- 4. ОКСИДЫОСНОВАНИЯMgOCaOK2ONa2OСа(OH)2 NaOHKOHLiOH
- 5. Что нас объединяет?
- 6. Из своего жизненного опыта вы знаете, что
- 7. «Кислоты»Д/з. § 20 стр. 102- 107Упр. 4, 5
- 8. Серная кислота
- 9. Хлороводородная (соляная) кислота
- 10. H3BO3Борная кислота
- 11. Уксусная кислота
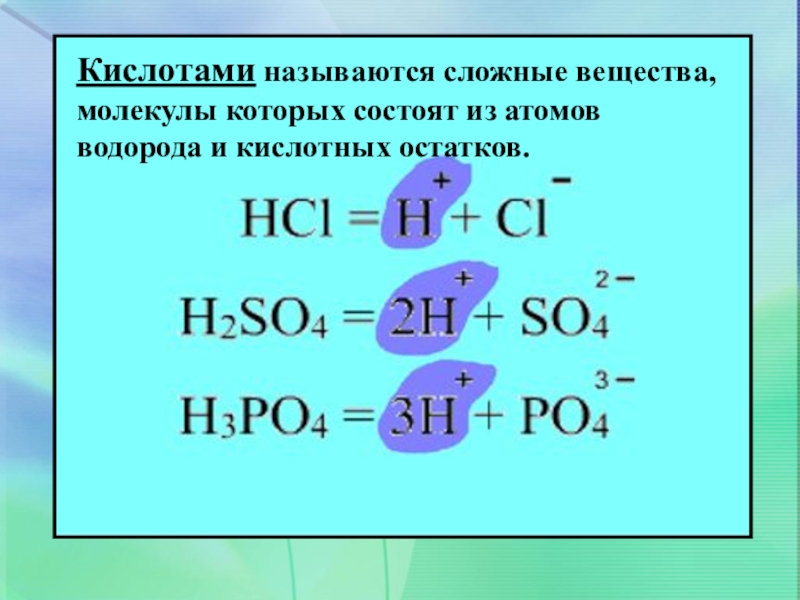
- 12. Кислотами называются сложные вещества, молекулы которых состоят из атомов водорода и кислотных остатков.
- 13. НхАn – общая формула
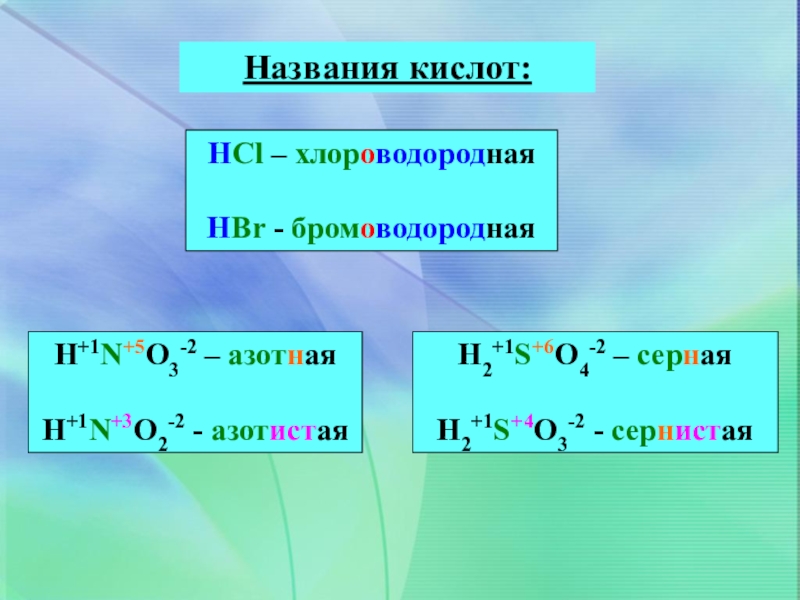
- 14. Названия кислот:HCl – хлороводородная HBr - бромоводороднаяH+1N+5O3-2 – азотнаяH+1N+3O2-2 - азотистаяH2+1S+6O4-2 – сернаяH2+1S+4O3-2 - сернистая
- 15. Слайд 15
- 16. По какому признаку кислоты разделены на группыHF
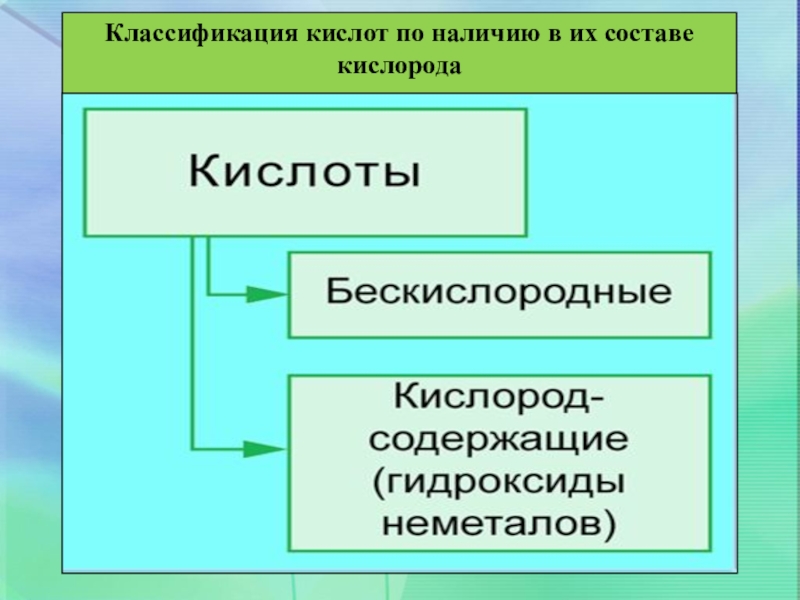
- 17. Классификация кислот по наличию в их составе кислорода
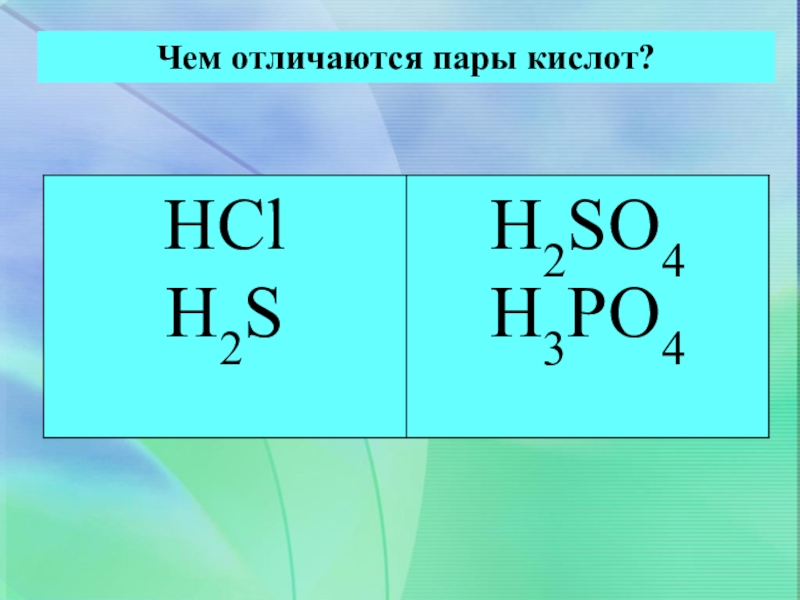
- 18. Чем отличаются пары кислот?
- 19. Классификация кислот
- 20. Характеристика кислотH2Sсероводородная, бескислородная, двухосновная, растворимаяHClO4хлорная, кислородсодержащая, одноосновная, растворимаяHFфтороводородная, бескислородная, одноосновная, растворимаяH3PO4фосфорная, кислородсодержащая, трехосновная, растворимая
- 21. Слайд 21
- 22. Обращаться осторожно! Работать
- 23. Слайд 23
- 24. Домашнее задание § 20 стр. 102- 107Упр. 4, 5.
Н NP S O C CI
Слайд 3MgO
CaO
Са(OH)2
K2O
Na2O
KOH
NaOH
LiOH
HNO3
HCl
H2CO3
H3PO4
H2S
H2SO4
Подумайте, к какой группе может относиться
эти формулы
Слайд 6Из своего жизненного опыта вы знаете, что многие продукты питания обладают
кислым вкусом. Кислый вкус этим продуктам придают кислоты. Кислый вкус лимону придает лимонная кислота, яблоку—яблочная кислота, скисшему молоку—молочная кислота. Щавель имеет кислый вкус благодаря наличию в его листьях щавелевой кислоты.
Слайд 12Кислотами называются сложные вещества, молекулы которых состоят из атомов водорода и
кислотных остатков.
Слайд 13 НхАn – общая формула кислот
Н -
атомы водорода
Аn – кислотный остаток
х – совпадает с валентностью
кислотного остатка
Аn – кислотный остаток
х – совпадает с валентностью
кислотного остатка
Слайд 14Названия кислот:
HCl – хлороводородная
HBr - бромоводородная
H+1N+5O3-2 – азотная
H+1N+3O2-2 - азотистая
H2+1S+6O4-2
– серная
H2+1S+4O3-2 - сернистая
H2+1S+4O3-2 - сернистая
Слайд 16
По какому признаку
кислоты разделены на группы
HF - фтороводородная
HCl -
хлороводородная
HBr - бромоводородная
HI - йодоводородная
H2S - сероводородная
HBr - бромоводородная
HI - йодоводородная
H2S - сероводородная
HNO3 - азотная
HNO2 - азотистая
HClO4 - хлорная
H2SO4 - серная
H2SO3 - сернистая
H2CO3 - угольная
H2SiO3- кремниевая
H3PO4 - фосфорная
H3BO3 - борная
Слайд 20Характеристика кислот
H2S
сероводородная, бескислородная, двухосновная, растворимая
HClO4
хлорная, кислородсодержащая, одноосновная, растворимая
HF
фтороводородная, бескислородная, одноосновная, растворимая
H3PO4
фосфорная,
кислородсодержащая,
трехосновная, растворимая
трехосновная, растворимая
Слайд 22Обращаться осторожно!
Работать в резиновых перчатках и
защитных очках!
Берегись ожога! Во избежание выбрызгивания и ожогов кислоту при сливании лить тонкой струей в воду, а не наоборот!
При попадании кислоты на кожу место поражения быстро промыть большим количеством воды.
Берегись ожога! Во избежание выбрызгивания и ожогов кислоту при сливании лить тонкой струей в воду, а не наоборот!
При попадании кислоты на кожу место поражения быстро промыть большим количеством воды.
ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ