- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему кислоты (8 класс)
Содержание
- 1. Презентация по химии на тему кислоты (8 класс)
- 2. HCl – соляная кислота H2S – Сероводородная
- 3. Бинарные кислоты Нсl и н2s в водных
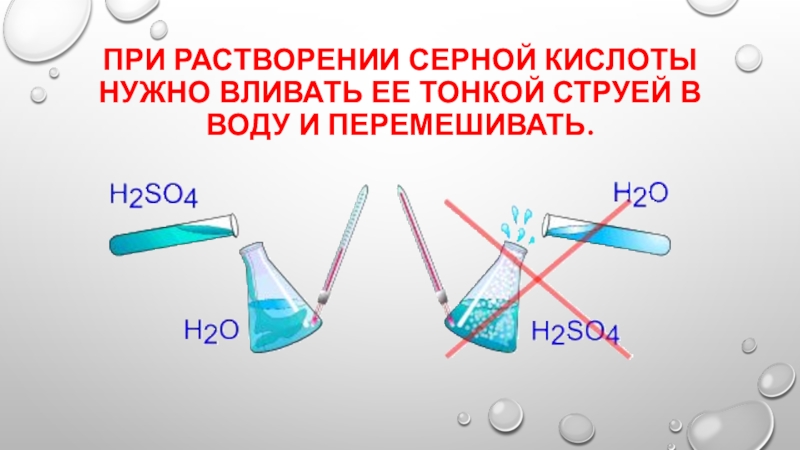
- 4. При растворении серной кислоты нужно вливать ее тонкой струей в воду и перемешивать.
- 5. Царская водка-смесь концентрированных азотной и соляной кислоты.
- 6. Интересно знать! случился во времена Второй мировой
- 7. Спасибо за внимание!
HCl – соляная кислота H2S – Сероводородная кислота HNO2 – азотистая кислота HNO3 - азотная кислота H2SO3 – сернистая кислота H2SO4 – серная кислота H2CO3 – угольная кислота H2SiO3 – кремниевая кислота H3PO4 – фосфорная кислота
Слайд 1Кислоты
Кислоты-сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка.
Слайд 2HCl – соляная кислота H2S – Сероводородная кислота HNO2 – азотистая кислота HNO3 -
азотная кислота
H2SO3 – сернистая кислота
H2SO4 – серная кислота
H2CO3 – угольная кислота
H2SiO3 – кремниевая кислота
H3PO4 – фосфорная кислота
Слайд 3Бинарные кислоты Нсl и н2s в водных растворах образуют простые ионы.
Остальные кислоты образуют сложные ионы.
Число атомов водорода в кислоте называют основностью.
Одноосновные: hcL, hno2, hno3.
ДВУХОСНОВНЫЕ: h2s, h2so3, h2so4, h2co3, h2sIo3.
ТРЕХОСНОВНЫЕ: h3po4.
ПО НАЛИЧИЮ КИСЛОРОДА
КИСЛОРОДОСОДЕРЖАЩИЕ: HNO2, HNO3, H2SO3, H2SO4, H2CO3, H2SIO3, H3PO4.
БЕСКИСЛОРОДНЫЕ: HCL, H2S.
Слайд 5Царская водка-смесь концентрированных азотной и соляной кислоты.
Благодаря сложной реакции между
азотной и соляной кислотой, рождается сила растворять металлы. Ей неподвластны тантал, иридий и родий. На вид царская водка просто жёлтая жидкость с резким неприятным запахом.
Слайд 6Интересно знать! случился во времена Второй мировой войны. В нацистской Германии было
запрещено получение Нобелевской премии. Поэтому два немецких физика (Макс фон Лауэ и Джеймс Франк) решили оставить на хранение свои золотые медали в Институте Нильса Бора (Дания). Когда Дания была оккупирована, один из химиков института растворил золотые медали в водке. Банка с раствором простояла всю войну среди сотен других различных растворов. После окончания войны, этот же химик выделил золото обратно из раствора и отдал его Шведской академии наук и Нобелевскому фонду. Из полученного золота изготовили новые медали и отдали их Джеймсу Франку и Максу фон Лауэ.