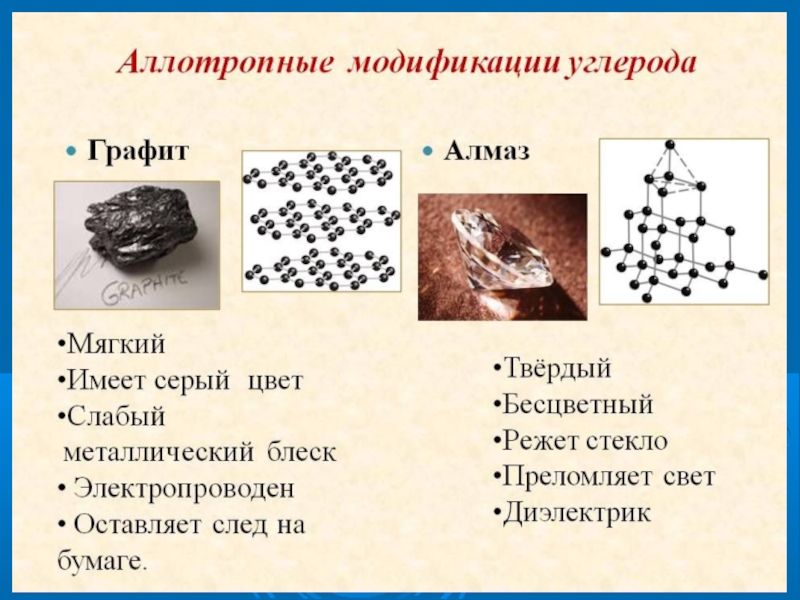
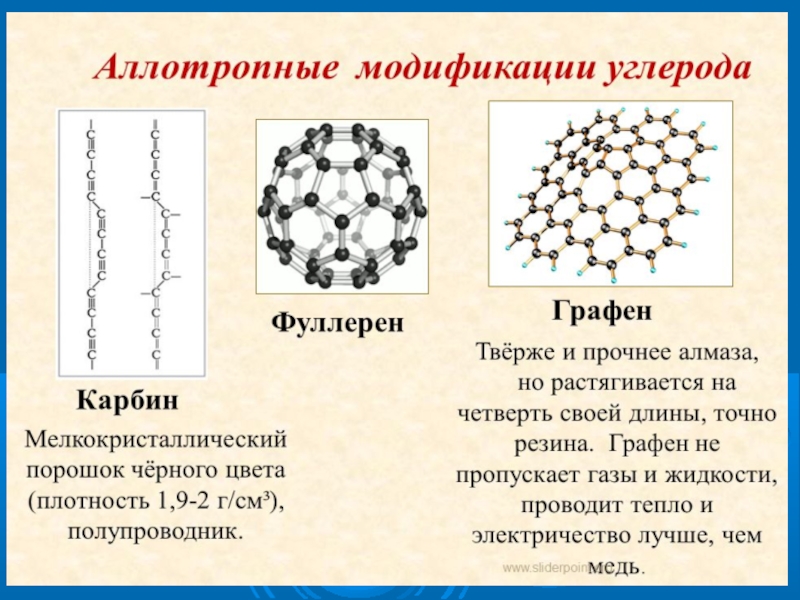
и его разновидностях идёт речь? Он имеет несколько аллотропных модификаций, бывает мягким и хрупким, серым и малопривлекательным, а может быть очень твёрдым и сверкающим.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Кислородные соединения углерода (9 класс)
Содержание
- 1. Презентация по химии на тему Кислородные соединения углерода (9 класс)
- 2. Слайд 2
- 3. Слайд 3
- 4. Слайд 4
- 5. Кислородные соединения углерода Химик не такой должен
- 6. ПОЧЕМУ ОБРАЗУЕТСЯ ПЕНА?
- 7. Исторический факт из жизни Клеопатры: «Она вынула
- 8. В результате какой химической
- 9. При содержании 0,08 % этого газа во
- 10. Каждый из живущих вблизи Неаполя хоть
- 11. Как очистить чайник от накипи?
- 12. Угарный газ (СО)содержится в выхлопных газах автомобилей
- 13. Воздух, окутывающий Землю, содержит около 3 млрд. т. СО2
- 14. План изучения веществСостав качественный и количественныйТип связиФизические свойстваХимические свойстваПолучениеПрименение
- 15. Сравнительная характеристика СО и СО2
- 16. Качественный составСОУглерод и кислородСО2Углерод и кислород
- 17. Количественный составСО1 атом углерода и 1 атом кислородаСО2 1 атом углерода и 2 атома кислорода
- 18. Тип связиСОКовалентная полярнаяС≡ОСО2Ковалентная полярнаяО=С=О
- 19. Физические свойстваСОГазБез цвета, без запаха, без вкусаМалорастворим
- 20. Горение угарного газа
- 21. Химические свойстваСОГорит1) 2СО+О2→→ 2СО22) FeO+СО→
- 22. ПолучениеСОВзаимо-действие углекислого газа с раскаленным углем
- 23. ПрименениеСОВ качестве топливаСО2
- 24. «Сухой лед» для хранения мороженного
- 25. Для тушения пожаров
- 26. Создание «дыма» на сцене
- 27. Производство газированных напитков
- 28. Слайд 28
- 29. Угольная кислота (Н2СО3 )Кислородосодержащая, нестойкая кислота, легко
- 30. Соли угольной кислотыКарбонаты( CaCO3, Na2CO3)Гидрокарбонаты(Ca(HCO3)2, NaHCO3)
Кислородные соединения углерода Химик не такой должен быть, который дальше дымуи пеплу ничего не видит, а такой, который на основанииопытных данных может делать теоретические выводы. М.В. Ломоносов
Слайд 5Кислородные соединения углерода
Химик не такой должен быть, который дальше дыму
и
пеплу ничего не видит, а такой, который на основании
опытных данных может делать теоретические выводы.
М.В. Ломоносов
опытных данных может делать теоретические выводы.
М.В. Ломоносов
Слайд 7Исторический факт из жизни Клеопатры: «Она вынула из шкатулки одну из
жемчужин и бросила её в яблочный уксус. Потрясенные гости, наблюдали, как дорогая жемчужина медленно растворяется с выделением пузырьков бесцветного газа. Когда от нее не осталось и следа, Клеопатра подняла кубок, покрутила его, взбалтывая полученный эликсир, и выпила весь до последней капли».
О какой химической реакции идёт речь??
О какой химической реакции идёт речь??
Слайд 9При содержании 0,08 % этого газа во вдыхаемом воздухе человек чувствует
головную боль и удушье. При повышении его концентрации до 0,32 % возникает паралич и потеря сознания (смерть наступает через 30 минут). При концентрации выше 1,2 % сознание теряется после двух—трёх вдохов, человек умирает менее чем через 3 минуты.
О каком газе идёт речь?
О каком газе идёт речь?
Слайд 10 Каждый из живущих вблизи Неаполя хоть раз слышал о Собачьей
пещере (Grotta del Cane), а многие и бывали в ней. Слава пещеры построена на костях собак, принадлежащих слишком любопытным владельцам. Человек мог беспрепятственно войти в неё и выйти, а его четвероногий спутник – нет. И чем дольше животное находилось в пещере, тем больше был шанс, что оно погибнет. Это место известно с давних пор. В XX веке люди поговаривали о злых духах, скрывающихся от солнечного света во мраке подземелья, что душили собак. В чём-то суеверия были верны. Собаки и правда были задушены, но не нечистой силой, а природной аномалией.
Слайд 14План изучения веществ
Состав качественный и количественный
Тип связи
Физические свойства
Химические свойства
Получение
Применение
Слайд 17Количественный состав
СО
1 атом углерода и 1 атом кислорода
СО2
1 атом углерода
и 2 атома кислорода
Слайд 19Физические свойства
СО
Газ
Без цвета,
без запаха,
без вкуса
Малорастворим в воде
Ядовит
СО2
Газ
Без цвета,
без
запаха,
имеет слегка кисловатый вкус
Растворяется в воде
имеет слегка кисловатый вкус
Растворяется в воде
Слайд 21Химические свойства
СО
Горит
1) 2СО+О2→
→ 2СО2
2) FeO+СО→
→Fe+CO2
СО2
Не
горит
1) СО2+Na2O→
→ Na2CO3
2) СО2+Ca(OH)2 →
→ CaCO3+H2O
3) СО2 + H2O ↔
↔ H2CO3
1) СО2+Na2O→
→ Na2CO3
2) СО2+Ca(OH)2 →
→ CaCO3+H2O
3) СО2 + H2O ↔
↔ H2CO3
Слайд 22Получение
СО
Взаимо-действие углекислого газа с раскаленным углем
СО2+С→2СО
СО2
CaCO3→
→ СaO+CO2↑
CaCO3+2HCl →
→ CaCl2+H2O+
+CO2↑
Слайд 29Угольная кислота (Н2СО3 )
Кислородосодержащая, нестойкая кислота, легко разлагается на исходные компоненты
– углекислый газ и воду:
Н2СО3↔СО2+ Н2О
Н2СО3↔СО2+ Н2О