- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Ионная связь.Металлическая и водородная связь (10 класс)
Содержание
- 1. Презентация по химии на тему Ионная связь.Металлическая и водородная связь (10 класс)
- 2. В результате изучения темы, вы будете способны:1.Объяснять
- 3. Определите элемент и назовите он является Ме
- 4. 1.Электроотрицательность - это …….2.Ковалентная полярная связь –
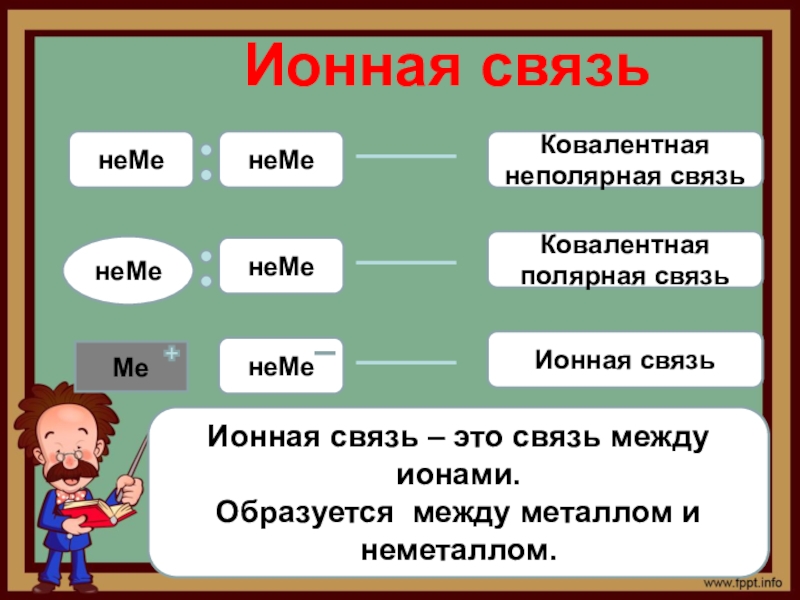
- 5. Ионная связьнеМенеМеКовалентная неполярная связьнеМенеМенеМеКовалентная полярная связьМеИонная связьИонная
- 6. Что происходит между атомами при отдаче и принятии электронов?
- 7. Me0 – nē → Me+nнеMe0 +
- 8. А что происходит между противоположно заряженными частицами – ионами?
- 9. В результате этого притяжения возникает ионная
- 10. Химическая связь, образующуюся между ионами, называется ионной.
- 11. Частица, отдающая электроны, превращается в положительный ион
- 12. КАТИОНЫАНИОНЫ+-Для двух подруг подарков грузВзвалил cебе Ион
- 13. Слайд 13
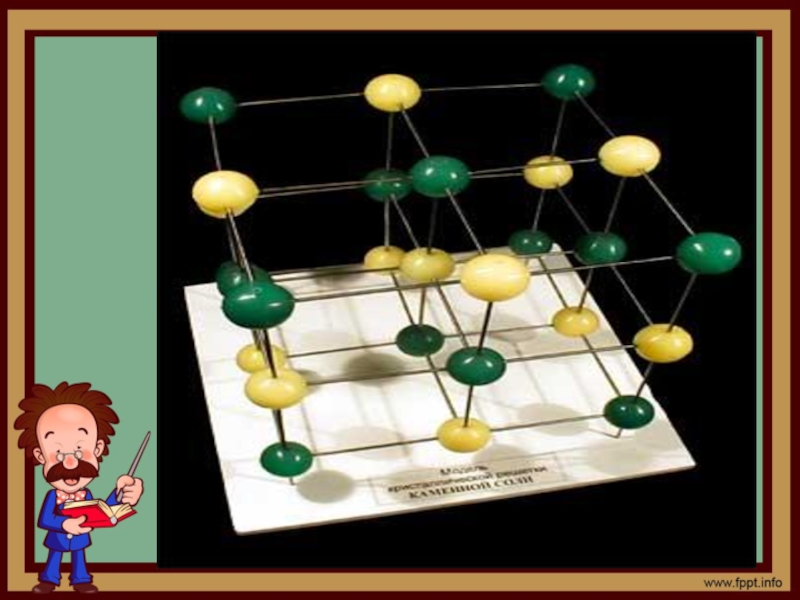
- 14. Ионными называются кристаллические решетки ,в узлах которых
- 15. Алгоритм записи схемы образования ионной связи.
- 16. Слайд 16
- 17. Итак, в большом 7 доме на 2
- 18. Но натрий не так-то легко было уговорить.
- 19. Путь к вершине химической пирамиды – ионная
- 20. Водородная связьO H…..O H…..O
- 21. Металлическая связьсвязь в металлах и сплавах, которую
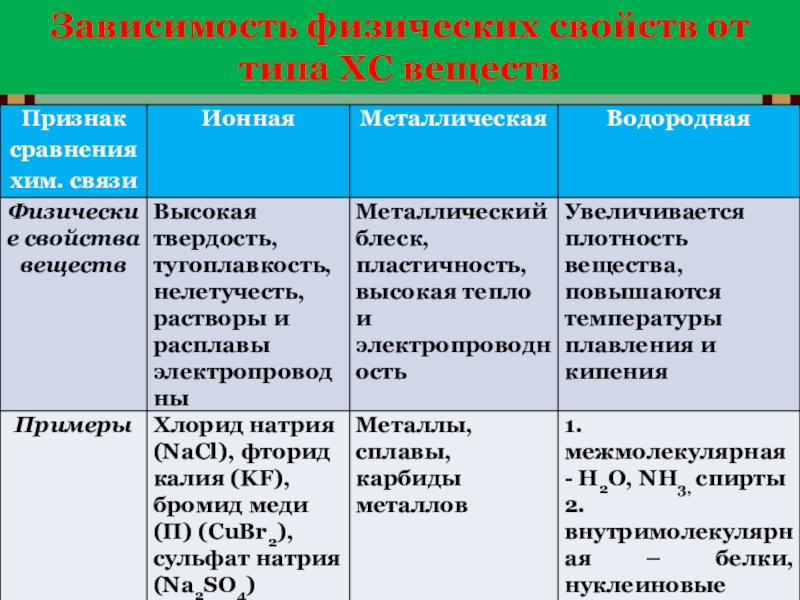
- 22. Зависимость физических свойств от типа ХС веществ
- 23. 1.В веществе PH₃ химическая связь:
- 24. 3. В каком соединении наименее полярная связь?
- 25. РефлексияКакова цель нашего урока?Достигли ли мы цели?Что представляло наибольшую трудность?
- 26. Домашнее заданиеРазобрать и выучить конспект.Повторить материал темы №3Подготовиться к КЗ
Слайд 1Ионная,
металлическая и водородная
химическая связь
10 класс
Бозаджи Н.М.
преподаватель химии,
высшая
Слайд 2
В результате изучения темы, вы будете способны:
1.Объяснять на конкретных примерах
механизмы
2. Рассматривать механизм образования
водородной связи.
3. Рассматривать механизм образования
металлической связи.
7.Осуществлять рефлексию своей деятельности.
Слайд 41.Электроотрицательность - это …….
2.Ковалентная полярная связь – это …..
3.Ковалентная неполярная связь
4.Какую кристаллическую решетку имеют вещества с ковалентным типом связи?
5.Из списка веществ назовите вещества с ковалентной а)неполярной и
б)полярной связью:
O2, Br2, H2,
HCl,
H 2S,
PCl3,
Слайд 5Ионная связь
неМе
неМе
Ковалентная неполярная связь
неМе
неМе
неМе
Ковалентная полярная связь
Ме
Ионная связь
Ионная связь – это связь
Образуется между металлом и неметаллом.
Слайд 7 Me0 – nē → Me+n
неMe0 + nē → неMe-n
При отдаче
При принятии ē атом неМе превращается в ион неМе
Слайд 9 В результате этого притяжения возникает ионная химическая связь – связь
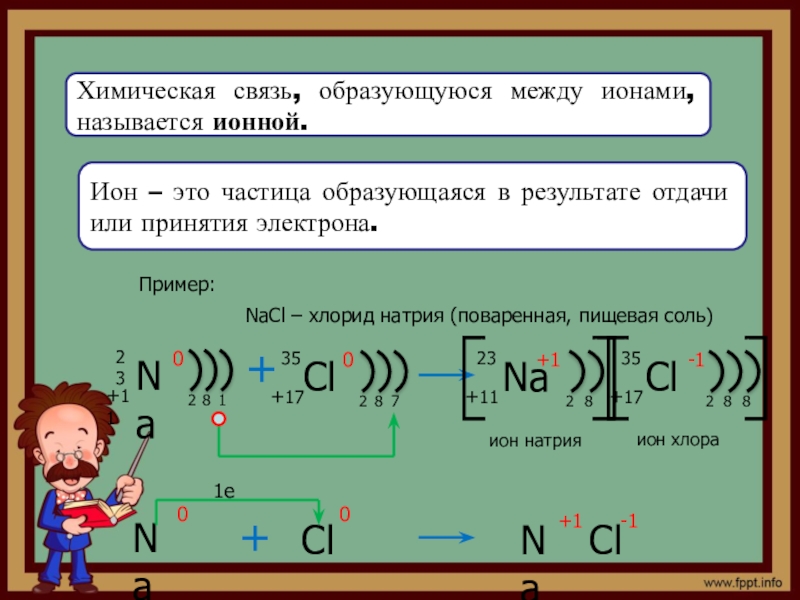
Слайд 10Химическая связь, образующуюся между ионами, называется ионной.
Ион – это частица
Пример:
NaCl – хлорид натрия (поваренная, пищевая соль)
+
1e
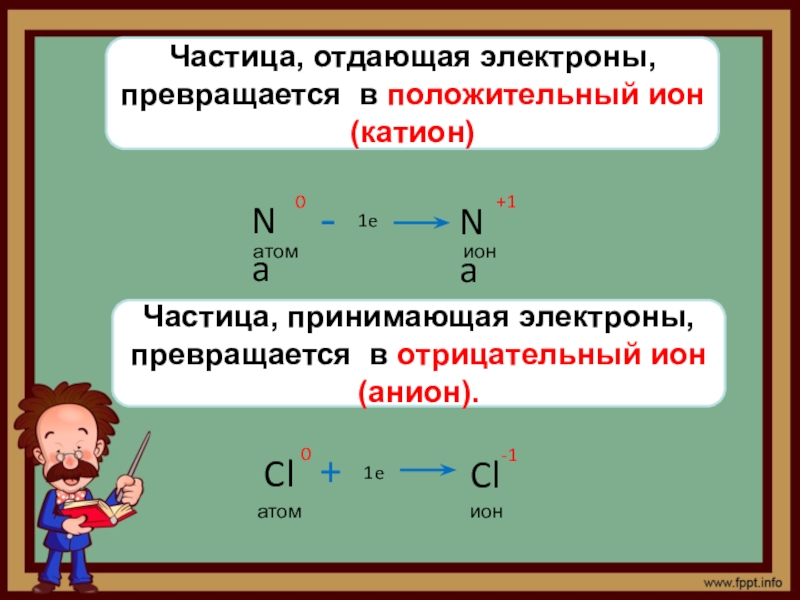
Слайд 11Частица, отдающая электроны,
превращается в положительный ион (катион)
Частица, принимающая электроны,
превращается в отрицательный ион (анион).
Слайд 12
КАТИОНЫ
АНИОНЫ
+
-
Для двух подруг подарков груз
Взвалил cебе Ион на плечи
Для Кати он
Для Ани он несет свой минус(-)
Слайд 14Ионными называются кристаллические решетки ,в узлах которых находятся чередуясь положительно и
Слайд 15
Алгоритм записи схемы образования ионной связи.
1.Составить схему строения и электронные формулы
2. Определить принадлежность элементов к металлам и неметаллам.
3.Составить схему перехода электронов и образования ионов.
4.Составить ионное соединение.
Слайд 17Итак, в большом 7 доме на 2 этаже ж
ил-был фтор. И
заветная мечта. Очень завидовал он неону – благородному газу, у которого былзавершен второй энергетический уровень. Всего одного электрона не
хватало фтору для полного счастья.
Вот и решил наш герой, во что бы то ни стало заполучить этот недостающий электрон. И вот однажды встретил фтор натрий, у которого на последнем
энергетическом уровне был один электрон. Он попросил отдать или
подарить ему его.
Слайд 18Но натрий не так-то легко было уговорить.
Что ты, я тоже
7 электронов, и я стану похожим на аргон! - сказал натрий.
Тут фтор решил прибегнуть к хитрости: «Давай объединим
свои электроны, и, когда они будут общими, я стану похожим на неон, а ты на аргон».
Так они и порешили.
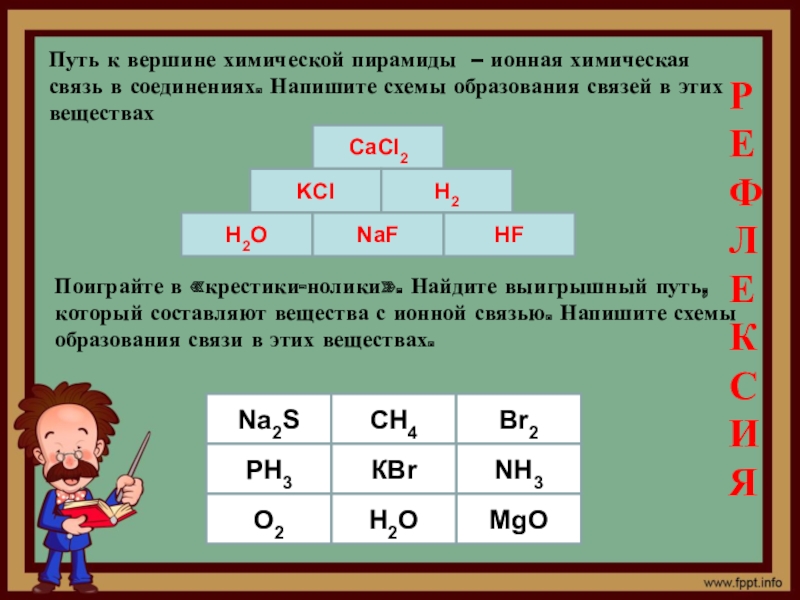
Слайд 19Путь к вершине химической пирамиды – ионная химическая связь в соединениях.
СаCl2
KCl
H2
H2O
NaF
HF
Поиграйте в «крестики-нолики». Найдите выигрышный путь, который составляют вещества с ионной связью. Напишите схемы образования связи в этих веществах.
Na2S
CH4
Br2
NH3
MgO
КBr
H2O
PH3
O2
Р
Е
Ф
Л
Е
К
С
И
Я
Слайд 20Водородная связь
O H…..O H…..O H….
H
Химическая связь между положительно поляризованными атомами водорода одной молекулы (или ее части)и отрицательно поляризованными атомами сильно
электроотрицательных элементов,
имеющих неподеленные электронные пары (F, О, N и реже С1 и S) другой молекулы (или ее части)
Слайд 21Металлическая связь
связь в металлах и сплавах, которую выполняют относительно свободные электроны
о п+
М — пе М
Схема образования металлической связи:
Задание:
Выпишите формулы веществ, в которых присутствует металлическая и водородная связи Na, KF, NH3, C2H2, CH3-COOH, H2S, AL,NaCL.
Слайд 231.В веществе PH₃ химическая связь:
а) ионная б)
в) ков. неполярная
б
2.Составьте формулу оксида
углерода(IV) и определите вид химической связи в ней,
а также охарактеризуйте связи.
CO₂ - ковалентная полярная
две = связи(пи и сигма)
Оценочная рефлексия
Слайд 243. В каком соединении наименее полярная связь?
а) метан - CH₄
4. Укажите кратность связи в молекуле азота
и хлора.
5. Укажите вещества с ионной и ковалентной
полярной связью:
а) Cl₂ и LiF б) MgCl₂ и H₂O
в) SO₃ и H₂O г) Na и K₂O
6.В какой молекуле наиболее прочная связь?
а) F₂ б) Cl₂ в) O₂ г) N₂
а
3, 1
б
г