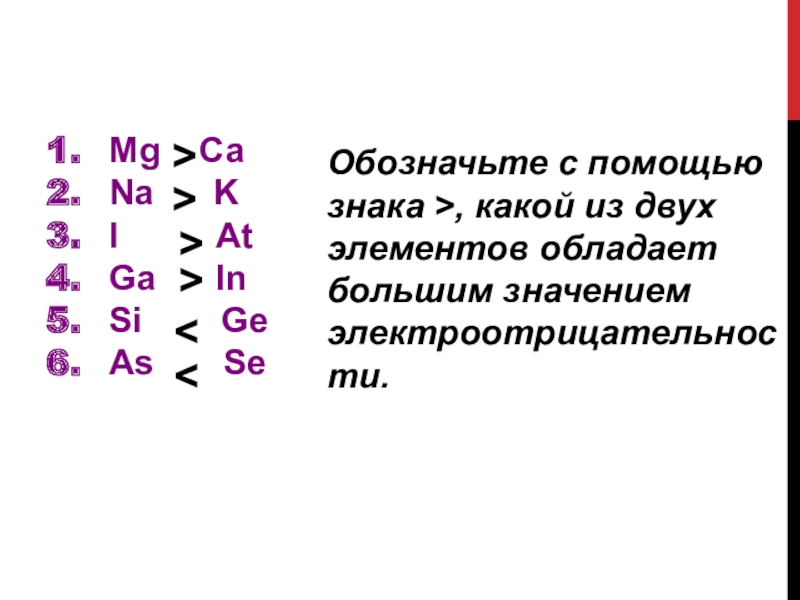
Mg Ca
Na K
I At
Ga In
Si Ge
As Se
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Химическая связь
Содержание
- 1. Презентация по химии на тему Химическая связь
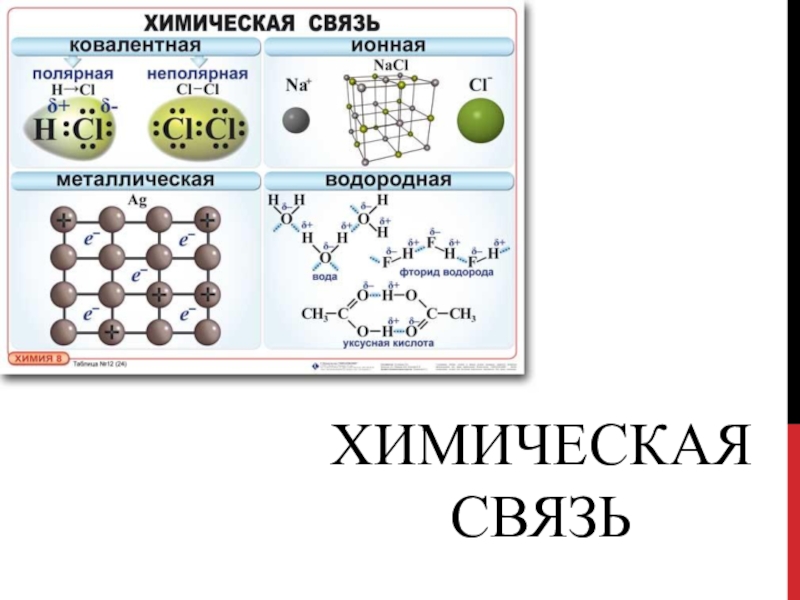
- 2. ХИМИЧЕСКая СВЯЗь
- 3. Цель урока:Сформировать представление о природе химической связи.Определить
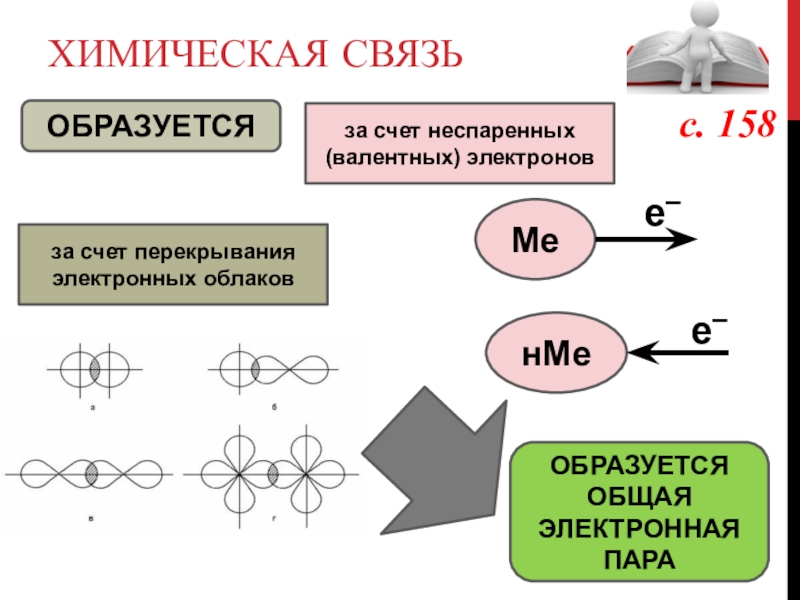
- 4. ХИМИЧЕСКАЯ СВЯзьс. 158ОБРАЗУЕТСЯза счет неспаренных (валентных) электроновза счет перекрывания электронных облаковМенМее‾е‾ОБРАЗУЕТСЯ ОБЩАЯ ЭЛЕКТРОННАЯ ПАРА
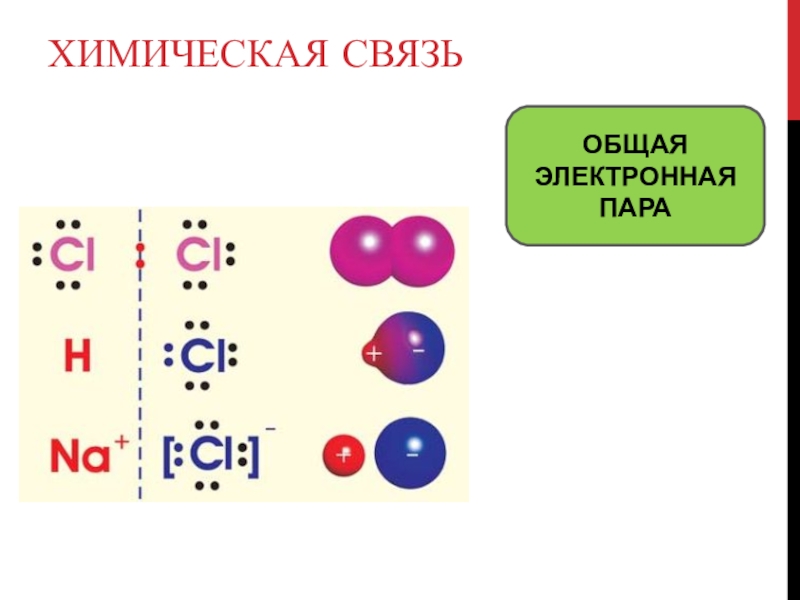
- 5. ХИМИЧЕСКАЯ СВЯзьОБЩАЯ ЭЛЕКТРОННАЯ ПАРА
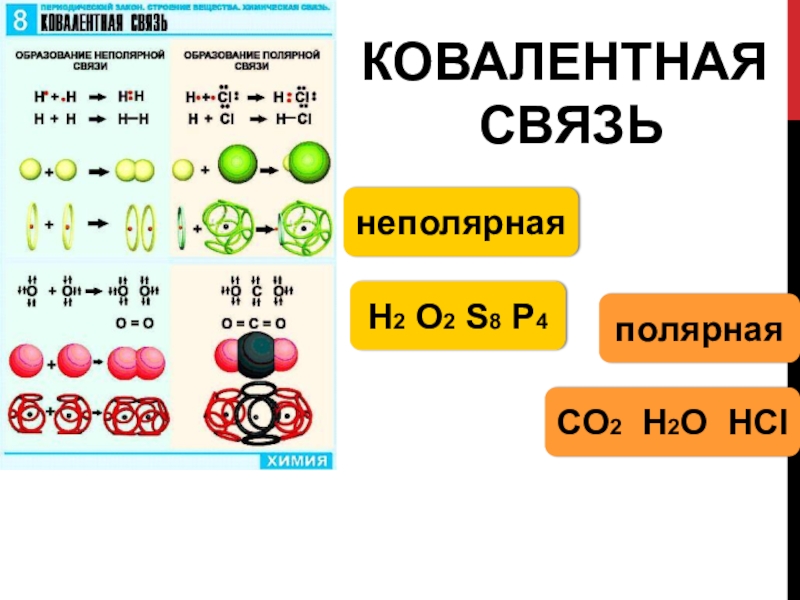
- 6. КОВАЛЕНТНАЯ СВЯЗЬнеполярнаяполярнаяН2 О2 S8 P4CO2 H2O HCl
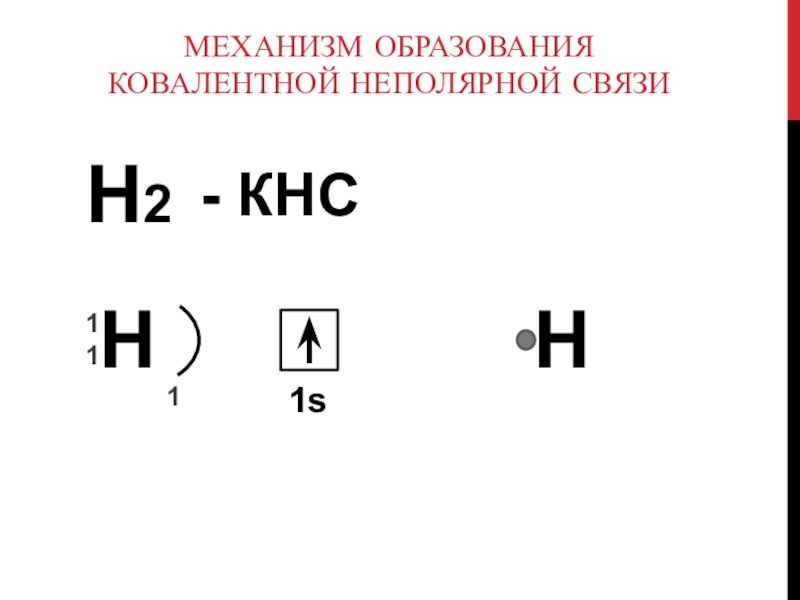
- 7. Механизм образования ковалентной неполярной связиH2- КHСH1111sH
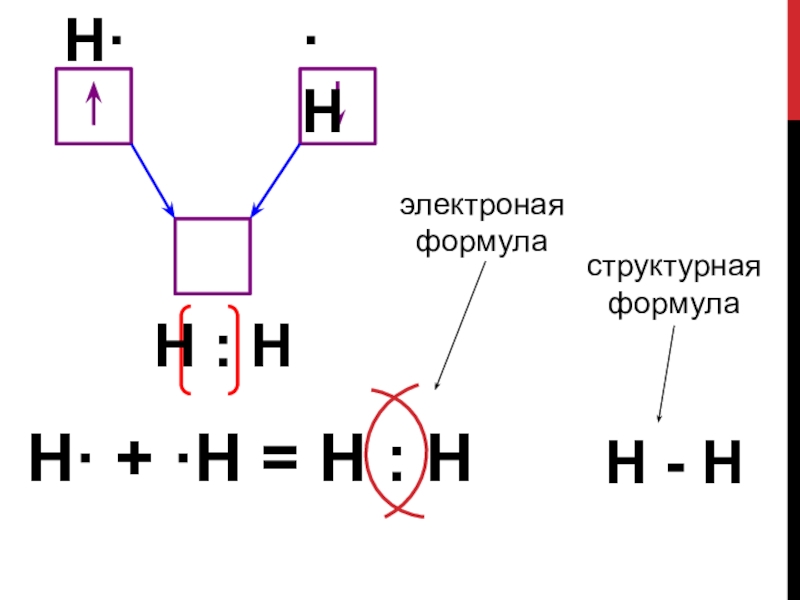
- 8. H· + ·Н = Н : Н
- 9. Характеристика связи1. Устанавливается между двумя …………
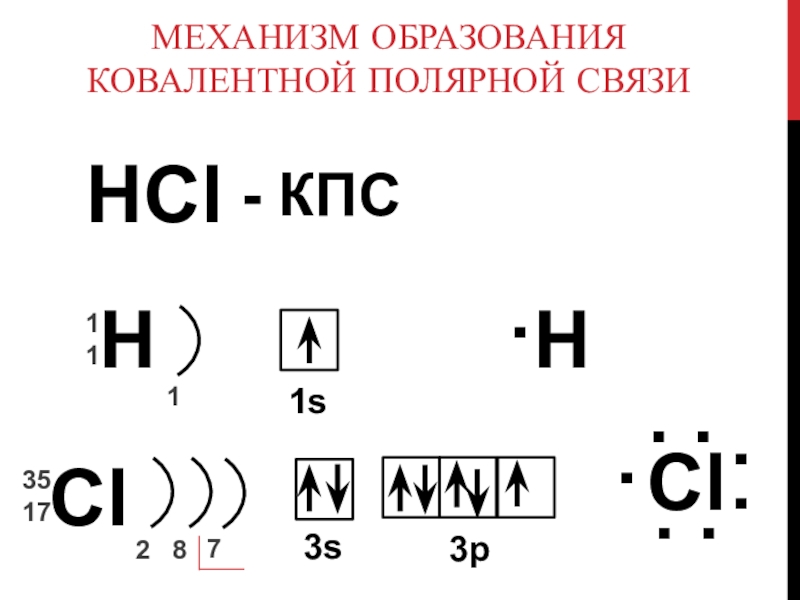
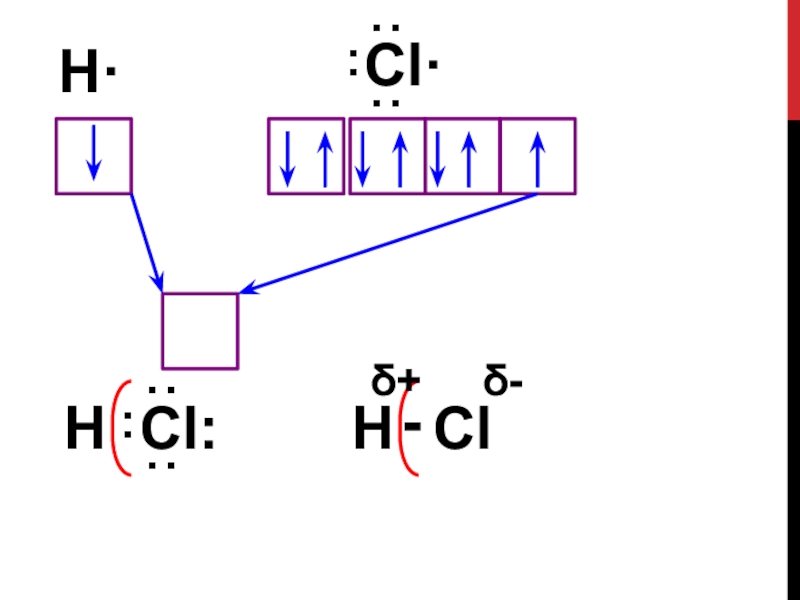
- 10. Механизм образования ковалентной полярной связиHCl- КПСH1111sHCl35172873s3рCl∙∙:::
- 11. H·
- 12. Характеристика связиКПС1. Устанавливается между двумя …………
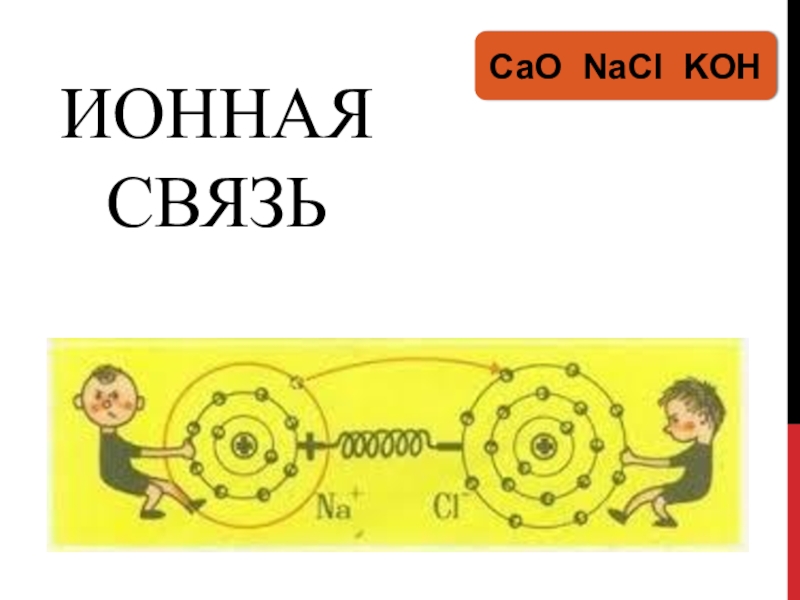
- 13. Ионная связьCаO NaCl KOH
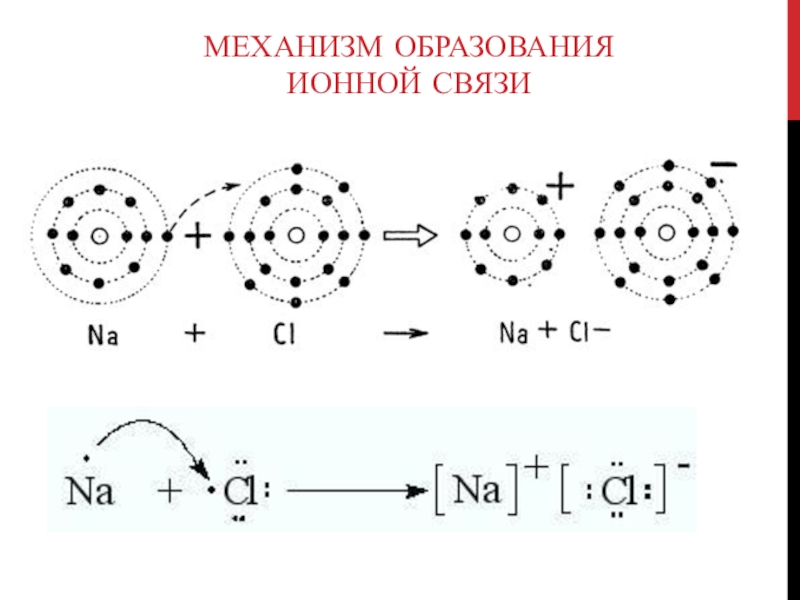
- 14. Механизм образования ионной связи
- 15. Характеристика связиИС1. Устанавливается между атомами …….
- 16. Металлическая связьвид химической связи, которую осуществляют относительно
- 17. Водородная связь – тип химической связи, при
- 18. Домашнее задание§ 7,8Упр.3, с. 34Тест 1-2, с. 37
Слайд 1Обозначьте с помощью знака >, какой из двух элементов обладает большим
Слайд 3Цель урока:
Сформировать представление о природе химической связи.
Определить условия возникновения химической связи.
Ознакомиться
Рассмотреть механизм образования разных типов химической связи.
Слайд 4ХИМИЧЕСКАЯ СВЯзь
с. 158
ОБРАЗУЕТСЯ
за счет неспаренных (валентных) электронов
за счет перекрывания электронных облаков
Ме
нМе
е‾
е‾
ОБРАЗУЕТСЯ
Слайд 9Характеристика связи
1. Устанавливается между двумя …………
атомами нМе
КHС
2. Устанавливается между атомами элементов
с …………. электроотрицательностью.
3. Устанавливается за счет образования ……….
электронных пар.
4. Электронная пара в …….. степени принадлежит
обоим атомам.
5. Молекула неполярна .
Слайд 12Характеристика связи
КПС
1. Устанавливается между двумя …………
атомами нМе
2. Устанавливается между атомами элементов,
электроотрицательность которых отличается …..
3. Устанавливается за счет образования ……….
электронных пар.
4. Электронная пара смещена в сторону …………
электроотрицательного элемента.
5. Молекула полярна .
Слайд 15Характеристика связи
ИС
1. Устанавливается между атомами ……. и …….
3. Устанавливается за
2. Связь между ………..
4. Электронная пара …….. смещена к атому …….
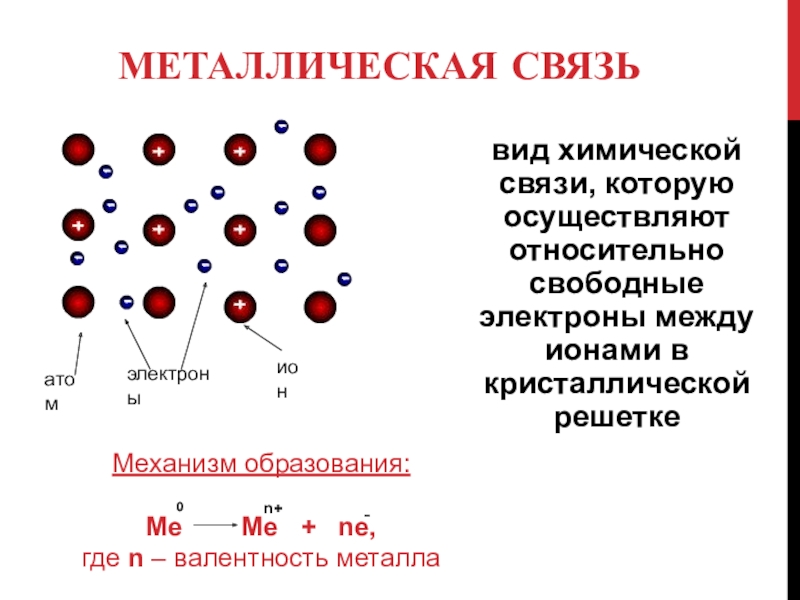
Слайд 16Металлическая связь
вид химической связи, которую осуществляют относительно свободные электроны между ионами
Механизм образования:
Ме Ме + nе,
где n – валентность металла
-
n+
0
атом
ион
электроны
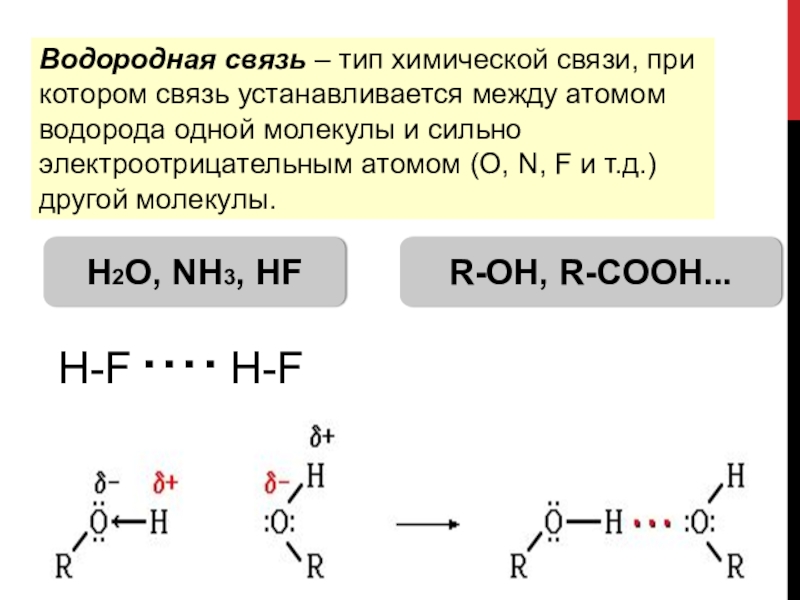
Слайд 17Водородная связь – тип химической связи, при котором связь устанавливается между
Н2О, NH3, HF
R-OH, R-COOH...
Н-F H-F
....