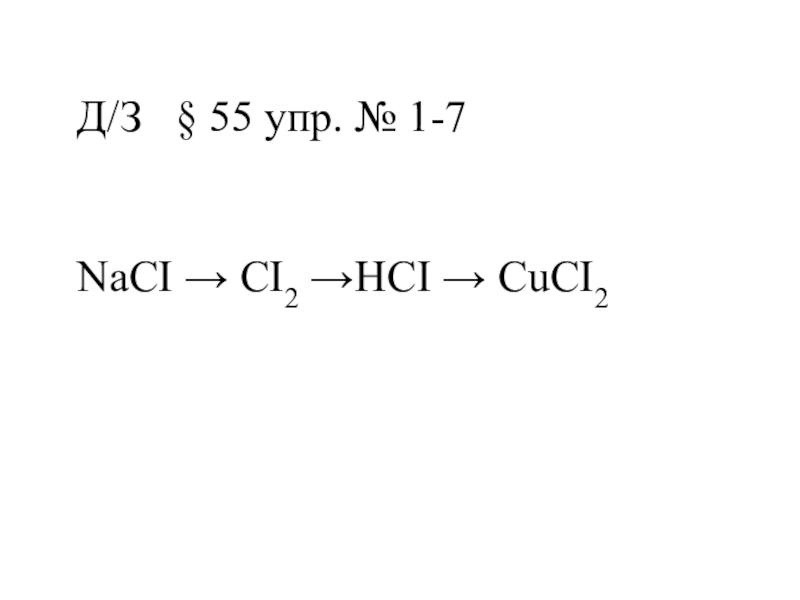- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Галогены
Содержание
- 1. Презентация по химии на тему Галогены
- 2. План урокаПоложение галогенов в ПСХЭ Д.И. Менделеева.Строение
- 3. 9F17CI35Br53IЭлементы 2 периода, VII А(галогены)85Аt+927…2s22р5+17…3s23р5+532818187…5s25р582187+35…4s24р5287- радиоактивный элемент1.
- 4. Слайд 4
- 5. Нахождение в природефлюорит (плавиковый шпат)галит (КСI·NаСI)сильвинитбишофит
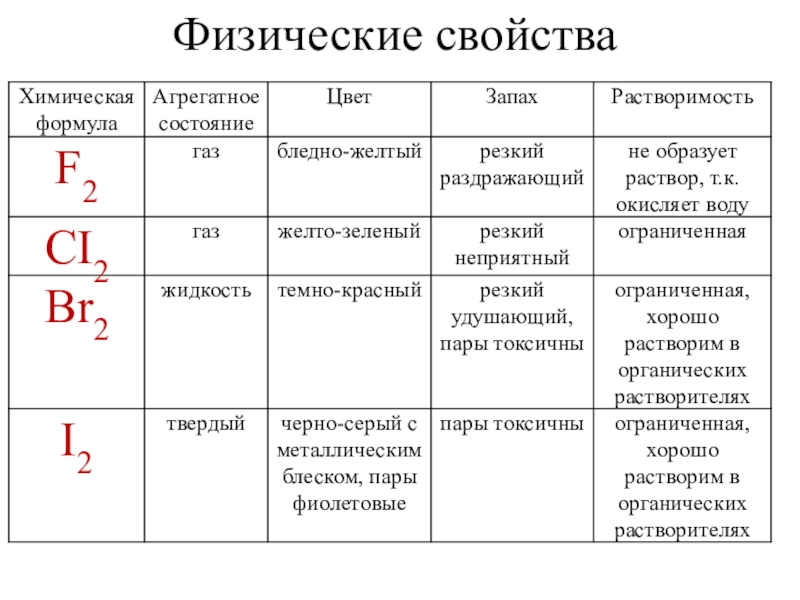
- 6. Физические свойства
- 7. F2СI2Вr2I2
- 8. 1. Взаимодействие с металлами2 Na + CI2
- 9. 2. Взаимодействие с водородомН2 + Г2 =
- 10. 3. Взаимодействие с неметаллами2Р + 3CI2 = 2РCI3 + Q2Р + 3Br2 = 2РBr3
- 11. 4. Взаимодействие с водойCI2 + H2O = HCI + HCIO
- 12. 5. Взаимодействие с растворами солей (более активный
- 13. Перечислите галогены.Фтор, хлор, бром, йод, астат.2. Где
- 14. Дополните:Самый сильный неметалл – Самая сильная бескислородная
- 15. Сопоставьте :Хлор
- 16. Оцени себя:- тему усвоил полностью- не понял
- 17. Д/З § 55 упр. № 1-7 NaCI → CI2 →HCI → CuCI2
Слайд 2План урока
Положение галогенов в ПСХЭ Д.И. Менделеева.
Строение атомов и характерные степени
Историческая справка.
Нахождение в природе.
Физические и химические свойства.
Слайд 39F
17CI
35Br
53I
Элементы 2 периода,
VII А(галогены)
85Аt
+9
2
7
…2s22р5
+17
…3s23р5
+53
2
8
18
18
7
…5s25р5
8
2
18
7
+35
…4s24р5
2
8
7
- радиоактивный элемент
1. Увеличиваются заряды атомных
2. Увеличивается число энергетических уровней.
3. Увеличивается радиус атома.
4. Число электронов на внешнем уровне не изменяется.
5. Неметаллические свойства ослабевают,
металлические усиливаются.
6. С.О. -1, 0
+1, +3, +5, +7 (кроме фтора)
Слайд 81. Взаимодействие с металлами
2 Na + CI2 = 2 NaCI
2Fe +
Химические свойства
Cu + CI2 = CuCI2
Слайд 92. Взаимодействие с водородом
Н2 + Г2 = 2Н Г
Н2 + F2
Н2 + CI2 = 2Н CI + Q
Н2 + Br2 = 2НBr
Н2 + I2 2Н I - Q
Слайд 125. Взаимодействие с растворами солей (более активный галоген вытесняет менее активный)
CI2
CI2 + 2NaI = 2 NaCI + I2
Br2 + 2NaI = 2 NaBr + I2
Слайд 13Перечислите галогены.
Фтор, хлор, бром, йод, астат.
2. Где в ПСХЭ располагаются галогены?
В
3. Чему равно число валентных электронов в атомах галогенов ?
Число валентных электронов равно семи.
Ответе на вопросы
Слайд 14Дополните:
Самый сильный неметалл –
Самая сильная бескислородная кислота –
Как изменяются
фтор.
HI.
Уменьшаются в ряду F CI Br I
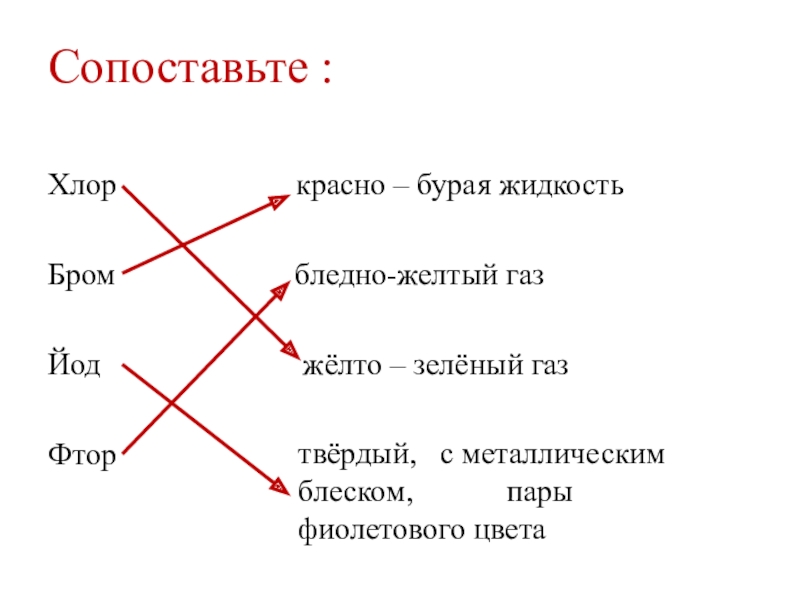
Слайд 15Сопоставьте :
Хлор
Бром бледно-желтый газ
Йод жёлто – зелёный газ
Фтор
твёрдый, с металлическим блеском, пары фиолетового цвета