- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Ферменты 10 класс
Содержание
- 1. Презентация по химии на тему Ферменты 10 класс
- 2. Оглавление 1.Определение2.Строение ферментов3.Номенклатура ферментов4.Свойства ферментов5.Роль ферментов в жизнедеятельности организмов6.Особенности ферментов7.Применение ферментов8.Проверь себя-тест
- 3. ОпределениеФерменты – биологические катализаторы белковой природы, ускоряющие
- 4. Строение ферментов1.двухкомпонентными - сложными белками Характерной особенностью
- 5. Номенклатура ферментовСейчас используется новая номенклатура ферментов, принятая
- 6. Свойства ферментовФерменты обладают такими общими для всех
- 7. Денатурация белка -- это разрушение вторичной и
- 8. Свойства ферментовФерменты обладают также уникальными свойствами:Необычно высокая
- 9. Свойства ферментовВысокая специфичность ферментов. Благодаря данному свойству
- 10. Роль ферментов в жизнедеятельности организмов можно проиллюстрировать схемой:
- 11. Особенности ферментовМногие ферменты наиболее эффективны при температуре
- 12. Особенности ферментовФерменты наиболее эффективно действуют при строго
- 13. ПрименениеФерменты используются в производстве:Пищи и напитков(вино, хлеб, сыр)Медикаментов («Пепсин», «Мезим», «Фестал»)Моющих средствТекстиляБумаги
- 14. Проверь себя: ТЕСТ
- 15. 1.(3 балла). Класс соединений, к которому относятся ферменты:А. БелкиБ. ЖирыВ. Углеводы.Г. Нуклеиновые кислоты.
- 16. 1.(3 балла). Класс соединений, к которому относятся ферменты:А. БелкиБ. ЖирыВ. Углеводы.Г. Нуклеиновые кислоты.
- 17. 2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:А. АминокислотыБ. Углеводороды.В. Углеводы.Г. Высшие (жирные) кислоты.
- 18. 2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:А. АминокислотыБ. Углеводороды.В. Углеводы.Г. Высшие (жирные) кислоты.
- 19. 3.(3 балла). Продуктами гидролиза белков являются:А. Глюкоза.Б. Аминокислоты.В. Глицерин и жирные кислоты.Г. Нуклеотиды.
- 20. 3.(3 балла). Продуктами гидролиза белков являются:А. Глюкоза.Б. Аминокислоты.В. Глицерин и жирные кислоты.Г. Нуклеотиды.
- 21. 4. (3 балла). Температура, при которой ферменты
- 22. 4. (3 балла). Температура, при которой ферменты
- 23. 5.(3 балла). Селективностью (избирательностью) действия ферментов называется:А.
- 24. 5.(3 балла). Селективностью (избирательностью) действия ферментов называется:А.
- 25. 6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее активен:А. 1,5—2,0. Б. 3,0—4,0. В. 5,0—6,0.Г. 7,0—8,0.
- 26. 6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее активен:А. 1,5—2,0. Б. 3,0—4,0. В. 5,0—6,0.Г. 7,0—8,0.
- 27. 7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:А. Амилаза. Б. Пепсин.В. Каталаза.Г. Фицин
- 28. 7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:А. Амилаза. Б. Пепсин.В. Каталаза.Г. Фицин
- 29. 8.(3 балла). Фермент трипсин расщепляет:А. Углеводы. Б. Белки. В. Жиры.Г. Нуклеиновые кислоты.
- 30. 8.(3 балла). Фермент трипсин расщепляет:А. Углеводы. Б. Белки. В. Жиры.Г. Нуклеиновые кислоты.
- 31. 9.(3 балла). Высокая эффективность ферментов объясняется:А. Быстрым
- 32. 9.(3 балла). Высокая эффективность ферментов объясняется:А. Быстрым
- 33. 10.(3 балла). Отдел желудка жвачных животных, в
- 34. 10.(3 балла). Отдел желудка жвачных животных, в
- 35. Домашнее задание.§ 19 учебника. Ответить на вопросы
- 36. Список литературы1. Габриелян О.С.,А.В.Яшукова Методическое пособие. Химия.
- 37. Интернет -ресурсыhttp://files.school-collection.edu.ru/dlrstore/d7794640-8cff-11db-b606-0800200c9a66/ch10_30_02.swfhttp://files.school-collection.edu.ru/dlrstore/d7791f54-8cff-11db-b606-0800200c9a66/ch10_30_01.swf
Слайд 1Ферменты
Звездова Ирина Анатольевна учитель химии МБОУ «Средняя общеобразовательная школа №190» г.
Слайд 2Оглавление
1.Определение
2.Строение ферментов
3.Номенклатура ферментов
4.Свойства ферментов
5.Роль ферментов в жизнедеятельности организмов
6.Особенности ферментов
7.Применение ферментов
8.Проверь
Слайд 3Определение
Ферменты – биологические катализаторы белковой природы, ускоряющие химические реакции в живых
На данный момент химикам известно более 2000 ферментов
Слайд 4Строение ферментов
1.двухкомпонентными - сложными белками
Характерной особенностью двухкомпонентного фермента
является то, что
отдельности не обладают заменой каталитической активностью.
Только их комплекс проявляет ферментативные свойства.
2.однокомпонентными -простыми белками;
Иначе обстоит дело у однокомпонентных ферментов, не имеющих
добавочной группы, которая могла бы входить в
непосредственный контакт с преобразуемым соединением. Эту
функцию выполняет часть белковой молекулы, называемая
каталитическим центром.
По строению ферменты могут быть:
Слайд 5Номенклатура ферментов
Сейчас используется новая номенклатура ферментов, принятая в 1961 году. В
Слайд 6Свойства ферментов
Ферменты обладают такими общими для всех белков свойствами, как:
Способность к
Амфотерность (способность проявлять в зависимости от условий как кислотные, так и основные свойства)
Способность к денатурации и гидролизу
Протекание цветных реакций (биуретовой и ксантопротеиновой)
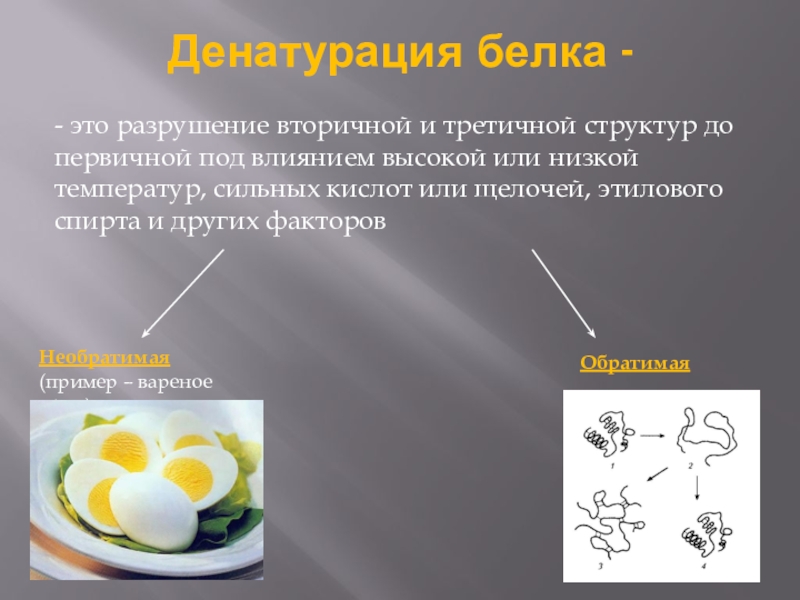
Слайд 7Денатурация белка -
- это разрушение вторичной и третичной структур до первичной
Необратимая
(пример – вареное яйцо)
Обратимая
Слайд 8Свойства ферментов
Ферменты обладают также уникальными свойствами:
Необычно высокая каталитическая активность. Так, добавка
Селективность (избирательность) действия – определяется их способностью превращать только данный тип субстратов в определенных реакциях и условиях
-9
-7
8
12
Слайд 9Свойства ферментов
Высокая специфичность ферментов. Благодаря данному свойству в организме не воцаряется
Стабильность – способность сохранять каталитическую активность при определенных условиях
Эффективность – скорость некоторых ферментативный реакций может быть в 10 раз больше скорости реакций, протекающих в их отсутствие
15
Слайд 11Особенности ферментов
Многие ферменты наиболее эффективны при температуре человеческого тела (35-42 С).
Слайд 12Особенности ферментов
Ферменты наиболее эффективно действуют при строго определенной среде раствора, при
Например, пепсин наиболее активен при pH от 1,5 до 2,0; каталаза крови – при pH, равном 7,0
Слайд 13Применение
Ферменты используются в производстве:
Пищи и напитков(вино, хлеб, сыр)
Медикаментов («Пепсин», «Мезим», «Фестал»)
Моющих
Текстиля
Бумаги
Слайд 151.(3 балла). Класс соединений, к которому относятся ферменты:
А. Белки
Б. Жиры
В. Углеводы.
Г.
Слайд 161.(3 балла). Класс соединений, к которому относятся ферменты:
А. Белки
Б. Жиры
В. Углеводы.
Г.
Слайд 172.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:
А. Аминокислоты
Б. Углеводороды.
В. Углеводы.
Г.
Слайд 182.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению:
А. Аминокислоты
Б. Углеводороды.
В. Углеводы.
Г.
Слайд 193.(3 балла). Продуктами гидролиза белков являются:
А. Глюкоза.
Б. Аминокислоты.
В. Глицерин и жирные
Г. Нуклеотиды.
Слайд 203.(3 балла). Продуктами гидролиза белков являются:
А. Глюкоза.
Б. Аминокислоты.
В. Глицерин и жирные
Г. Нуклеотиды.
Слайд 214. (3 балла). Температура, при которой ферменты в организме человека наиболее
А. 10 °С.
Б. 30 °С.
В. 37 °С.
Г. 40 °С.
Слайд 224. (3 балла). Температура, при которой ферменты в организме человека наиболее
А. 10 °С.
Б. 30 °С.
В. 37 °С.
Г. 40 °С.
Слайд 235.(3 балла). Селективностью (избирательностью) действия ферментов называется:
А. Способность фермента ускорять одну
Б. Способность фермента ускорять любые реакции.
В. Способность фермента замедлять любые реакции.
Г. Способность фермента замедлять одну или группу однотипных реакций.
Слайд 245.(3 балла). Селективностью (избирательностью) действия ферментов называется:
А. Способность фермента ускорять одну
Б. Способность фермента ускорять любые реакции.
В. Способность фермента замедлять любые реакции.
Г. Способность фермента замедлять одну или группу однотипных реакций.
Слайд 256.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее
А. 1,5—2,0.
Б. 3,0—4,0.
В. 5,0—6,0.
Г. 7,0—8,0.
Слайд 266.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее
А. 1,5—2,0.
Б. 3,0—4,0.
В. 5,0—6,0.
Г. 7,0—8,0.
Слайд 277.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:
А.
Б. Пепсин.
В. Каталаза.
Г. Фицин
Слайд 287.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета:
А.
Б. Пепсин.
В. Каталаза.
Г. Фицин
Слайд 298.(3 балла). Фермент трипсин расщепляет:
А. Углеводы.
Б. Белки.
В. Жиры.
Г. Нуклеиновые кислоты.
Слайд 308.(3 балла). Фермент трипсин расщепляет:
А. Углеводы.
Б. Белки.
В. Жиры.
Г. Нуклеиновые кислоты.
Слайд 319.(3 балла). Высокая эффективность ферментов объясняется:
А. Быстрым восстановлением их молекул в
Б. Многообразием ферментов.
В. Высокой активностью молекул ферментов.
Г. Все предыдущие ответы верны.
Слайд 329.(3 балла). Высокая эффективность ферментов объясняется:
А. Быстрым восстановлением их молекул в
Б. Многообразием ферментов.
В. Высокой активностью молекул ферментов.
Г. Все предыдущие ответы верны.
Слайд 3310.(3 балла). Отдел желудка жвачных животных, в котором вырабатывается фермент реннин,
А. Сетка.
Б. Книжка.
В. Сычуг.
Г. Рубец.
Слайд 3410.(3 балла). Отдел желудка жвачных животных, в котором вырабатывается фермент реннин,
А. Сетка.
Б. Книжка.
В. Сычуг.
Г. Рубец.
Слайд 35Домашнее задание.
§ 19 учебника. Ответить на вопросы и выполнить задания после
Подготовить презентацию «Витамины»
10-12 слайдов.
Слайд 36Список литературы
1. Габриелян О.С.,А.В.Яшукова Методическое пособие. Химия. 10 класс.(базовый уровень) ,
2. Габриелян О.С.Химия.10 класс: контрольные и проверочные работы-М. Дрофа,2011
3. Власова З. А. Биология. Справочник школьника. Всероссийское слово, 1995 г.
4. Хомченко Г. Л. Химия для поступающих в ВУЗЫ. Высшая школа,1993 г.
5. Биологический энциклопедический словарь. Советская энциклопедия, 1987г.