- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Бензол 10 класс
Содержание
- 1. Презентация по химии на тему Бензол 10 класс
- 2. Общая формула: СnН2n-2 Алкадиены являются представителями ненасыщенных
- 3. Связи алкадиенов 1.Изолированные двойные связи разделены в цепи
- 4. Физические свойства алкадиенов Низшие диены — бесцветные
- 5. Химические свойства алкадиенов 1.Галогенирование. При присоединении к алкадиенам
- 6. Получение алкадиенов Основные способы получения алкадиенов –
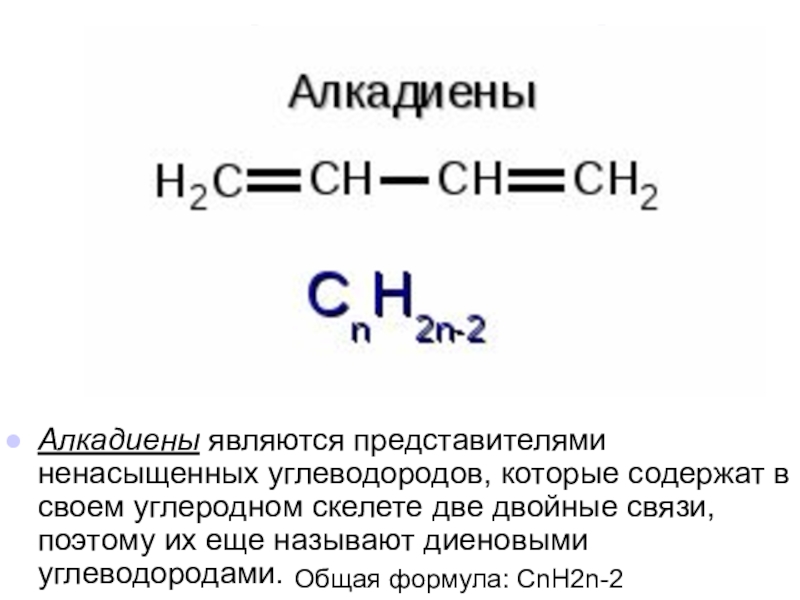
Общая формула: СnН2n-2 Алкадиены являются представителями ненасыщенных углеводородов, которые содержат в своем углеродном скелете две двойные связи, поэтому их еще называют диеновыми углеводородами.
Слайд 2Общая формула: СnН2n-2
Алкадиены являются представителями ненасыщенных углеводородов, которые содержат в
своем углеродном скелете две двойные связи, поэтому их еще называют диеновыми углеводородами.
Слайд 3Связи алкадиенов
1.Изолированные двойные связи разделены в цепи двумя или более s-связями: СН2=СН–СН2–СН=СН2
2. Кумулированные двойные связи расположены у одного атома углерода: СН2=С=СН2(аллен)
3.Сопряженные двойные связи разделены одной s-связью:
СН2=СН–СН=СН2
Слайд 4Физические свойства алкадиенов
Низшие диены — бесцветные легкокипящие жидкости. 1,3-Бутадиен и аллен
(1,2 — пропадиен) — легко сжижающиеся газы, обладающие неприятным запахом. Высшие диены представляют собой твердые вещества.
Слайд 5Химические свойства алкадиенов
1.Галогенирование. При присоединении к алкадиенам хлора или брома образуются тетрагалогеноалканы,
причем, возможно образование продуктов как 1,2-, так и 1,4- присоединения. Соотношение продуктов зависит от условий проведения реакции: типа растворителя и температуры.
CH2 = CH-CH = CH2 + Br2 (гексан) → CH2(Br)-CH(Br)-CH = CH2 + CH2(Br)-CH = CH-CH2-Br
2. Гидрогалогенирование протекает подобно галогенированию, т.е. с образованием смеси продуктов 1,2 – и 1,4 – присоединения. Соотношение продуктов в основном зависит от температуры, так, при высоких температурах преобладают продукты 1,2 – присоединения, а при низких — 1,4 – присоединения.
CH2 = CH-CH = CH2 +HBr → CH3-CH(Br)-CH = CH2 + CH3-CH = CH-CH2-Br
3. Гидрирование алкадиенов происходит в условиях жидкого аммиака и приводит к образованию смеси продуктов 1,2 – и 1,4 – присоединения:
CH2 = CH-CH = CH2 + H2 → CH3-CH2-CH = CH2 + CH3-CH = CH-CH3.
4. Реакции изомеризации алкадиенов протекают в щелочной среде при нагревании и в присутствии катализатора – оксида алюминия:
R-CH = C = C-CH-R → RC≡C-CH2-R
5. Полимеризация алкадиенов может протекать как 1,2 – или 1,4 – присоединение:
nCH2 = CH-CH = CH2 → (-CH2-CH = CH-CH2-)n
CH2 = CH-CH = CH2 + Br2 (гексан) → CH2(Br)-CH(Br)-CH = CH2 + CH2(Br)-CH = CH-CH2-Br
2. Гидрогалогенирование протекает подобно галогенированию, т.е. с образованием смеси продуктов 1,2 – и 1,4 – присоединения. Соотношение продуктов в основном зависит от температуры, так, при высоких температурах преобладают продукты 1,2 – присоединения, а при низких — 1,4 – присоединения.
CH2 = CH-CH = CH2 +HBr → CH3-CH(Br)-CH = CH2 + CH3-CH = CH-CH2-Br
3. Гидрирование алкадиенов происходит в условиях жидкого аммиака и приводит к образованию смеси продуктов 1,2 – и 1,4 – присоединения:
CH2 = CH-CH = CH2 + H2 → CH3-CH2-CH = CH2 + CH3-CH = CH-CH3.
4. Реакции изомеризации алкадиенов протекают в щелочной среде при нагревании и в присутствии катализатора – оксида алюминия:
R-CH = C = C-CH-R → RC≡C-CH2-R
5. Полимеризация алкадиенов может протекать как 1,2 – или 1,4 – присоединение:
nCH2 = CH-CH = CH2 → (-CH2-CH = CH-CH2-)n
Слайд 6Получение алкадиенов
Основные способы получения алкадиенов – дегидрирование алканов (1), реакция Лебедева
(2), дегидратация гликолей (3), дегалагенирование дигалогенпроизводных (4) алкенов и реакции перегруппировки (5):
CH3-CH2-CH2-CH3 → CH2 = CH-CH = CH2 (1);
2C2H5OH → CH2 = CH-CH = CH2 + 2H2O + H2 (2);
CH3-CH(OH)-CH2-CH2-OH → CH2 = CH-CH = CH2 + 2H2O (3);
СH2 = C(Br)-CH2-Br + Zn → CH2 = C = CH2 + ZnBr2 (4);
HC≡C-CH(CH3)-CH3 + NaOH → CH2 = C = CH(CH3)-CH3 (5).
Основная сфера использования диенов и их производных – это производство каучука.
CH3-CH2-CH2-CH3 → CH2 = CH-CH = CH2 (1);
2C2H5OH → CH2 = CH-CH = CH2 + 2H2O + H2 (2);
CH3-CH(OH)-CH2-CH2-OH → CH2 = CH-CH = CH2 + 2H2O (3);
СH2 = C(Br)-CH2-Br + Zn → CH2 = C = CH2 + ZnBr2 (4);
HC≡C-CH(CH3)-CH3 + NaOH → CH2 = C = CH(CH3)-CH3 (5).
Основная сфера использования диенов и их производных – это производство каучука.