- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Азот (9 класс)
Содержание
- 1. Презентация по химии на тему Азот (9 класс)
- 2. Азот N2Открыт Д.Резерфордом в 1772 гназван А.Лавуазье в 1787 г«Азоэ» (греч.) - безжизненный
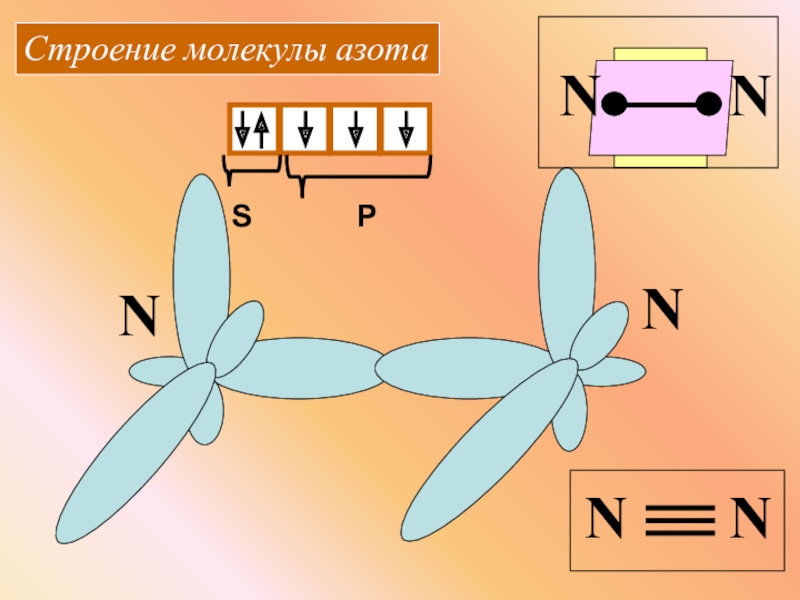
- 3. Строение молекулы азотаSPNNNNNN
- 4. Степени окисления1.Окислительные свойстваN0N-3по отношению к металлам,H2, элементамс
- 5. Физические свойстваАзот – это газ без цвета,
- 6. Нахождение в природеВ воздухе содержится 78,09% азота(по
- 7. Химические свойстваАзот – восстановитель: N2 → 2N+2
- 8. Азот – окислитель: N02→ 2N-31.Взаимодействие с водородом:
- 9. ВоздухФракционная перегонка жидкого воздуха. Азот отделяют от
- 10. Получение азота в лабораторииРазложение азотнокислых солей: NH4NO2→
- 11. Слайд 11
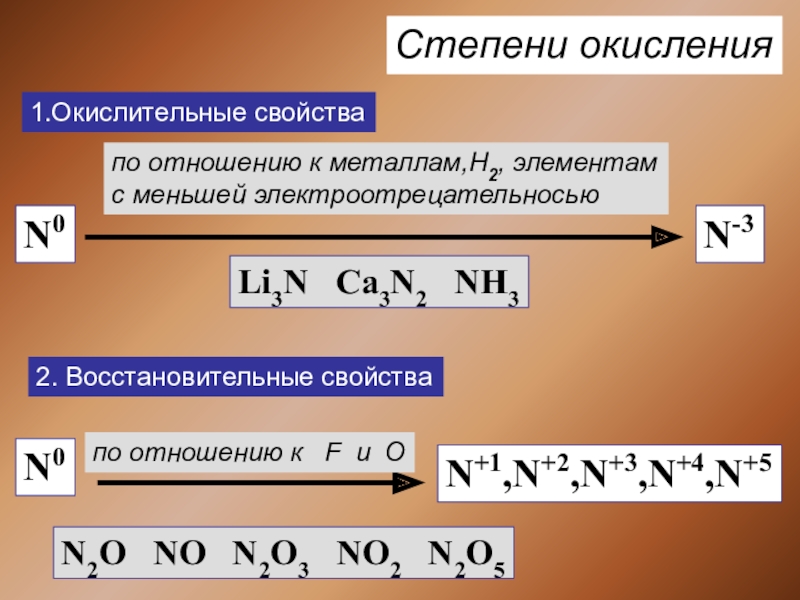
Слайд 4Степени окисления
1.Окислительные свойства
N0
N-3
по отношению к металлам,H2, элементам
с меньшей электроотрецательносью
Li3N Ca3N2
2. Восстановительные свойства
N0
N+1,N+2,N+3,N+4,N+5
по отношению к F и О
N2O NO N2O3 NO2 N2O5
Слайд 5Физические свойства
Азот – это газ без цвета, без запаха и вкуса,
до -1960С превращается в бесцветную жидкость, а при
-2100 – в снегообразную массу. Жидкий азот применяют в
медицине для лечения кожных заболеваний.
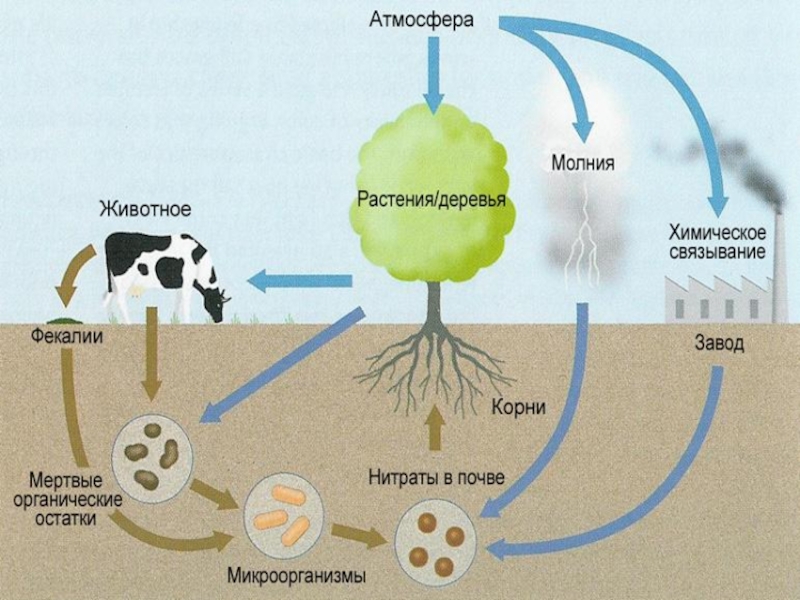
Слайд 6Нахождение в природе
В воздухе содержится 78,09% азота(по объему),
а в земной коре(в
Азот входит в состав важнейших
органических соединений – белков,
содержащихся во всех живых организмах
N2
Слайд 7Химические свойства
Азот – восстановитель: N2 → 2N+2
происходит реакция:
N2 + O2 2NO - Q
Она возможна благодаря тому, что температура воздуха
в канале молнии повышается до нескольких тысяч градусов
N2
Слайд 8Азот – окислитель: N02→ 2N-3
1.Взаимодействие с водородом: катализатор - Fe,
N20 + 3H2 2N-3H3
2.Взаимодействие с активными металлами:
6Li + N02 = 2Li3N-3
N2
Слайд 9Воздух
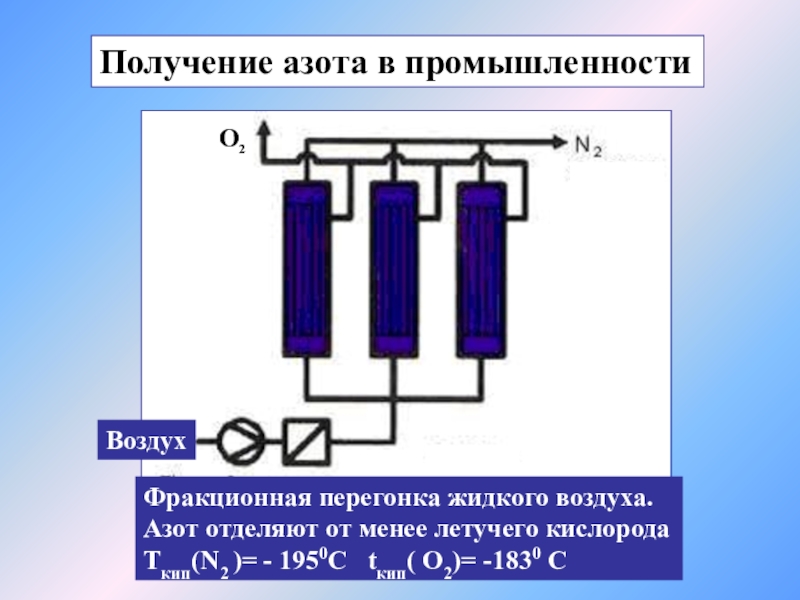
Фракционная перегонка жидкого воздуха.
Азот отделяют от менее летучего кислорода
Tкип(N2 )=
O2
Получение азота в промышленности
Слайд 10Получение азота в лаборатории
Разложение азотнокислых солей: NH4NO2→ N2 + 2H2O
t0
Свободный азот
для заполнения электроламп или для глубокого
охлаждения (жидкий азот). Однако огромное
значение имеет азот в качестве сырья при синтезе
aммиака – NH3.