При сжигании органического вещества массой 9 г. образовалось 17,6 г. оксида углерода (IV), 12,6 г. воды и азот. Относительная плотность вещества по водороду равна 22,5. Найдите молекулярную формулу вещества?
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Амины (10 класс)
Содержание
- 1. Презентация по химии на тему Амины (10 класс)
- 2. Составьте структурные формулы данных соединений.
- 3. Это производные углеводородов, в молекулах которых
- 4. Классификация аминов1. По природе радикала2. По числу
- 5. Строение и номенклатура аминов CH3
- 6. C C4 NH2
- 7. Химические свойства аммиака
- 8. Химические свойства аминов H
- 9. 1) с водой 2) с кислотами 3) горениеХимические свойства аминов
- 10. Химические свойства аминов
- 11. Слайд 11
- 12. Получение аминов1) CH3CL + 2NH3
- 13. Выполнение самостоятельной работыЗадачник:1 вариант: стр. 123 №1-62 вариант: стр. 125 №1-63 вариант: стр. 126 №1-6
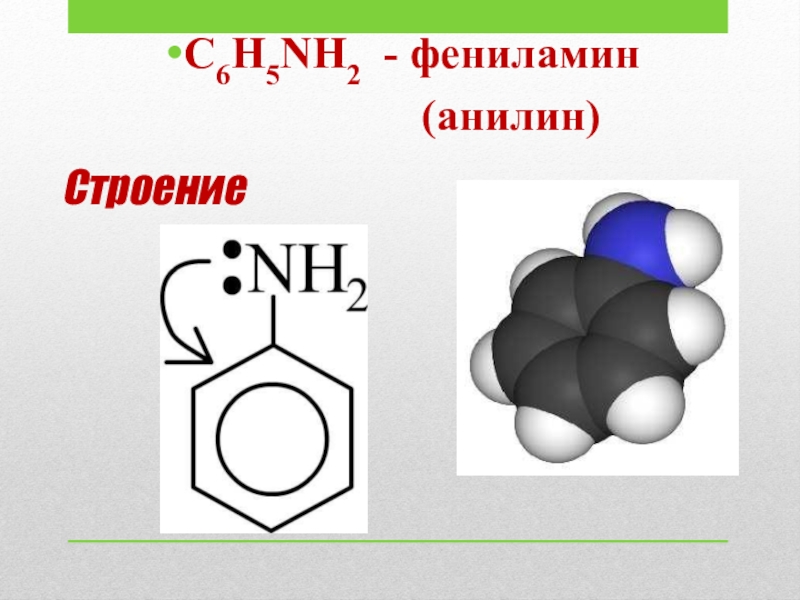
- 14. СтроениеC6H5NH2 - фениламин (анилин)
- 15. Физические свойстваАнилин - бесцветная маслянистая жидкость.При окислении
- 16. ЗИНИН Николай Николаевич (25.08.1812–18.02.1880)академик, возглавлял кафедру
- 17. Получениев промышленности:
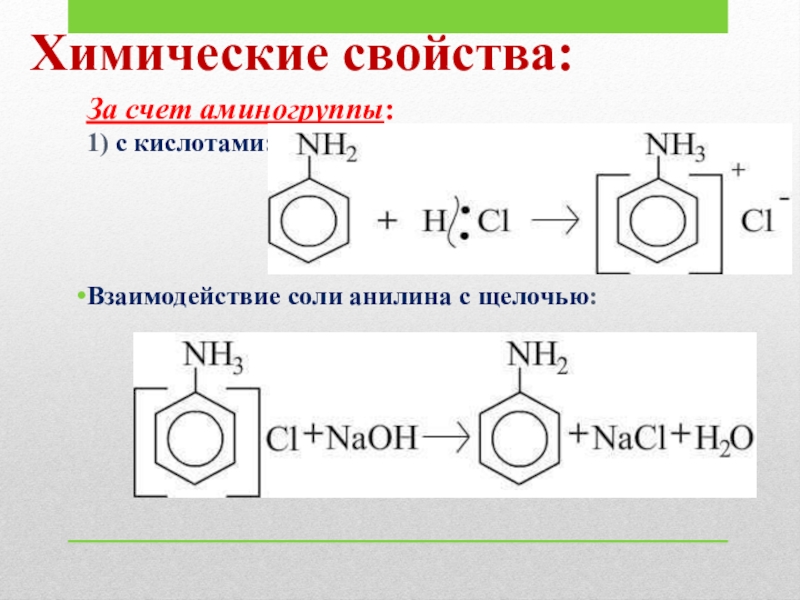
- 18. Химические свойства:За счет аминогруппы:1) с кислотами:Взаимодействие соли анилина с щелочью:
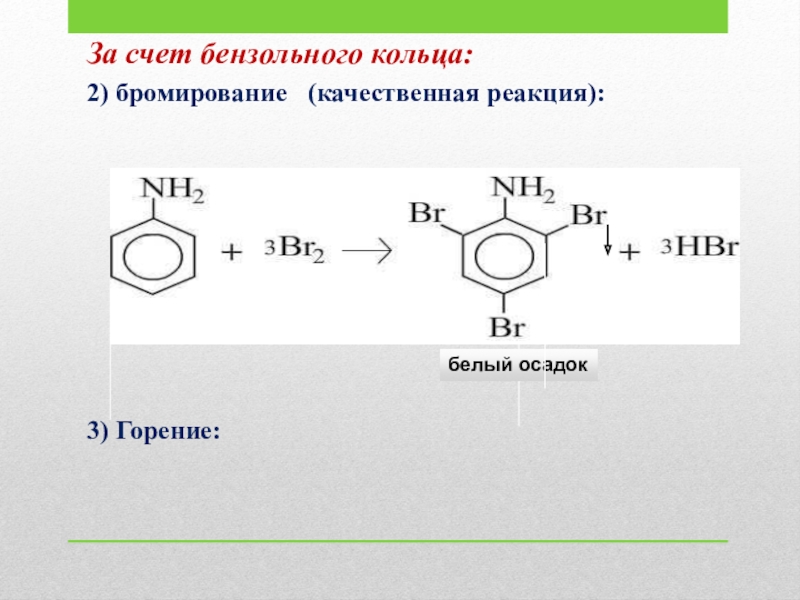
- 19. За счет бензольного кольца:2) бромирование (качественная реакция):3) Горение:белый осадок
- 20. ПрименениеВ настоящий момент в мире основная часть
- 21. Задание на самоподготовку:§ 16 №1-4Б №5П№8
- 22. ПрименениеОсновная область применения анилина – синтез красителей
- 23. Закрепление1. Какие из приведенных ниже веществ относятся
Слайд 1Задача
Определите молекулярную формулу органического вещества, массовые доли углерода 38,7%; азота
Слайд 3 Это производные углеводородов, в молекулах которых атом водорода замещен на
H
H C
H
NH2
H N H
CH3
Это производные аммиака, в молекуле которого один или несколько атомов водорода замещены на углеводородный радикал.
Тема урока: Амины
H
H
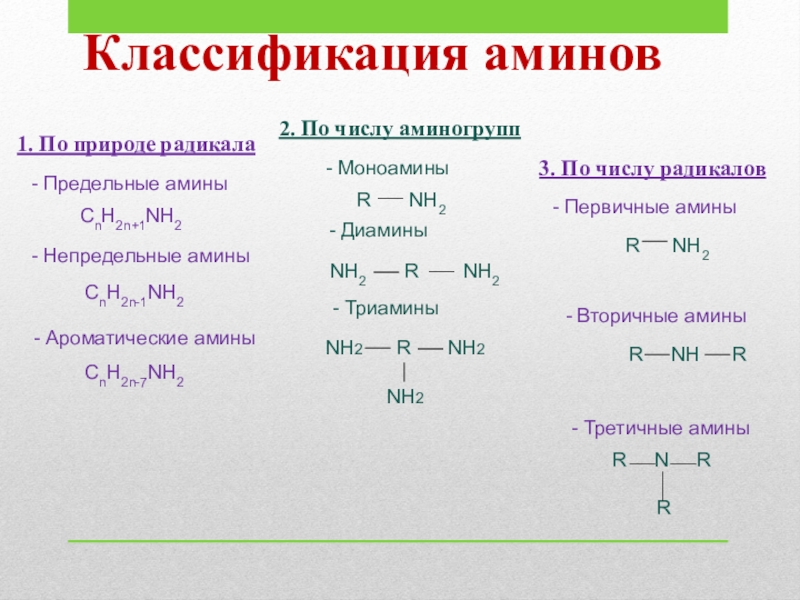
Слайд 4Классификация аминов
1. По природе радикала
2. По числу аминогрупп
- Предельные амины
CnH2n+1NH2
- Непредельные
CnH2n-1NH2
- Ароматические амины
CnH2n-7NH2
- Моноамины
R NH2
- Диамины
NH2 R NH2
- Триамины
NH2 R NH2
NH2
3. По числу радикалов
- Третичные амины
- Вторичные амины
- Первичные амины
R N R
R
R NН R
R NH2
Слайд 5Строение
и номенклатура аминов
CH3 N
H
CH3 N H
CH3
CH3 N CH3
CH3
C6H5 N H
H
CH3 N H
C2H5
CH3 CH CH2 NH2
CH3
метиламин
диметиламин
триметиламин
Фениламин (анилин)
метилэтиламин
1-амино-2-метилпропан
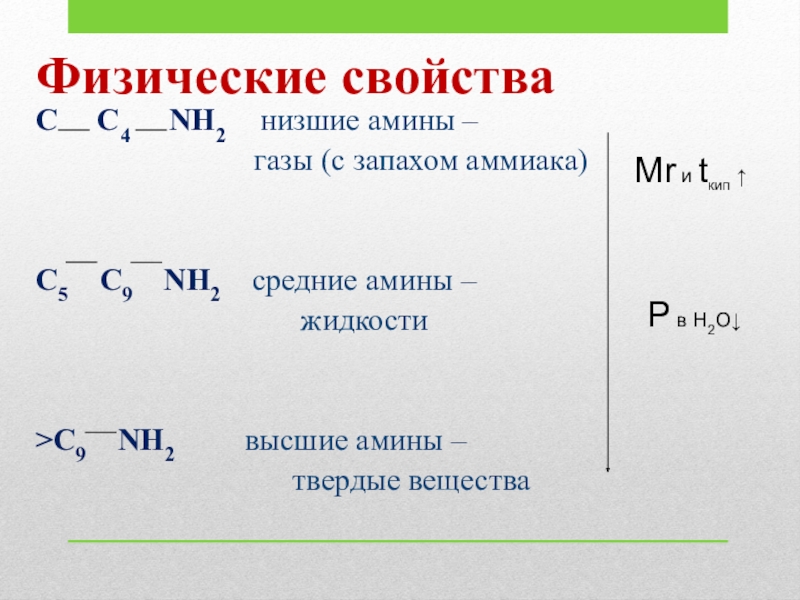
Слайд 6C C4 NH2 низшие амины
газы (с запахом аммиака)
C5 C9 NH2 средние амины –
жидкости
>C9 NH2 высшие амины –
твердые вещества
Физические свойства
Mr и tкип ↑
Р в H2O↓
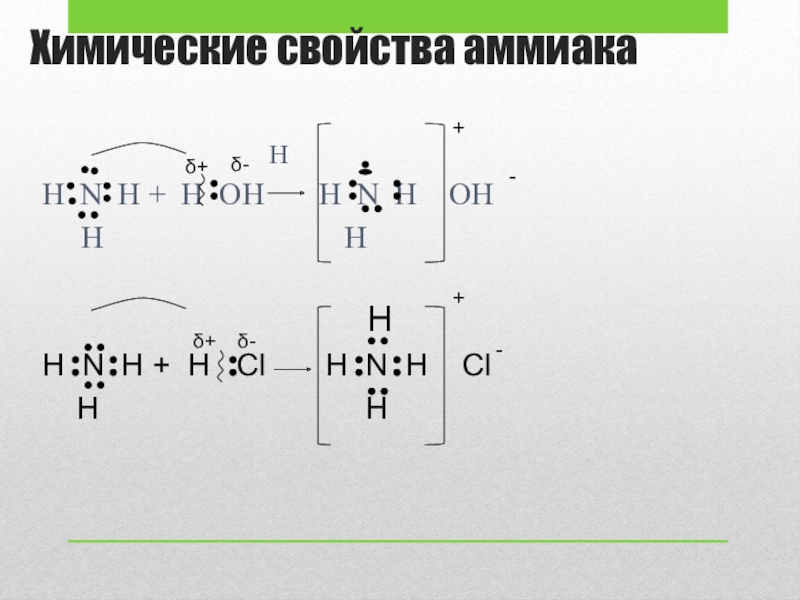
Слайд 7Химические свойства аммиака
H N H + H OH H N H OH
H H
δ+
δ-
+
-
H
H N H + H Cl H N H Cl
H H
δ+
δ-
+
-
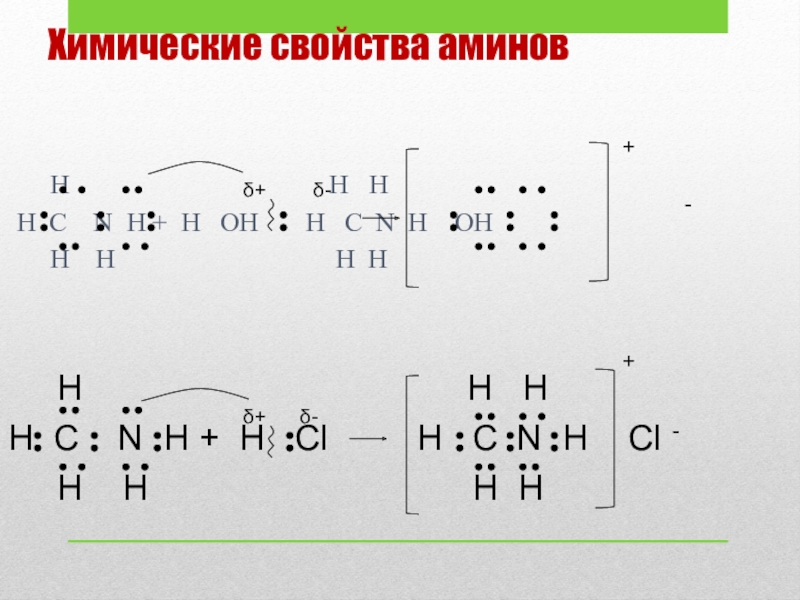
Слайд 8Химические свойства аминов
H
H C N H + H OH H C N H OH
H H H H
δ+
δ-
-
+
H H H
H C N H + H Cl H C N H Cl
H H H H
δ-
+
-
δ+
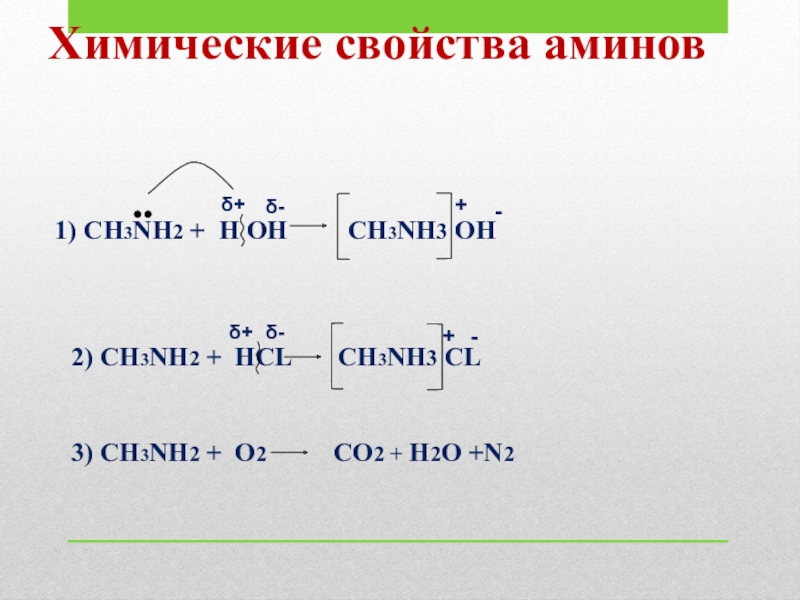
Слайд 10Химические свойства аминов
1) CH3NH2 + H OН CH3NH3 OН
δ+
δ-
-
+
2) CH3NH2 + HСL CH3NH3 CL
+
-
δ+
δ-
3) CH3NH2 + О2 CО2 + H2О +N2
Слайд 13Выполнение самостоятельной работы
Задачник:
1 вариант: стр. 123 №1-6
2 вариант: стр. 125 №1-6
3
Слайд 15Физические свойства
Анилин - бесцветная маслянистая жидкость.
При окислении на воздухе становится светло-коричневого
Имеет неприятный запах, малорастворим в воде.
Хорошо растворяется в этаноле и бензоле.
Температура кипения – 174 С.
Ядовит.
Проявляет слабые основные свойства.
Слайд 16
ЗИНИН
Николай Николаевич
(25.08.1812–18.02.1880)
академик, возглавлял кафедру общей химии Медико-хирургической академии в
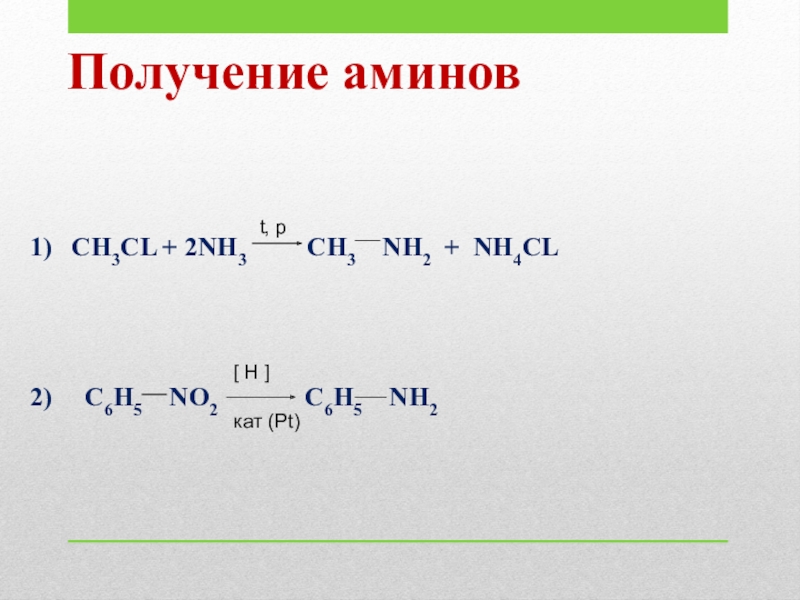
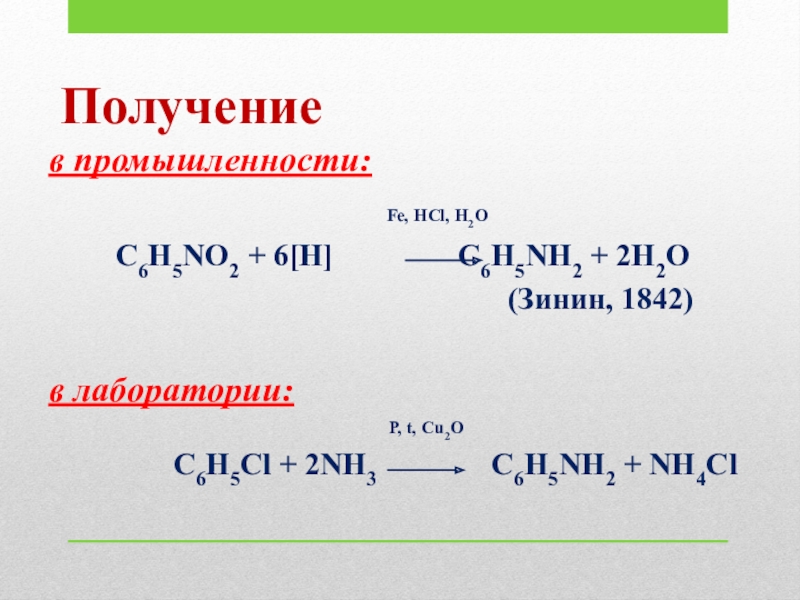
Слайд 17Получение
в промышленности:
C6H5NO2 + 6[H] C6H5NH2 + 2H2O
(Зинин, 1842)
в лаборатории:
P, t, Cu2O
C6H5Cl + 2NH3 C6H5NH2 + NH4Cl
Слайд 18Химические свойства:
За счет аминогруппы:
1) с кислотами:
Взаимодействие соли анилина с щелочью:
Слайд 20Применение
В настоящий момент в мире основная часть (85%) производимого анилина используется
В России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты), но в связи с ожидаемым ростом производства полиуретанов возможно значительное изменение картины потребителей в среднесрочной перспективе.
Слайд 22Применение
Основная область применения анилина – синтез красителей и лекарственных средств. В
H2SO4
NH2
сульфаниловая кислота
4-диазобензол-сульфокислота
+
N(CH3)2
HO3S
метиловый оранжевый
1.
2.
3.
Слайд 23Закрепление
1. Какие из приведенных ниже веществ относятся к аминам?
а) CH3
CH3
в) С6H5 NH2 г) C2H5 NO2
2. Какие амины проявляют более основные свойства:
а) метиламин или этиламин
б) метиламин или диметиламин. Почему?