молекулах ,которых имеются атомы углерода,, связанные между собой двойной или тройной связью.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Алкены (10 класс)
Содержание
- 1. Презентация по химии на тему Алкены (10 класс)
- 2. Учебная цель: изучить способы получения, химические
- 3. Эпиграф к уроку«Границ научному познанию и предсказанию предвидеть невозможно»Д.И.Менделеев
- 4. Лист самоанализа учебной
- 5. Ответьте, пожалуйста, на следующие вопросы:1.Какие углеводороды называются
- 6. Этиленовые углеводородыАлкены - непредельные углеводороды ,в молекулах
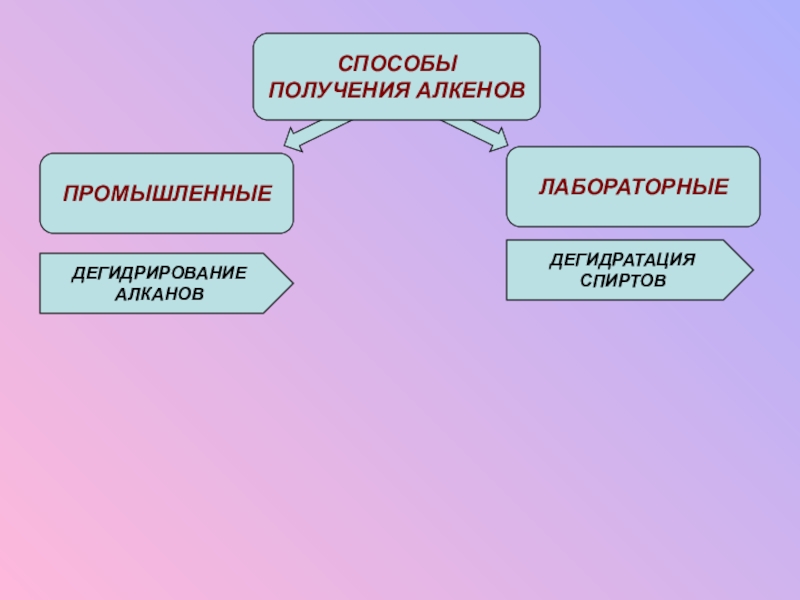
- 7. ПРОМЫШЛЕННЫЕСПОСОБЫПОЛУЧЕНИЯ АЛКЕНОВЛАБОРАТОРНЫЕДЕГИДРИРОВАНИЕАЛКАНОВДЕГИДРАТАЦИЯСПИРТОВ
- 8. ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН →
- 9. ЛАБОРАТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯДЕГИДРАТАЦИЯ СПИРТОВСПИРТ → АЛКЕН +
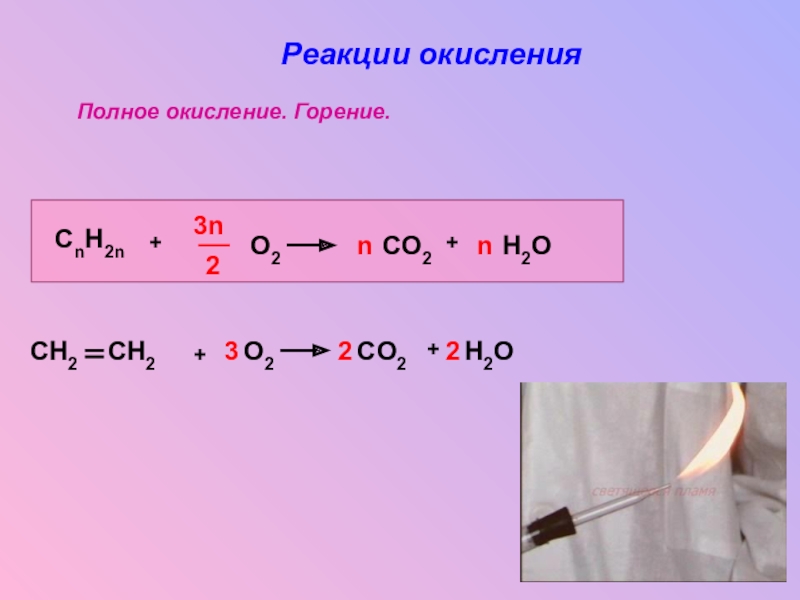
- 10. Химические свойства алкенов: Химические свойства определяются
- 11. CH3 CH3CH2 CH2HH2H+Алкены взаимодействуют с
- 12. CH2 CH2CH2Br CH2BrBrBr2Br+Галогенирование (присоединение галогенов)
- 13. Слайд 13
- 14. Реакция Вагнера (качественная реакция)- обесцвечивание
- 15. РЕАКЦИЯ ПОЛИМЕРИЗАЦИИЭто процесс соединения одинаковых молекул в
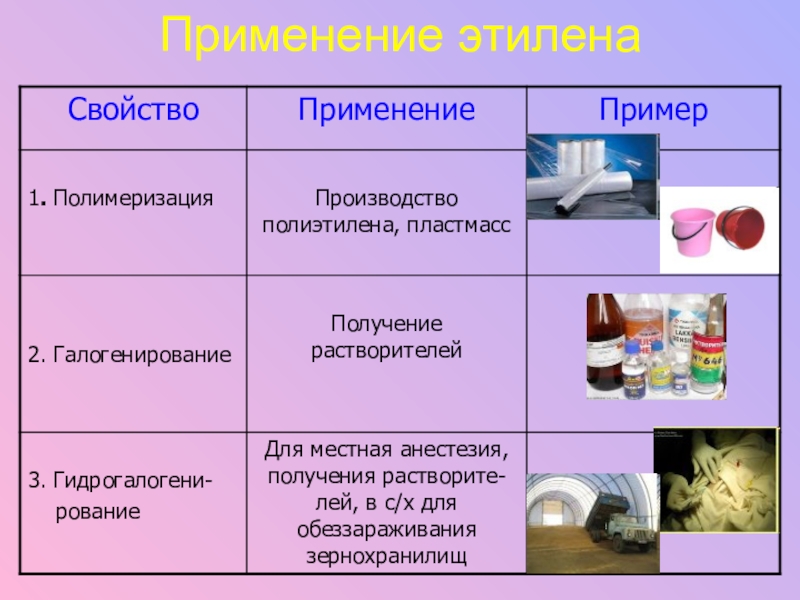
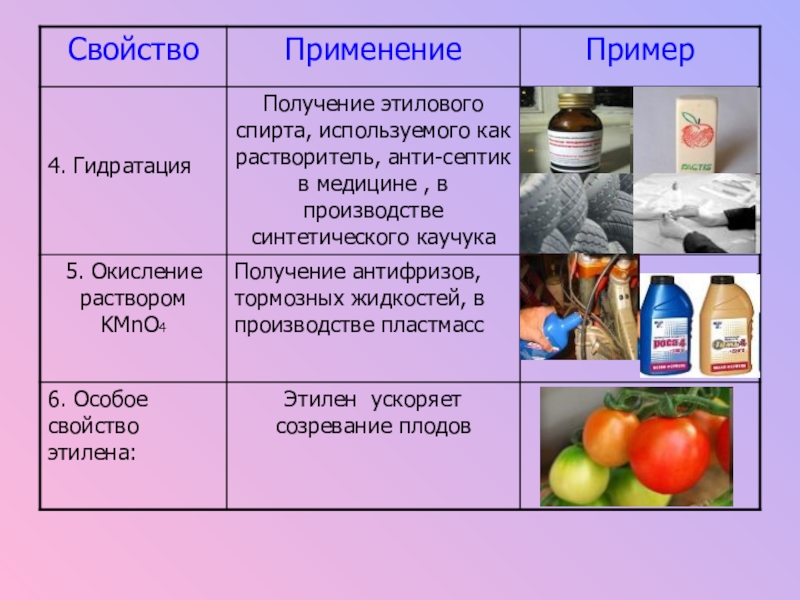
- 16. Применение этилена
- 17. Слайд 17
- 18. Диеновые углеводороды -мономеры синтетического каучука.В апреле 1926г.
- 19. В этом конкурсе победил русский ученый С.В. Лебедев и возглавил работу по производству СКБ.
- 20. Первым заводом по производству СК был Воронежский
- 21. ОАО «Воронежсинтезкаучук»
- 22. СИНКВЕЙН1 строка – имя существительное (тема синквейна)2
- 23. ЭтиленНенасыщенный, активныйГорит, обесцвечивает, присоединяетЭтилен – представитель непредельных углеводородовАлкен
- 24. СПАСИБО ЗА ХОРОШУЮ РАБОТУ!
Учебная цель: изучить способы получения, химические свойства и применение алкенов на примере непредельного углеводорода - этилена
Слайд 1Непредельные углеводороды
Разработка урока учителя химии Рыжковой Е.В.
Непредельными называются углеводороды в
Слайд 2Учебная цель:
изучить способы получения,
химические свойства
и применение алкенов
на примере непредельного углеводорода - этилена
Слайд 4 Лист самоанализа учебной деятельности учащегося ___________ по теме «Получение, химические свойства
и применение алкенов»
Слайд 5Ответьте, пожалуйста, на следующие вопросы:
1.Какие углеводороды называются алканами?
2.Какова общая формула алканов?
СnН2n+2.
3.Какова структурная формула первого представителя гомологического ряда алканов? Назовите его.
CH4 – метан
4.Где алканы встречаются в природе?
нефть, природный газ
5.Какие химические свойства характерны для алканов?
реакции замещения и окисления
3.Какова структурная формула первого представителя гомологического ряда алканов? Назовите его.
CH4 – метан
4.Где алканы встречаются в природе?
нефть, природный газ
5.Какие химические свойства характерны для алканов?
реакции замещения и окисления
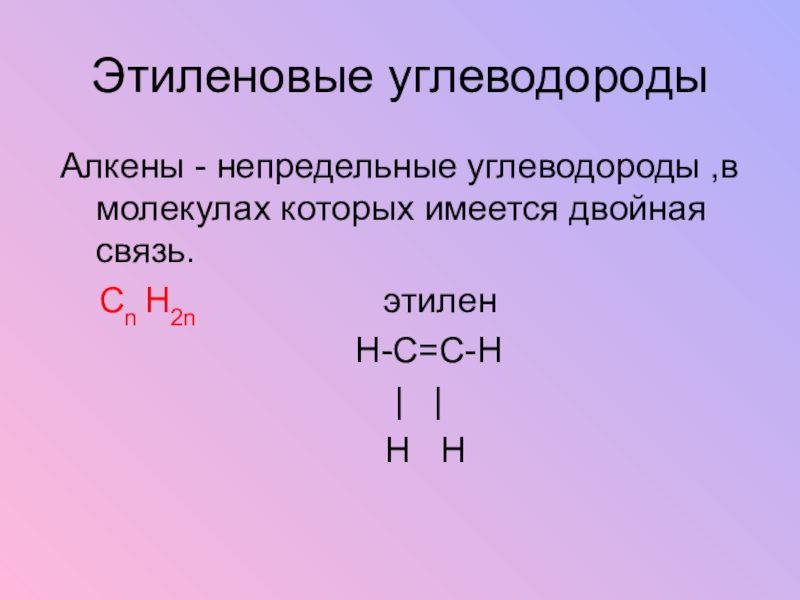
Слайд 6Этиленовые углеводороды
Алкены - непредельные углеводороды ,в молекулах которых имеется двойная связь.
Cn H2n этилен
Н-С=С-Н
| |
H H
Слайд 8ПРОМЫШЛЕННЫЙ
СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРИРОВАНИЕ АЛКАНОВ
АЛКАН → АЛКЕН + ВОДОРОД
ПРИМЕР:
Ni, t=500C
Н3С - СН3 → Н2С = СН2 + Н2
этан этен
(этилен)
Н3С - СН3 → Н2С = СН2 + Н2
этан этен
(этилен)
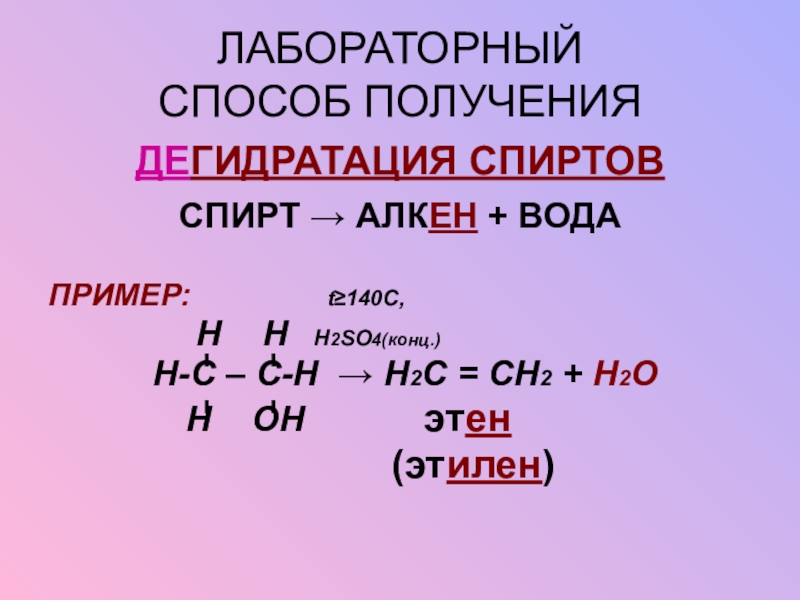
Слайд 9ЛАБОРАТОРНЫЙ
СПОСОБ ПОЛУЧЕНИЯ
ДЕГИДРАТАЦИЯ СПИРТОВ
СПИРТ → АЛКЕН + ВОДА
ПРИМЕР:
t≥140C,
Н Н Н2SO4(конц.)
Н-С – С-Н → Н2С = СН2 + Н2О
Н ОН этен
(этилен)
Н Н Н2SO4(конц.)
Н-С – С-Н → Н2С = СН2 + Н2О
Н ОН этен
(этилен)
Слайд 10Химические свойства алкенов:
Химические свойства определяются наличием двойной связи.
Характерные
реакции - присоединение , окисление, полимеризация
Слайд 11CH3 CH3
CH2 CH2
H
H2
H
+
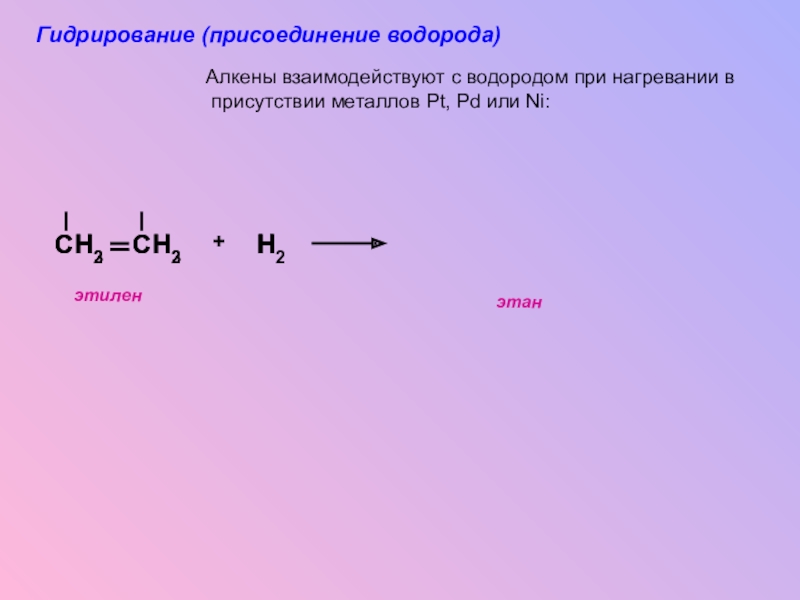
Алкены взаимодействуют с водородом при нагревании в
присутствии металлов Pt, Pd или Ni:
Гидрирование (присоединение водорода)
Слайд 12CH2 CH2
CH2Br CH2Br
Br
Br2
Br
+
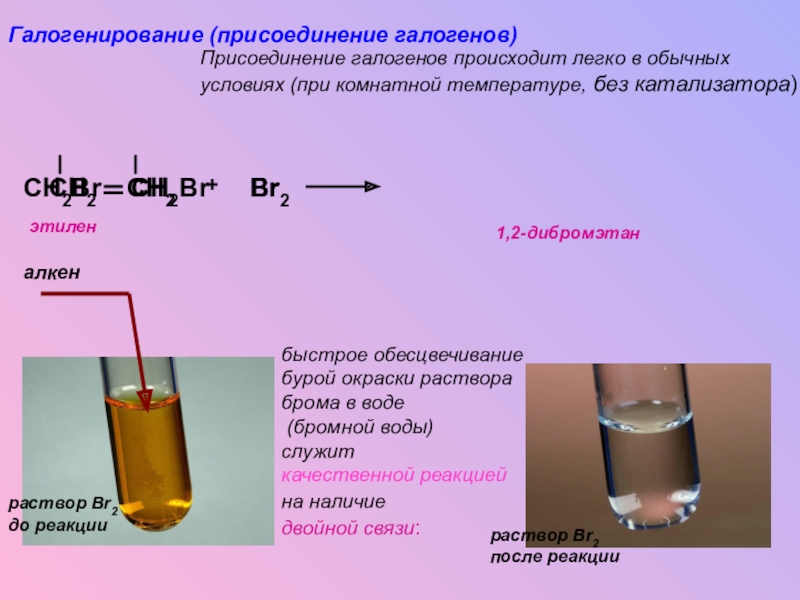
Галогенирование (присоединение галогенов)
Присоединение галогенов происходит легко
в обычных
условиях (при комнатной температуре, без катализатора).
условиях (при комнатной температуре, без катализатора).
Слайд 15РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ
Это процесс соединения одинаковых молекул в более крупные.
ПРИМЕР: n CH2=CH2
(-CH2-CH2-)n
этилен полиэтилен
(мономер) (полимер)
этилен полиэтилен
(мономер) (полимер)
Слайд 18Диеновые углеводороды -мономеры синтетического каучука.
В апреле 1926г. ВСНХ объявил международный конкурс
на лучший способ получения синтетического каучука.
Слайд 20Первым заводом по производству СК был Воронежский завод, построенный в 1932
г.
А в 1936 году уже было выпущено
15 411 т. СКБ.
А в 1936 году уже было выпущено
15 411 т. СКБ.
Слайд 22СИНКВЕЙН
1 строка – имя существительное (тема синквейна)
2 строка – два прилагательных
(раскрывающие тему синквейна)
3 строка – три глагола (описывают действия)
4 строка – фраза или предложение
(высказывают своё отношение к теме)
5 строка – синоним (слово-резюме)