- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Алканы
Содержание
- 1. Презентация по химии на тему: Алканы
- 2. План изучения классов веществ1. Название класса веществ,
- 3. АЛКАНЫ
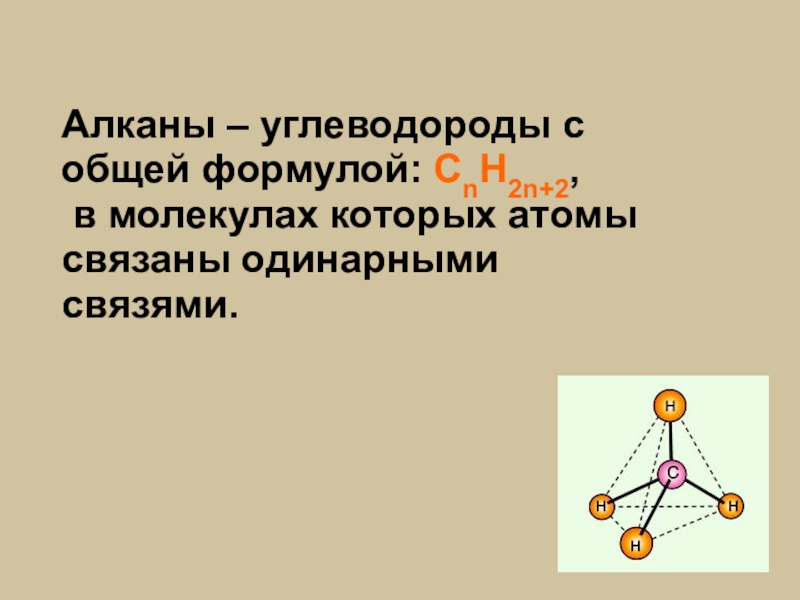
- 4. Алканы – углеводороды с общей формулой: СnH2n+2, в молекулах которых атомы связаны одинарными связями.
- 5. АЛКАНЫ (предельные, насыщенные, парафины) –это углеводороды, в
- 6. Простейшие представители алканов
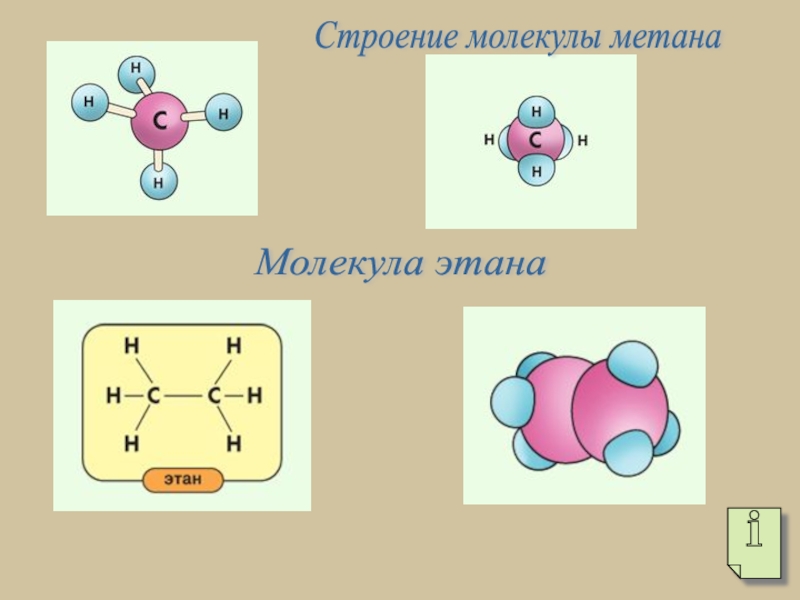
- 7. Строение молекулы метана Молекула этана
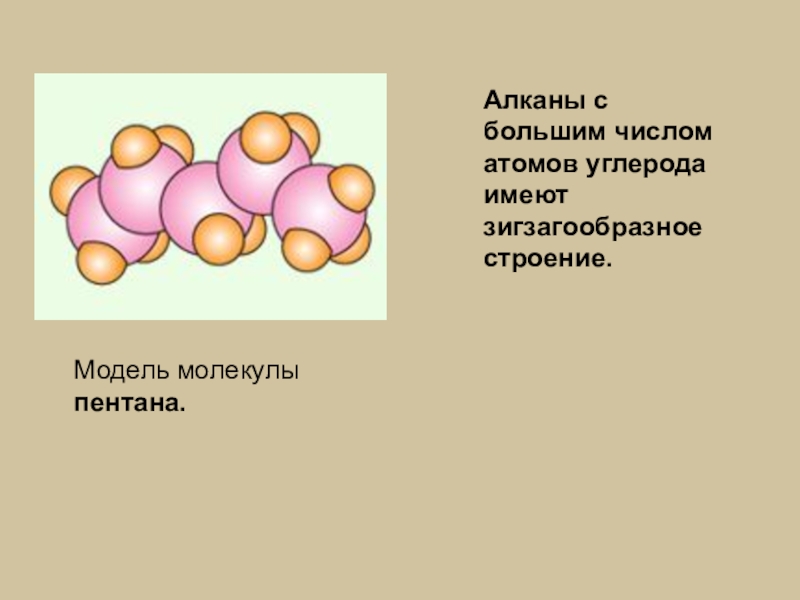
- 8. Модель молекулы пентана.Алканы с большим числом атомов углерода имеют зигзагообразное строение.
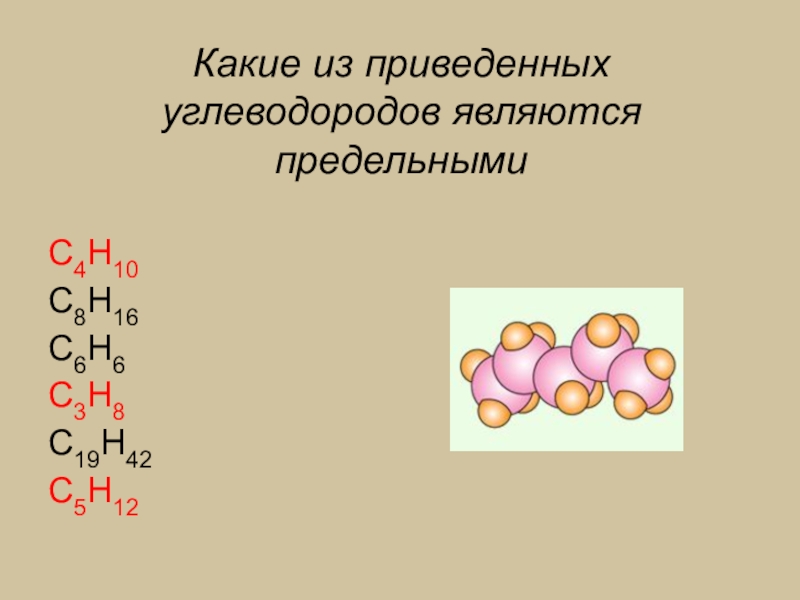
- 9. Какие из приведенных углеводородов являются предельными?С4Н10С8Н16С6Н6С3Н8С19Н42С5Н12
- 10. Какие из приведенных углеводородов являются предельнымиС4Н10С8Н16С6Н6С3Н8С19Н42С5Н12
- 11. Составьте полные и сокращенные структурные формулы для пропана, бутана и пентана.
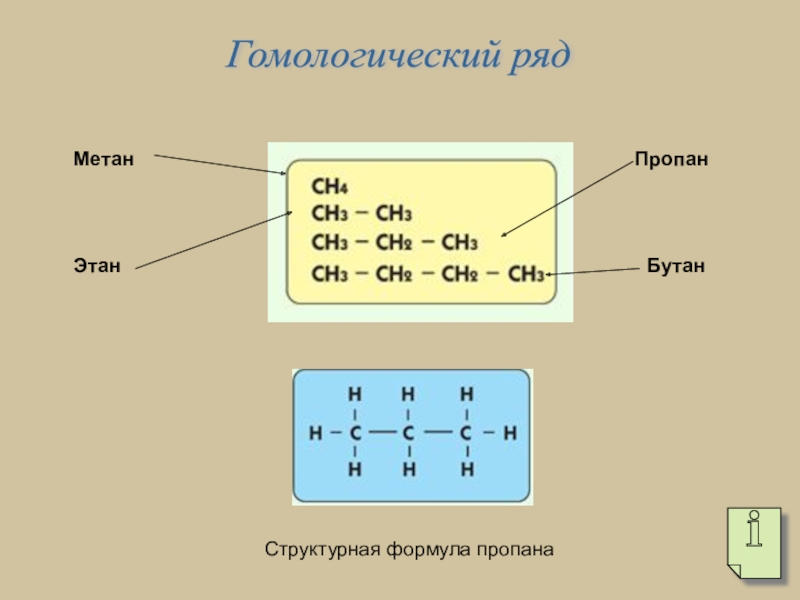
- 12. Гомологический ряд МетанЭтанПропан БутанСтруктурная формула пропана
- 13. Какие вещества называются изомерами?Какие виды изомерии вы
- 14. Изомерия Структурная изомерия. Строение структурных изомеров отражается
- 15. Вариант 1 Вариант 2Составьте 2 изомерапентанаи назовите ихСоставьтегомолог иизомербутана,назовите всевещества.
- 16. Выберите изомеры и гомологи А) СН3⎯СН2⎯ СН2⎯
- 17. Выберите изомеры и гомологи А) СН3⎯СН2⎯ СН2⎯
- 18. Выберите изомеры и гомологи А) СН3⎯СН2⎯ СН2⎯
- 19. Физические свойства Все алканы плохо растворимы в
- 20. Задача
- 21. Получение алкановАлканы выделяют из природных источников (природный
- 22. 2. Гидрирование непредельных углеводородов:
- 23. 4. Термокаталитическое восстановление оксидов углерода:
- 24. 5. Гидролиз карбида алюминия:Аl4С3 + 12Н2О →
- 25. 7. Из солей карбоновых кислот: а)
- 26. Задача
- 27. Химические свойства 1. Реакция замещения2. Реакция дегидрирования3. Реакция горения4. Реакция разложения
- 28. 1 ст. CH4 + Cl2 = CH3Cl
- 29. Реакция разложенияпиролиз метана при 1000о ССН4→С+2Н2
- 30. Реакция дегидрирования - отщепление водорода.При дегидрировании алканов
- 31. Реакция горения.Все алканы горят с образованием углекислого
- 32. Применение Получение ацетиленаГорючее для дизельных и турбореактивных
- 33. Слайд 33
- 34. Задача
- 35. Проверка диктантаВещества, которые имеют одинаковый качественный и
- 36. 4. Углеводороды, состав которых отвечает формуле СnH2n+2,
- 37. Домашнее задание§32, упр. 4-5 Составить презентацию или
Слайд 2
План изучения классов веществ
1. Название класса веществ, общая формула.
2. Особенности электронного
Слайд 4Алканы – углеводороды с общей формулой: СnH2n+2,
в молекулах которых атомы
Слайд 5
АЛКАНЫ (предельные, насыщенные, парафины) –это углеводороды, в молекулах которых атомы связаны
АЛКАНЫ –
название предельных углеводородов по международной номенклатуре (ИЮПАК).
ПАРАФИНЫ –
исторически сохранившееся название предельных углеводородов (от лат. parrum affinis – малоактивный).
ПРЕДЕЛЬНЫМИ, или НАСЫЩЕННЫМИ
эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода.
Слайд 8Модель молекулы пентана.
Алканы с большим числом атомов углерода имеют зигзагообразное
Слайд 13
Какие вещества называются изомерами?
Какие виды изомерии вы знаете?
Сравните формулы веществ, представленных
Изомеры состава С5Н12
Слайд 14Изомерия
Структурная изомерия. Строение структурных изомеров отражается в структурных формулах. В
СН3
⏐
СН3−С−СН2−СН3 СН3− СН2− СН2 − СН2 −СН2−СН3
⏐
СН3
2,2 - диметилбутан
н- гексан
Слайд 15Вариант 1 Вариант 2
Составьте
2 изомера
пентана
и
Составьте
гомолог и
изомер
бутана,
назовите все
вещества.
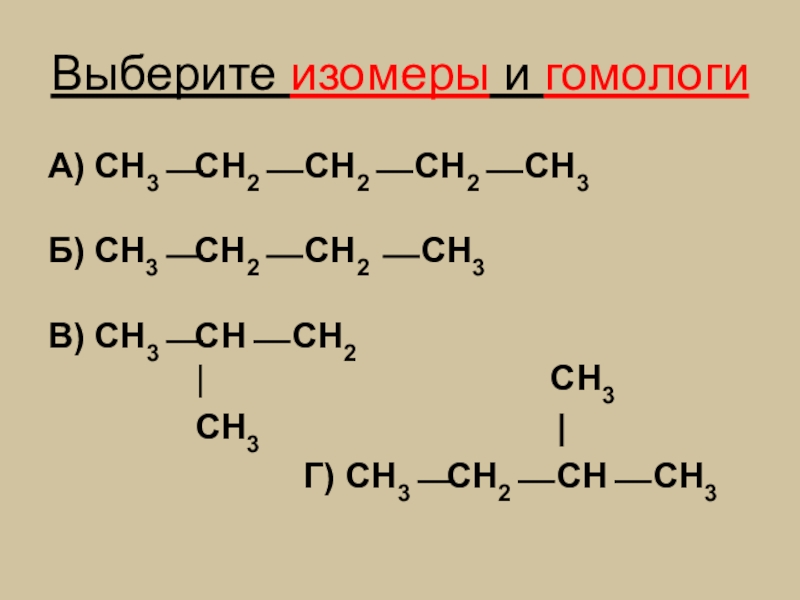
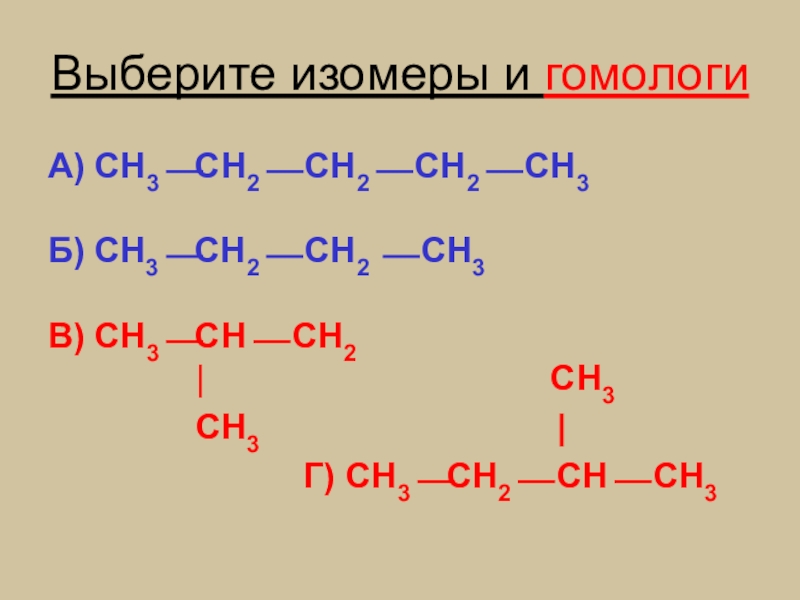
Слайд 16Выберите изомеры и гомологи
А) СН3⎯СН2⎯ СН2⎯ СН2⎯ СН3
Б) СН3⎯СН2⎯ СН2
В) СН3⎯СН⎯ СН2
| СН3
СН3 |
Г) СН3⎯СН2⎯ СН⎯ СН3
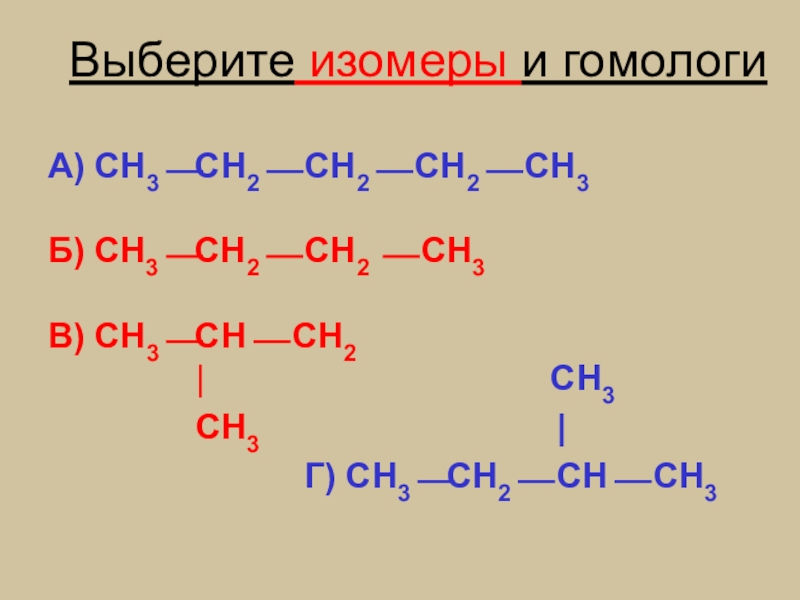
Слайд 17Выберите изомеры и гомологи
А) СН3⎯СН2⎯ СН2⎯ СН2⎯ СН3
Б) СН3⎯СН2⎯ СН2
В) СН3⎯СН⎯ СН2
| СН3
СН3 |
Г) СН3⎯СН2⎯ СН⎯ СН3
Слайд 18Выберите изомеры и гомологи
А) СН3⎯СН2⎯ СН2⎯ СН2⎯ СН3
Б) СН3⎯СН2⎯ СН2
В) СН3⎯СН⎯ СН2
| СН3
СН3 |
Г) СН3⎯СН2⎯ СН⎯ СН3
Слайд 19Физические свойства
Все алканы плохо растворимы в воде. С ростом молекулярной
Начиная с гексадекана, появляются твёрдые алканы.
Слайд 21
Получение алканов
Алканы выделяют из природных источников (природный и попутный газы, нефть,
1. Крекинг алканов:
tº
С8Н 18 → С4Н10 + С4Н8
октан бутан бутен
Слайд 22
2. Гидрирование непредельных углеводородов:
Ni, tº, р
С2Н4 + Н2 → С2Н6
этилен этан
Рt, tº, р
С2Н2 + Н2 → С2Н6
ацетилен этан
3. Гидрирование угля:
кt, tº, р
С + 2Н2 → СН4 ↑
метан
Слайд 23
4. Термокаталитическое восстановление оксидов углерода:
СО + 3Н2 → СН4 ↑+ Н2О
Изменяя катализаторы, можно получить более тяжелые алканы: этан, пропан, бутан.
Ni, tº
СО + 4Н2 → СН4 ↑+ 2Н2О
Слайд 24
5. Гидролиз карбида алюминия:
Аl4С3 + 12Н2О → 4Al(ОН)3 + 3СН4↑
6. Реакция Вюрца:
tº
2СН3Вr + 2Nа → СН3 –СН3 + 2NaBr
бромметан
этан
Слайд 25
7. Из солей карбоновых кислот:
а) электролиз раствора
2СН3COONa + 2H2O → СН3–СН3 + 2CO2 ↑ + H2↑+ 2NaOH
ацетат натрия
б) сплавление со щелочью
t
СН3СООNa + NaОН → СН4↑ + Na2СО3
Слайд 27Химические свойства
1. Реакция замещения
2. Реакция дегидрирования
3. Реакция горения
4. Реакция разложения
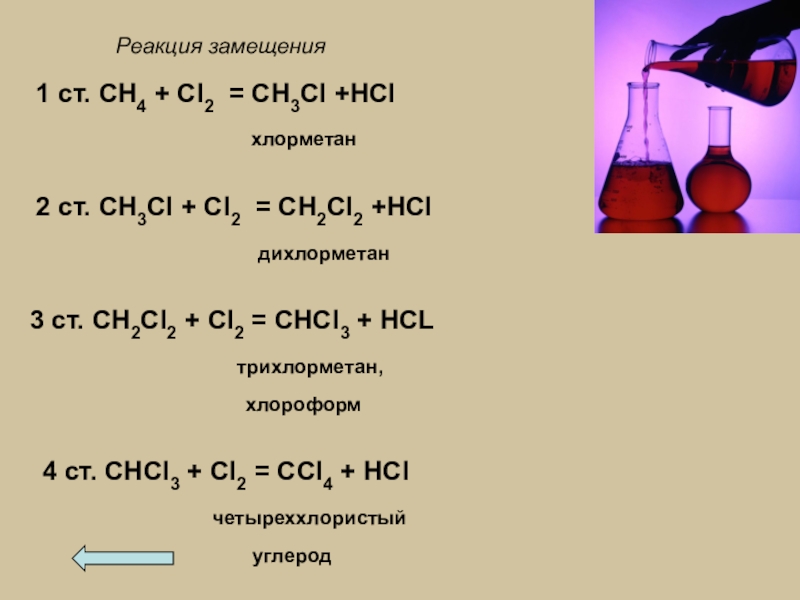
Слайд 281 ст. CH4 + Cl2 = CH3Cl +HCl
2 ст. CH3Cl + Cl2 = CH2Cl2 +HCl
дихлорметан
3 ст. CH2Cl2 + Cl2 = CHCl3 + HCL
трихлорметан,
хлороформ
4 ст. CHCl3 + Cl2 = CCl4 + HCl
четыреххлористый
углерод
Реакция замещения
Слайд 30Реакция дегидрирования - отщепление водорода.
При дегидрировании алканов образуются алкены и другие
Например, дегидрирование пентана:
С5Н12 → С5Н10 + Н2
пентен
Слайд 31Реакция горения.
Все алканы горят с образованием углекислого газа и воды
2С4Н10 +
Например: горение бутана.
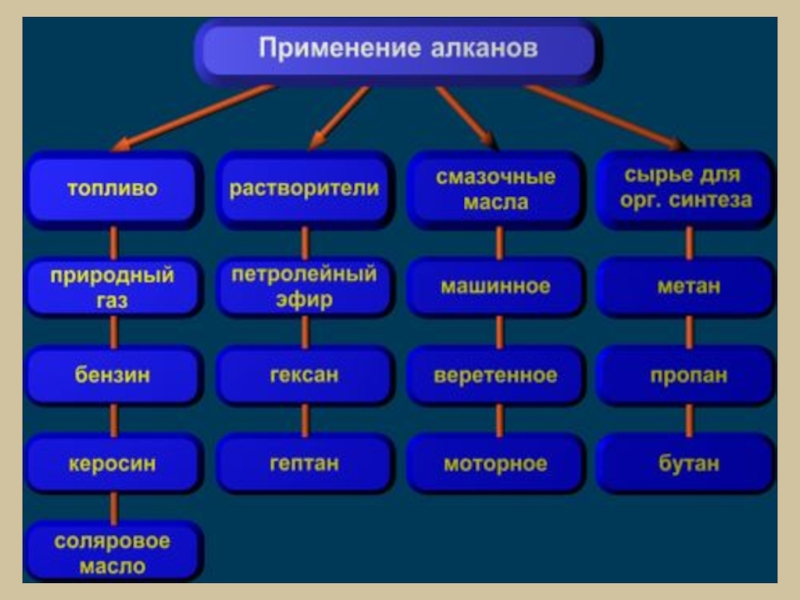
Слайд 32Применение
Получение ацетилена
Горючее для дизельных и турбореактивных двигателей
Получение растворителей
В металлургии
А также
Слайд 35Проверка диктанта
Вещества, которые имеют одинаковый качественный и количественный состав, но разное
2. Вещества, которые состоят из атомов углерода и водорода, называются углеводородами.
3. Вещества, сходные по строению и свойствам, но отличающиеся на одну или несколько групп СН2, называются гомологами.
Слайд 364. Углеводороды, состав которых отвечает формуле СnH2n+2, называются алканами.
5. СH4
6. С3H8 пропан
7. Бутан С4H10
8. Этан С2H6
9. Пентан С5H12
10. С6H14 гексан
11. Метил СH3
12. Этил С2H5
Слайд 37Домашнее задание
§32, упр. 4-5
Составить презентацию или реферат о:
истории открытия алканов,
происхождении названия,
применении алканов,
влиянии алканов на организм человека,
перспективах использования другого вида топлива (спирт, водород).