- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Алюминий
Содержание
- 1. Презентация по химии Алюминий
- 2. Алюминий
- 3. Цели урока:Изучить свойства металлов 3 А группы
- 4. Алюминий находится в _ периоде,
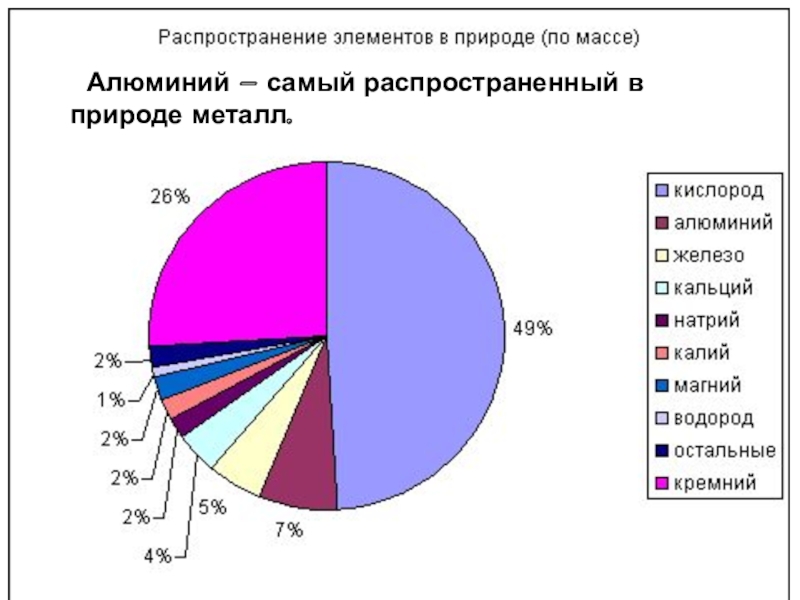
- 5. Алюминий – самый распространенный в природе металл.
- 6. В природе алюминий в связи с высокой
- 7. 3ВеО · Al2О3 · 6SiO2Изумруд аквамаринБерилл
- 8. Алуниты — (Na,K)2SO4·Al2(SO4)3·4Al(OH)3Корунд Al2O3Рубин Сапфир
- 9. BeAl2O4.Александрит Хризоберилл
- 10. ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯНазвание соединенияФормулаСодержание AlКаолинит БокситПолевой шпатКорундНефелинAl2O3*2SiO2*H2OAl2O3* H2OK2O*Al2O3*6SiO2Al2O3Na2O*Al2O3*2SiO222,5%45%10%53%19%
- 11. История открытия алюминияОРИХАЛКДо сих пор не разгадана
- 12. Древний историк Плиний Старший рассказывает об интересном событии.
- 13. Квасцы служили не только делу мира, но
- 14. в XVI веке, т. е. спустя примерно полторы тысячи лет,
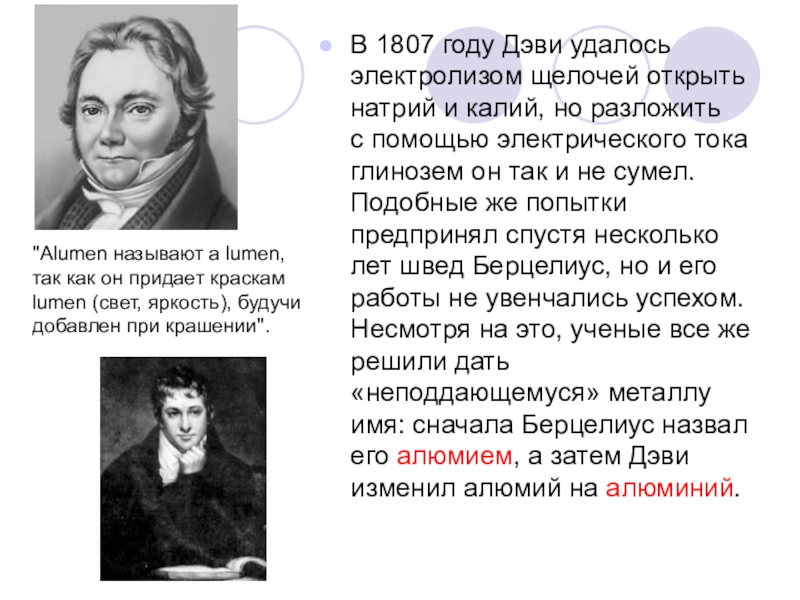
- 15. В 1807 году Дэви удалось электролизом щелочей открыть натрий
- 16. В чистом виде его впервые получил
- 17. в 19 веке на императорских приемах алюминиевая
- 18. Алюминий был дороже золота. Так дорог,
- 19. Алюминий – серебристый металл, его плотность
- 20. Химические свойстваГорение алюминия в кислородеХимически активен. Легко
- 21. Металлический алюминий является сильным восстановителем и восстанавливает другие металлы из их оксидов:
- 22. Взаимодействие алюминия с водойХимические свойства
- 23. Слайд 23
- 24. 2Al + 6H2O + 2KOH =
- 25. Применение алюминия и его соединений В
- 26. Слайд 26
- 27. Сплавы алюминия используют в строительстве, т.
- 28. Производство алюминиевых труб.
- 29. Алюминий очень технологичный металл: его можно
- 30. Гель из гидроксида алюминия входит
- 31. Получение алюминия Впервые получен восстановлением хлорида
- 32. Слайд 32
- 33. Алюминий –металл будущего
- 34. Выполните тест1. Самым распространенным в земной коре
- 35. Выполните тест1. Самым распространенным в земной коре
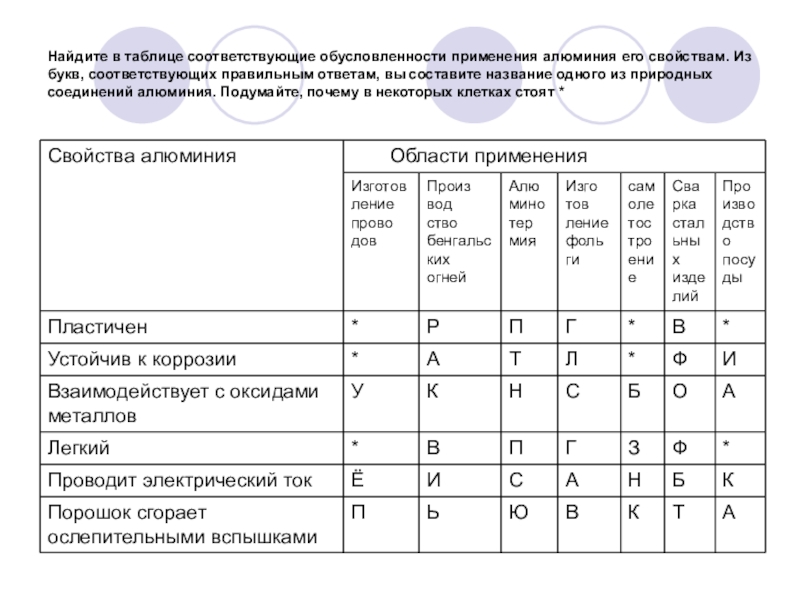
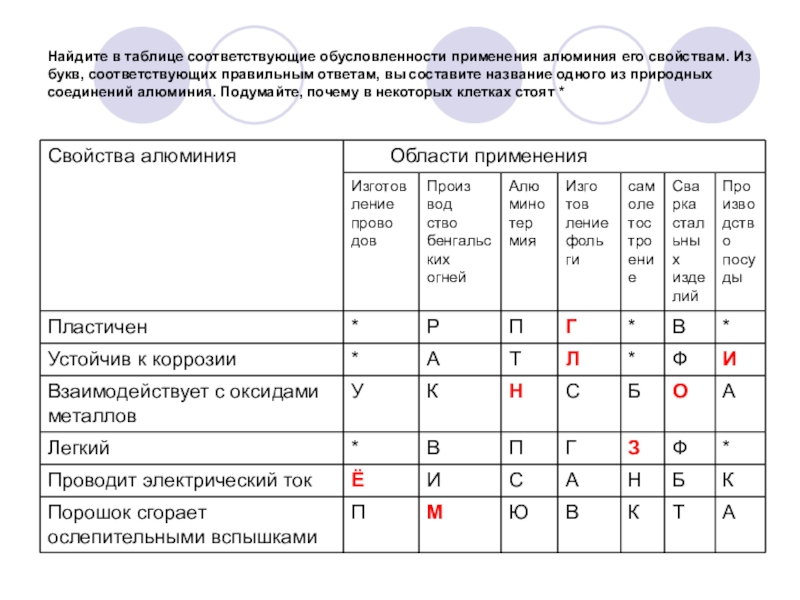
- 36. Найдите в таблице соответствующие обусловленности применения алюминия
- 37. Найдите в таблице соответствующие обусловленности применения алюминия
Слайд 3Цели урока:
Изучить свойства металлов 3 А группы на примере алюминия.
Дать
На основе строения атома рассмотреть его физические и химические свойства, указать области применения алюминия.
Ответить на вопрос: « Почему алюминий называют металлом будущего?»
Слайд 4Алюминий находится в _ периоде, _ группе. Порядковый
3
3А
13
27
13
14
13
+13
3
3
+3
Слайд 6В природе алюминий в связи с высокой химической активностью встречается почти
Бокситы
Al2O3 · H2O (с примесями SiO2, Fe2O3, CaCO3) Нефелины — KNa3[AlSiO4]4
Глинозёмы (смеси каолинов с песком SiO2, известняком CaCO3, магнезитом MgCO3)
Полевые шпаты
(K,Na)2O·Al2O3·6SiO2, Ca[Al2Si2O8]
Каолинит — Al2O3·2SiO2 · 2H2O
Слайд 10ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ
Название соединения
Формула
Содержание Al
Каолинит
Боксит
Полевой шпат
Корунд
Нефелин
Al2O3*2SiO2*H2O
Al2O3* H2O
K2O*Al2O3*6SiO2
Al2O3
Na2O*Al2O3*2SiO2
22,5%
45%
10%
53%
19%
Слайд 11История открытия алюминия
ОРИХАЛК
До сих пор не разгадана тайна Атлантиды - легендарного
Слайд 12Древний историк Плиний Старший рассказывает об интересном событии. Однажды к римскому императору Тиберию,
Написанные им 37 томов "Естественной истории" наиболее полно отражают знания, накопленные на протяжении веков в странах древнего мира.
У него мы находим слово "алюмен" (что означает "вяжущий"). Нет, это еще не алюминий, а лишь одно из его соединений. Так Плиний называл квасцы, которые тогда уже применяли красильщики в качестве протравы при окраске тканей.
Слайд 13Квасцы служили не только делу мира, но иногда применялись и на
Их словно заколдовали. Враги так и не поняли, что за чудо произошло. А ведь в те времена верили в чудеса и сверхъестественные силы! Но все оказалось гораздо проще. Римляне, видимо, знали кое-что о квасцах. Они обмазали деревянные башни и стены раствором квасцов, и дерево стало огнестойким. Прошло почти полторы тысячи лет, прежде чем ученые по-настоящему заинтересовались квасцами и попытались разгадать тайну их состава.
Слайд 14в XVI веке, т. е. спустя примерно полторы тысячи лет, в историю алюминия была вписана
Исследуя различные вещества и минералы, в том числе квасцы, Парацельс установил, что они «есть соль некоторой квасцовой земли», в состав которой входит окись неизвестного металла, впоследствии названная глиноземом.
Слайд 15В 1807 году Дэви удалось электролизом щелочей открыть натрий и калий, но разложить с помощью электрического
"Alumen называют a lumen, так как он придает краскам lumen (свет, яркость), будучи добавлен при крашении".
Слайд 16 В чистом виде его впервые получил датский физик Х. Эрстед
в 1827 г. Велер выделил металлический алюминий нагреванием безводного хлористого алюминия с металлическим калием.
В 1854 г. француз А. Сент- Клер Девиль получил его посредством электролиза.
Слайд 17в 19 веке на императорских приемах алюминиевая посуда была самой престижной.
Слайд 18 Алюминий был дороже золота. Так дорог, что из него делали
украшения. В Англии хотели почтить
богатым подарком нашего великого химика Менделеева.
и сделали химические весы, в которых одна чаша была из золота,
другая из алюминия. Чаша из алюминия стоила дороже золотой.
Слайд 19 Алюминий – серебристый металл, его плотность – 2,7 г/ см3,
Слайд 20Химические свойства
Горение алюминия в кислороде
Химически активен. Легко окисляется кислородом воздуха, при
Без оксидной пленки алюминий активно взаимодействует с неметаллами. При обычной температуре реагирует с хлором и бромом, а с фтором и йодом –лишь при нагревании.
Слайд 21 Металлический алюминий является сильным восстановителем и восстанавливает другие металлы из
Слайд 22Взаимодействие алюминия с водой
Химические свойства
Взаимодействие алюминия с сложными
Алюминий взаимодействует с кислотами, щелочами и солями
Слайд 23
Поместите в три пробирки алюминий. В первую пробирку добавьте раствор соляной кислоты, во вторую –раствор гидроксида натрия, в третью –раствор сульфата меди (II). Объясните явления. Напишите уравнения в молекулярном и ионном виде.
Слайд 24 2Al + 6H2O + 2KOH = 2K Al(OH)4 +3H2
Тетрагидроксоалюминат
Напишите уравнение реакции взаимодействия алюминия с соляной кислотой и разберите её с т. з. окисления – восстановления.
Алюминий без оксидной пленки активно взаимодействует с водой:
Слайд 25Применение алюминия и его соединений
В чистом виде алюминий находит
Большая часть производимого алюминия идет для получения легких сплавов.
Дуралюмин по прочности на разрыв близок к стали, но почти в 3 раза легче её. Его используют для производства самолетов.
Слайд 27
Сплавы алюминия используют в строительстве, т. к. из них легко
Слайд 29 Алюминий очень технологичный металл: его можно обрабатывать давлением при нормальных
Слайд 30 Гель из гидроксида алюминия входит в состав лекарств для
Гидроксид алюминия используется для очистки воды, т. к. обладает способностью поглощать различные вещества.
Оксид алюминия в виде корунда используется как абразивный материал для обработки металлических изделий.
Оксид алюминия в виде рубина широко используется в лазерной технике.
Оксид алюминия применяется в качестве катализатора, для разделения веществ в хроматографии.
Слайд 31Получение алюминия
Впервые получен восстановлением хлорида алюминия металлическим калием или
AlCl3 + 3Na = Al + 3NaCl
2. В промышленности – электролиз раствора глинозема Al2O3 в расплаве криолита Na3AlF6 с добавкой CaF2. криолит используется как растворитель оксида алюминия, а добавка фторида кальция позволяет поддерживать температуру плавления в электролитической ванне не выше 1000 0С.
Слайд 34Выполните тест
1. Самым распространенным в земной коре металлом является
а) Са б)
2. Алюминий входит в состав следующего природного соединения
а) сильвинит б) кальцит в) гипс г) корунд
3. При растворении алюминия в воде получается раствор
а) алюминия б) оксида алюминия в) гидроксида алюминия
г) гидрида алюминия
4. В ряду Na – Мg – Аl – Si
а) увеличивается число энергетических уровней в атомах
б) усиливаются металлические свойства элементов
в) уменьшается высшая степень окисления элементов
г) ослабевают металлические свойства элементов
Слайд 35Выполните тест
1. Самым распространенным в земной коре металлом является
а) Са б)
2. Алюминий входит в состав следующего природного соединения
а) сильвинит б) кальцит в) гипс г) корунд
3. При растворении алюминия в воде получается раствор
а) алюминия б) оксида алюминия в) гидроксида алюминия
г) гидрида алюминия
4. В ряду Na – Мg – Аl – Si
а) увеличивается число энергетических уровней в атомах
б) усиливаются металлические свойства элементов
в) уменьшается высшая степень окисления элементов
г) ослабевают металлические свойства элементов