- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии АЛКАНЫ
Содержание
- 1. Презентация по химии АЛКАНЫ
- 2. Алканы - это насыщенные или предельные углеводороды.
- 3. Между атомами C и H присутствуют прочные,
- 4. Все 4 гибридные орбитали атома С идентичны
- 5. Простейшим представителем класса является метан (CH4). Углеводород с самой
- 6. Алканы, число атомов углерода в которых больше
- 7. Физические свойства алканов.Алканы – это вещества, которые
- 8. Физические свойства алканов.Газообразные алканы способны гореть бледно-голубым
- 9. Химические свойства Данные соединения являются малоактивными в
- 10. Химические свойства Алканы взаимодействуют только с азотной
- 11. Химические свойства Алканы способны к окислению. В
- 12. Химические свойства Также окисление алканов может производиться
- 13. Химические свойства При воздействии ультрафиолетового излучения алканы
- 14. Предельные углеводороды достаточно широко распространены в природе.
- 15. Также алканы можно получить методом коксования каменного
- 16. Также метан можно получить в лабораторных условиях,
- 17. Алканы на бытовом уровне широко применяются во
- 18. Холодильник, который есть в доме у каждого,
- 19. В качестве растворителя и для синтеза различных
- 20. Парафин является смесью высших алканов, а так
- 21. Спасибо за внимание!
Алканы - это насыщенные или предельные углеводороды. Также можно сказать, что это углеводороды, в которых соединение атомов C осуществляется посредством простых связей. Общая формула имеет вид:
Слайд 2Алканы - это насыщенные или предельные углеводороды. Также можно сказать, что
это углеводороды, в которых соединение атомов C осуществляется посредством простых связей.
Общая формула имеет вид:
Общая формула имеет вид:
Также существует более древнее наименование, которое лучше всего отражает их относительную химинертность – парафины, что в переводе означает «лишенные сродства».
CnH₂n+ 2
Слайд 3Между атомами C и H присутствуют прочные, весьма малополярные s-связи. Атомы
же вокруг простых связей всегда вращаются, ввиду чего молекулы алканов принимают разнообразные формы, причем длина связи, угол между ними - постоянные величины.
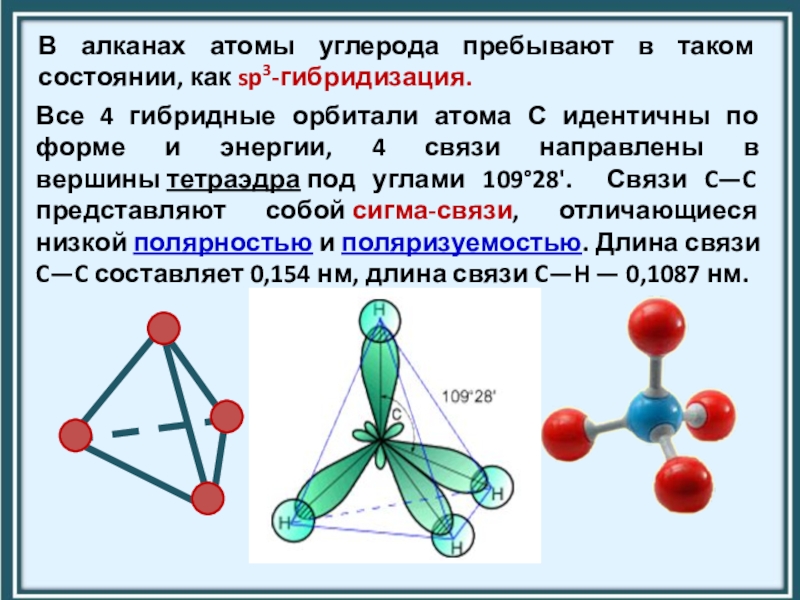
Слайд 4Все 4 гибридные орбитали атома С идентичны по форме и энергии,
4 связи направлены в вершины тетраэдра под углами 109°28'. Связи C—C представляют собой сигма-связи, отличающиеся низкой полярностью и поляризуемостью. Длина связи C—C составляет 0,154 нм, длина связи C—H — 0,1087 нм.
В алканах атомы углерода пребывают в таком состоянии, как sp3-гибридизация.
Слайд 5Простейшим представителем класса является метан (CH4). Углеводород с самой длинной цепью — нонаконтатриктан ( C390H782
) синтезировали в 1985 году английские химики И. Бидд и М. К. Уайтинг.
Слайд 6Алканы, число атомов углерода в которых больше трёх, имеют изомеры. Изомерия предельных углеводородов
обусловлена простейшим видом структурной изомерии — изомерией углеродного скелета, а начиная с C7H16 — также оптической изомерией.
Слайд 7Физические свойства алканов.
Алканы – это вещества, которые не имеют цвета и
нерастворимы в воде. Температура, при которой алканы начинают плавиться, и температура, при которой они закипают, повышаются в соответствии с увеличением молекулярной массы и длины углеводородной цепи. От менее разветвленных к более разветвленным алканам температуры кипения и плавления понижаются.
Слайд 8Физические свойства алканов.
Газообразные алканы способны гореть бледно-голубым либо бесцветным пламенем, при
этом выделяется довольно много тепла. СН4-С4Н10 представляют собой газы, у которых отсутствует также и запах. С5Н12-С15Н32 – это жидкости, которые обладают специфическим запахом. С15Н32 и так далее – это твердые вещества, которые также не имеют запаха.
Слайд 9Химические свойства
Данные соединения являются малоактивными в химическом плане, что можно
объяснить прочностью трудноразрываемых сигма-связей - С-С и С-Н. Также стоит учитывать, что связи С-С неполярны, а С-Н малополярны. Таким образом, химические свойства алканов в основном ограничиваются реакциями радикального замещения.
Слайд 10Химические свойства
Алканы взаимодействуют только с азотной кислотой с концентрацией 10%
либо с оксидом четырехвалентного азота в газовой среде при температуре 140°С.
В результате образуются нитросоединения и вода: CH4 + азотная кислота (разбавленная) = CH3 – NO2 (нитрометан) + вода.
В результате образуются нитросоединения и вода: CH4 + азотная кислота (разбавленная) = CH3 – NO2 (нитрометан) + вода.
Слайд 11Химические свойства
Алканы способны к окислению. В зависимости от того, какие
условия сопровождают реакцию и как их изменяют, можно из одного и того же вещества получить различные конечные продукты. Мягкое окисление метана кислородом при наличии катализатора, ускоряющего реакцию, и температуры около 200 °С может дать в результате следующие вещества:
спирт – метанол;
альдегид – метаналь или формальдегид;
карбоновая кислота, метановая или муравьиная.
спирт – метанол;
альдегид – метаналь или формальдегид;
карбоновая кислота, метановая или муравьиная.
Слайд 12Химические свойства
Также окисление алканов может производиться в газообразной или жидкой
среде воздухом. Такие реакции приводят к образованию высших жирных спиртов и соответствующих кислот.
Слайд 13Химические свойства
При воздействии ультрафиолетового излучения алканы способны реагировать со смесью
хлора и диоксида серы. В результате образуется хлороводород, а также алкильный радикал, который присоединяет к себе диоксид серы.
Образовавшиеся в результате реакции сульфонилхлориды находят широкое применение в производстве поверхностно-активных веществ.
Образовавшиеся в результате реакции сульфонилхлориды находят широкое применение в производстве поверхностно-активных веществ.
Слайд 14Предельные углеводороды достаточно широко распространены в природе. Например, метан, образуется при
разложении животных и растительных организмов в болотистых местах (без доступа воздуха). Кроме того, это соединение присутствует в угольных шахтах, что часто приводит к серьезным взрывам и гибели шахтеров. Предельные углеводороды в большом количестве содержатся в твердом, жидком, а также газообразном виде в нефти. Помимо метана в нефти есть пропан, этан, бутан, пентан.
Слайд 15Также алканы можно получить методом коксования каменного угля. В природе встречаются
и так называемые твердые алканы – озокериты, которые представлены в виде залежей горного воска. Озокерит можно обнаружить в восковых покрытиях растений или их семян, а также в составе пчелиного воска.
Слайд 16Также метан можно получить в лабораторных условиях, используя метод нагревания ацетата
натрия с твердой щелочью или гидролизом некоторых карбидов. А можно получить способом декарбоксилирования карбоновых кислот при их электролизе.
Слайд 17Алканы на бытовом уровне широко применяются во многих сферах деятельности человека.
Ведь очень сложно представить нашу жизнь без природного газа. И ни для кого не будет секретом, что основой природного газа является метан, из которого производят технический углерод, используемый при производстве топографических красок и шин.
Слайд 18Холодильник, который есть в доме у каждого, также работает благодаря соединениям
алканов, применяющихся в качестве хладагентов.
А полученный из метана ацетилен используют для сварки и резки металлов.
Алканы присутствуют в составе бензина, керосина, солярового масла и мазута. Кроме этого, они есть и в составе смазочных масел.
А полученный из метана ацетилен используют для сварки и резки металлов.
Алканы присутствуют в составе бензина, керосина, солярового масла и мазута. Кроме этого, они есть и в составе смазочных масел.
Слайд 19В качестве растворителя и для синтеза различных полимеров, широкое применение нашел
циклогексан.
А в наркозе используют циклопропан.
Сквалан, как высококачественное смазочное масло, является компонентом многих фармацевтических и косметических препаратов.
А в наркозе используют циклопропан.
Сквалан, как высококачественное смазочное масло, является компонентом многих фармацевтических и косметических препаратов.
Слайд 20Парафин является смесью высших алканов, а так как он нетоксичен, то
широко используется в пищевой промышленности. Его применяют при пропитки упаковок для молочной продукции, соков, круп и так далее, при изготовлении жевательных резинок. А разогретый парафин используют при парафинолечении.
Из парафина получают вазелин, который нашел широкое применение как в парфюмерии и косметологии, так и в медицине.
Из парафина получают вазелин, который нашел широкое применение как в парфюмерии и косметологии, так и в медицине.