- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 9 класс Спирты
Содержание
- 1. Презентация по химии 9 класс Спирты
- 2. О чем пойдет речь сегодня на уроке?
- 3. Урок химии в 9 классеУчитель Крапивкина Т.М. Спирты
- 4. ЦелепологаниеС чем связано такое поведение людей?Какую проблему вы увидели в данной теме?Что вы знаете о спиртах?
- 5. Слайд 5
- 6. Слайд 6
- 7. ПроблемыСвойства спиртов Влияние спиртов на организм(алкоголизм) Значение спиртов Спирт хорошо это или плохо?
- 8. 1.Понятие о спиртах. Если в молекулах У.В.
- 9. Слайд 9
- 10. ОН – группа называется функциональной группой.Функциональной называется группа атомов, определяющая принадлежность вещества к определённому классу.
- 11. Запомним, друг, и
- 12. Классификация спиртов1) СН3 -СН2 -СН2 -ОН
- 13. Классификация спиртов
- 14. Номенклатура спиртов. Задание 2. Просмотрите таблицу и сделайте вывод о номенклатуре спиртов
- 15. Номенклатура спиртовСН3 –СН-СН2-ОН СН2
- 16. Г) Н3С – СН – СН2 –
- 17. ВыводНазвания одноатомных спиртов
- 18. Одноатомный спирт - метанолЖидкость без цвета с
- 19. Метанол - ядЯдовитое действие метанола основано на
- 20. Одноатомный спирт - этанолБесцветная жидкость с характерным
- 21. Физические свойстваЗадание 5 :Исследование свойств спиртов (инструкция).
- 22. Задание 6. Сравните физические свойства
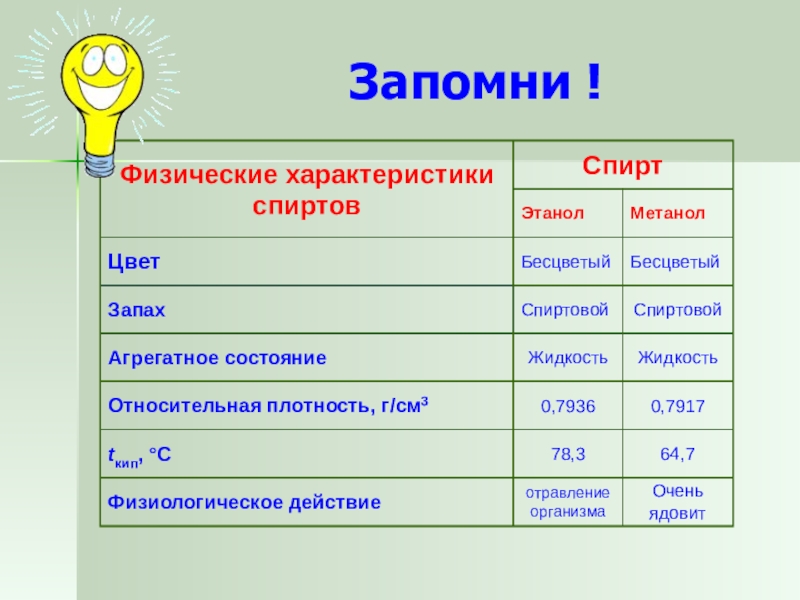
- 23. Запомни !
- 24. Химические свойстваГорение спиртов (эксперимент).С2Н5ОН + 3О2 2СО2+ 3Н2О
- 25. Вывод Химические свойства спиртов определяются наличием функциональной группы - ОН.
- 26. Получение спиртов Метанол
- 27. Применение этилового спиртаПроизводство каучука (резины), исходя из
- 28. Этанол в косметике и парфюмерии— растворитель для духов и лосьонов.
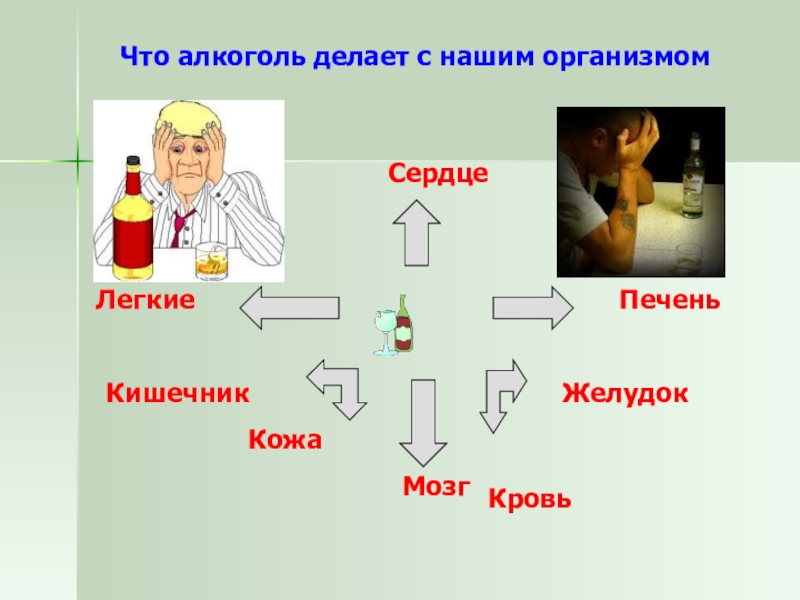
- 29. Что алкоголь делает с нашим организмом
- 30. Вредное воздействие этанола В начале опьянения страдают
- 31. Вредное воздействие этанолаИзменения структуры мозга, вызванные многолетней
- 32. Вредное воздействие этанолаАлкоголь крайне неблагоприятно влияет на
- 33. Многоатомный спирт -этиленгликольЭтиленгликоль — представитель предельных двухатомных
- 34. Применение этиленгликоляВажным свойством этиленгликоля является способность понижать
- 35. Этиленгликоль - яд Дозы вызывающие смертельное отравление
- 36. Многоатомный спирт - глицеринГлицерин – трехатомный предельный
- 37. Применение глицеринаПрименяется в производстве взрывчатых веществ нитроглицерина.При
- 38. Качественная реакция на многоатомные спирты
- 39. Качественная реакция на многоатомные спиртыРеакцией на многоатомные
- 40. Рефлексия:Вино губит … Если в трезвом состоянии
- 41. «Вино губит телесное здоровье людей,
- 42. Степень сложности заданий******Закрепление
- 43. 123456789101112Дидактическая игра
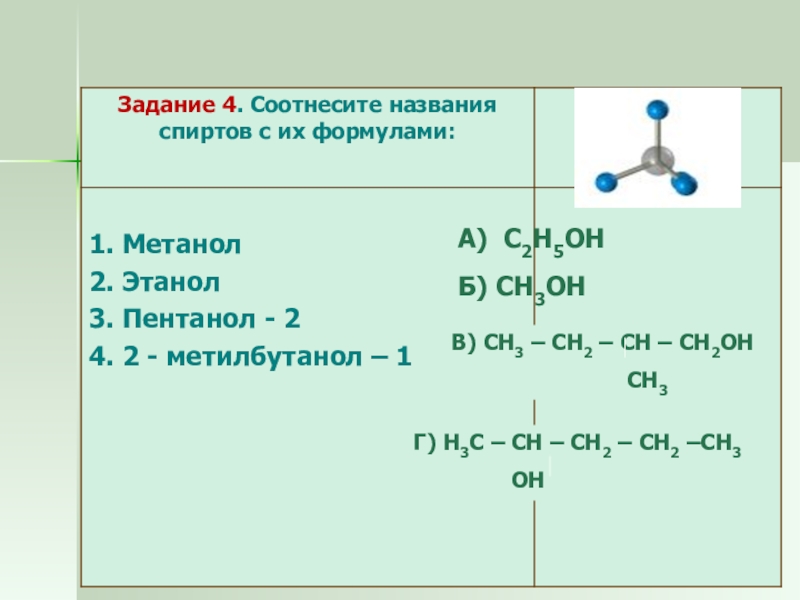
- 44. 1.Что такое спирты?
- 45. 3.Какие химические свойства спиртов вы знаете?
- 46. 4.Какие спирты растворимы?
- 47. 5.Как можно охарактеризовать физические свойства спиртов?
- 48. 6.Какие из спиртов ядовиты?
- 49. 7.Какие свойства метилового и этилового спирта находят применение?
- 50. Где применяют спирты?8
- 51. 9.Как называют функциональную группу спиртов – OH?
- 52. 10.Как образуют названия одноатомных спиртов?
- 53. Какое агрегатное состояние не характерно для спиртов при обычных условиях?2
- 54. 11.Что такое гигроскопичность?
- 55. Какова общая формула предельных одноатомных спиртов?12
- 56. РефлексияРазрешили ли вы проблему, поставленную в начале
- 57. Домашнее задание§ 35.Эссе «Вино сообщает каждому,
О чем пойдет речь сегодня на уроке?
Слайд 4Целепологание
С чем связано такое поведение людей?
Какую проблему вы увидели в данной
теме?
Что вы знаете о спиртах?
Что вы знаете о спиртах?
Слайд 5
Вывод
Этиловый спирт - наркотик При приеме внутрь он вследствие высокой растворимости быстро всасывается в кровь и возбуждающе действует на организм. Под влиянием спиртного у человека ослабевает внимание, затормаживается реакция, нарушается координация, появляется развязность, грубость в поведении.
Но следствия употребления алкоголя могут быть и более глубокими. При частом потреблении появляется привыкание, пагубное пристрастие к нему и в конце концов тяжелое заболевание алкоголизм.
Этиловый спирт - наркотик При приеме внутрь он вследствие высокой растворимости быстро всасывается в кровь и возбуждающе действует на организм. Под влиянием спиртного у человека ослабевает внимание, затормаживается реакция, нарушается координация, появляется развязность, грубость в поведении.
Но следствия употребления алкоголя могут быть и более глубокими. При частом потреблении появляется привыкание, пагубное пристрастие к нему и в конце концов тяжелое заболевание алкоголизм.
Слайд 6
Цели и задачи урока:
образовательные: - Рассмотреть состав и строение спиртов. Познакомиться
с отдельными представителями спиртов, их свойствами, способами
получения. Выяснить влияние спиртов на живые организмы.
Решить для себя: спирт это хорошо или плохо.
воспитательные: - продолжить формирование познавательного интереса
к предмету через использование нестандартных форм обучения и создания
ситуации успеха
развивающие: - продолжить развитие учебно-интеллектуальных умении:
выделять главное и существенное, устанавливать причинно-следственные
связи (развитие логического мышления)
- продолжить развитие учебно-организационных умений: организовать себя
на выполнение поставленной задачи, осуществлять самоконтроль и
самоанализ учебной деятельности, развивать критическое мышление.
образовательные: - Рассмотреть состав и строение спиртов. Познакомиться
с отдельными представителями спиртов, их свойствами, способами
получения. Выяснить влияние спиртов на живые организмы.
Решить для себя: спирт это хорошо или плохо.
воспитательные: - продолжить формирование познавательного интереса
к предмету через использование нестандартных форм обучения и создания
ситуации успеха
развивающие: - продолжить развитие учебно-интеллектуальных умении:
выделять главное и существенное, устанавливать причинно-следственные
связи (развитие логического мышления)
- продолжить развитие учебно-организационных умений: организовать себя
на выполнение поставленной задачи, осуществлять самоконтроль и
самоанализ учебной деятельности, развивать критическое мышление.
Слайд 7Проблемы
Свойства спиртов
Влияние спиртов на организм(алкоголизм)
Значение спиртов
Спирт
хорошо это или плохо?
Слайд 81.Понятие о спиртах.
Если в молекулах У.В. атом водорода
заместить на гидроксильную группу, то
получатся соединения относящиеся к
классу спиртов.
Задание 1:
Напишите структурную формулу этана и один атом водорода
замените на ОН группу.
получатся соединения относящиеся к
классу спиртов.
Задание 1:
Напишите структурную формулу этана и один атом водорода
замените на ОН группу.
Слайд 9
Спиртами называются
органические вещества, в которых гидроксильная группа связана с углеводородным радикалом.
С2Н6 – этан;
С2Н5 – ОН – этанол.
Слайд 10ОН – группа называется функциональной группой.
Функциональной называется
группа атомов, определяющая
принадлежность
вещества к определённому классу.
Слайд 11 Запомним, друг, и я и ты,
Чем отличаются спирты.
В них углерод и гидроксид,
И каждый спирт легко
горит.
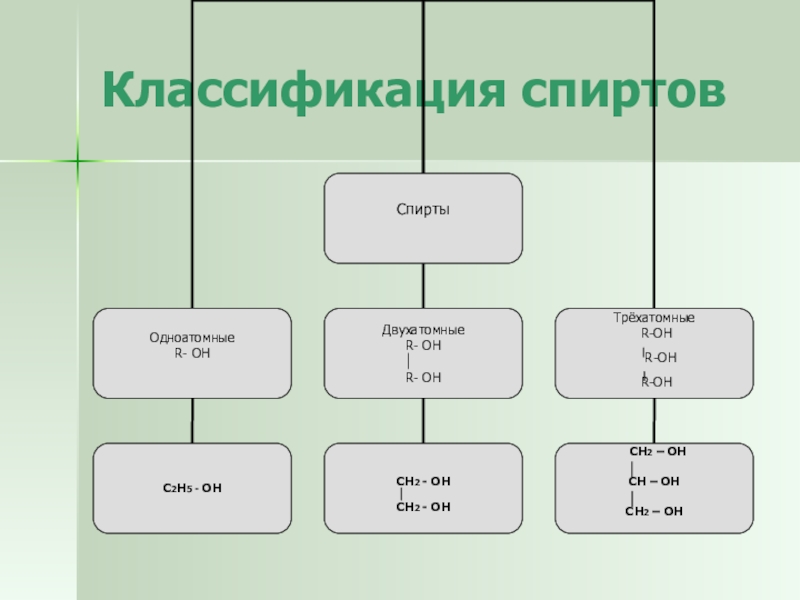
Слайд 12Классификация спиртов
1) СН3 -СН2 -СН2 -ОН 2)
СН2 – СН2
| |
ОН ОН
3) СН2 – СН - СН2
| | | 4) СН3 - ОН
ОН ОН ОН
| |
ОН ОН
3) СН2 – СН - СН2
| | | 4) СН3 - ОН
ОН ОН ОН
Слайд 14 Номенклатура спиртов. Задание 2. Просмотрите таблицу и сделайте вывод
о номенклатуре спиртов
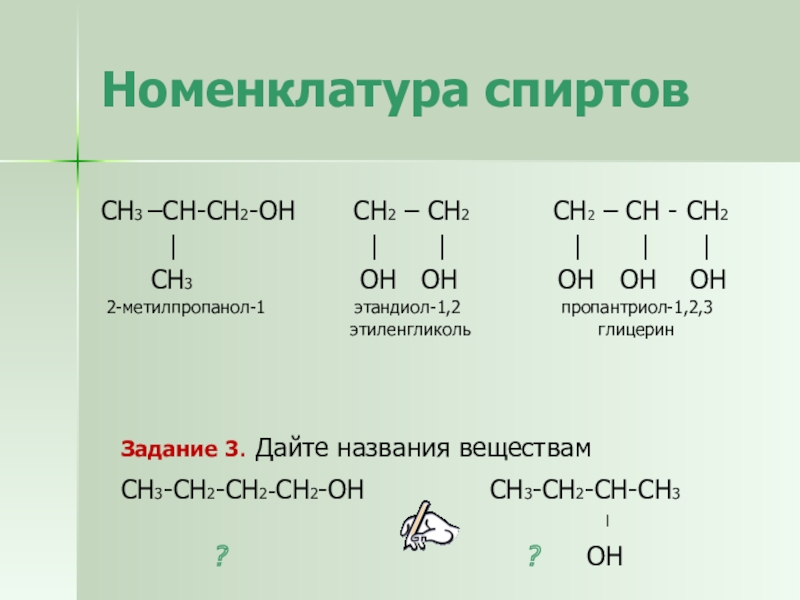
Слайд 15Номенклатура спиртов
СН3 –СН-СН2-ОН СН2 – СН2
СН2 – СН - СН2
| | | | | |
СН3 ОН ОН ОН ОН ОН
2-метилпропанол-1 этандиол-1,2 пропантриол-1,2,3
этиленгликоль глицерин
| | | | | |
СН3 ОН ОН ОН ОН ОН
2-метилпропанол-1 этандиол-1,2 пропантриол-1,2,3
этиленгликоль глицерин
Задание 3. Дайте названия веществам
СН3-СН2-СН2-СН2-ОН СН3-СН2-СН-СН3
l
? ? ОН
Слайд 17 Вывод
Названия одноатомных спиртов образуются из названия углеводорода
с самой длинной углеродной цепью, содержащей гидроксильную группу, путём добавления суффикса -ол.
Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, ...) указывается количество гидроксильных групп.
Например: CH3-CH2-OH этанол
Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, ...) указывается количество гидроксильных групп.
Например: CH3-CH2-OH этанол
Слайд 18Одноатомный спирт - метанол
Жидкость без цвета с температурой кипения 64С, характерным
запахом Легче воды. Горит бесцветным пламенем.
Применяется в качестве растворителя и
топлива в двигателях внутреннего сгорания.
Применяется в качестве растворителя и
топлива в двигателях внутреннего сгорания.
Слайд 19Метанол - яд
Ядовитое действие метанола основано на поражении нервной и сосудистой
системы. Приём внутрь 5—10 мл метанола приводит к тяжёлому отравлению, а 30 мл и более — к смерти.
Слайд 20Одноатомный спирт - этанол
Бесцветная жидкость с характерным запахом и жгучим вкусом,
температурой кипения78С. Легче воды. Смешивается с ней в любых отношениях.
Легко воспламеняется, горит слабо светящимся голубоватым пламенем.
Легко воспламеняется, горит слабо светящимся голубоватым пламенем.
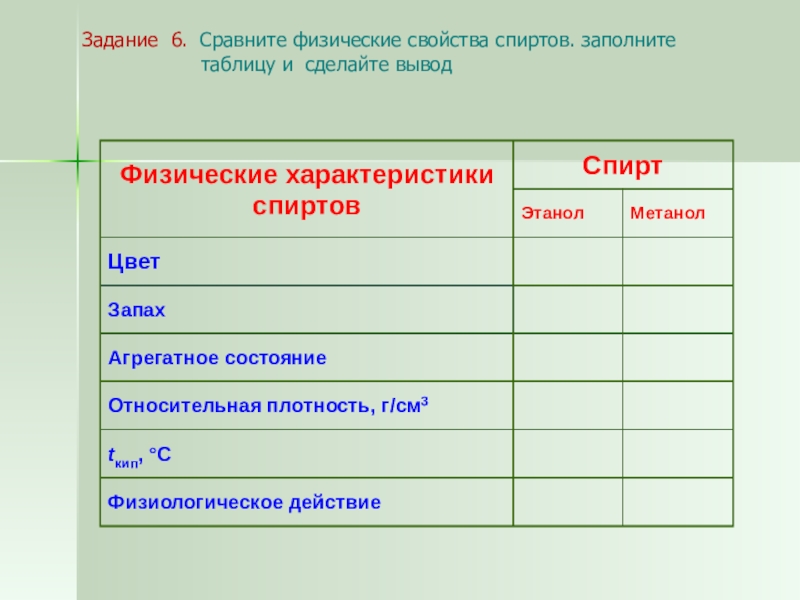
Слайд 21Физические свойства
Задание 5 :
Исследование свойств спиртов (инструкция).
У вас есть
возможность сравнить и дополнить материалом учебника из §35.
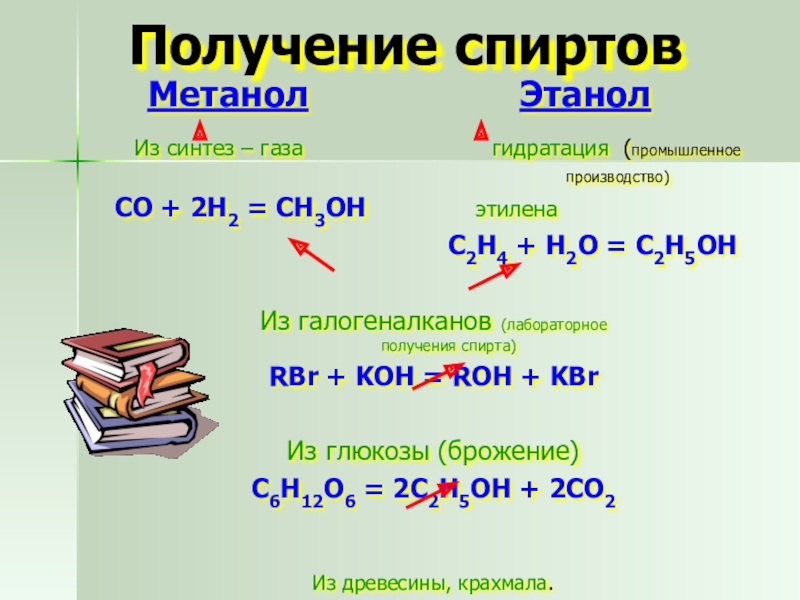
Слайд 26Получение спиртов
Метанол
Этанол
Из синтез – газа гидратация (промышленное
производство)
СО + 2Н2 = СН3ОН этилена
С2Н4 + Н2О = С2Н5ОН
Из галогеналканов (лабораторное получения спирта)
RBr + KOH = ROH + KBr
Из глюкозы (брожение)
C6H12O6 = 2С2Н5ОН + 2CO2
Из древесины, крахмала.
Из синтез – газа гидратация (промышленное
производство)
СО + 2Н2 = СН3ОН этилена
С2Н4 + Н2О = С2Н5ОН
Из галогеналканов (лабораторное получения спирта)
RBr + KOH = ROH + KBr
Из глюкозы (брожение)
C6H12O6 = 2С2Н5ОН + 2CO2
Из древесины, крахмала.
Слайд 27Применение этилового спирта
Производство каучука (резины), исходя из спирта.
Растворитель в лакокрасочной и
химико-фармацевтической промышленности.
Для приготовления настоек и экстрактов, а также многих лекарств.
В медицине для компрессов, обтираний, дезинфекции кожи перед уколом.
Основное сырьё для ликёроводочных и винных производств.
Для приготовления настоек и экстрактов, а также многих лекарств.
В медицине для компрессов, обтираний, дезинфекции кожи перед уколом.
Основное сырьё для ликёроводочных и винных производств.
Слайд 30Вредное воздействие этанола
В начале опьянения страдают структуры коры больших полушарий;
активность центров мозга, управляющих поведением, подавляется: утрачивается разумный контроль над поступками, снижается критическое отношение к себе. И. П. Павлов называл такое состояние «буйством подкорки».
При очень большом содержании алкоголя в крови угнетается активность двигательных центров мозга, главным образом страдает функция мозжечка - человек полностью теряет ориентацию.
При очень большом содержании алкоголя в крови угнетается активность двигательных центров мозга, главным образом страдает функция мозжечка - человек полностью теряет ориентацию.
Слайд 31Вредное воздействие этанола
Изменения структуры мозга, вызванные многолетней алкогольной интоксикацией, почти необратимы,
и даже после длительного воздержания от употребления спиртных напитков они сохраняются. Если же человек не может остановиться, то органические и, следовательно, психические отклонения от нормы идут по нарастающей.
Слайд 32Вредное воздействие этанола
Алкоголь крайне неблагоприятно влияет на сосуды головного мозга. В
начале опьянения они расширяются, кровоток в них замедляется, что приводит к застойным явлениям в головном мозге. Затем, когда в крови помимо алкоголя начинают накапливаться вредные продукты его неполного распада, наступает резкий спазм, сужение сосудов, развиваются такие опасные осложнения, как мозговые инсульты, приводящие к тяжелой инвалидности и даже смерти.
Слайд 33Многоатомный спирт -этиленгликоль
Этиленгликоль — представитель предельных двухатомных спиртов — гликолей.
Название
гликоли получили вследствие сладкого вкуса многих представителей ряда (греч. «гликос» — сладкий).
Этиленгликоль - сиропообразная жидкость сладкого вкуса, без запаха, ядовит. Хорошо смешивается с водой и спиртом, гигроскопичен.
Этиленгликоль - сиропообразная жидкость сладкого вкуса, без запаха, ядовит. Хорошо смешивается с водой и спиртом, гигроскопичен.
Слайд 34Применение этиленгликоля
Важным свойством этиленгликоля является способность понижать температуру замерзания воды, от
чего вещество нашло широкое применения как компонент автомобильных антифризов и незамерзающих жидкостей.
Он применяется для получения лавсана (ценного синтетического волокна).
Он применяется для получения лавсана (ценного синтетического волокна).
Слайд 35Этиленгликоль - яд
Дозы вызывающие смертельное отравление этиленгликолем варьируются в широких
пределах - от 100 до 600 мл. По данным ряда авторов смертельной дозой для человека является 50-150 мл. Смертность при поражении этиленгликолем очень высока и составляет более 60% всех случаев отравления.
Механизм токсического действия этиленгликоля до настоящего времени изучен недостаточно. Этиленгликоль быстро всасывается (в том числе через поры кожи) и в течение нескольких часов циркулирует в крови в неизмененном виде, достигая максимальной концентрации через 2-5 часов. Затем его содержание в крови постепенно снижается, и он фиксируется в тканях.
Механизм токсического действия этиленгликоля до настоящего времени изучен недостаточно. Этиленгликоль быстро всасывается (в том числе через поры кожи) и в течение нескольких часов циркулирует в крови в неизмененном виде, достигая максимальной концентрации через 2-5 часов. Затем его содержание в крови постепенно снижается, и он фиксируется в тканях.
Слайд 36Многоатомный спирт - глицерин
Глицерин – трехатомный предельный спирт. Бесцветная, вязкая, гигроскопичная,
сладкая на вкус жидкость. Смешивается с водой в любых отношениях , хороший растворитель. Реагирует с азотной кислотой с образованием нитроглицерина. С карбоновыми кислотами образует жиры и масла.
Слайд 37Применение глицерина
Применяется в производстве взрывчатых веществ нитроглицерина.
При обработке кожи.
Как компонент
некоторых клеёв.
При производстве пластмасс глицерин используют в качестве пластификатора.
В производстве кондитерских изделий и напитков (как пищевая добавкаE422).
При производстве пластмасс глицерин используют в качестве пластификатора.
В производстве кондитерских изделий и напитков (как пищевая добавкаE422).
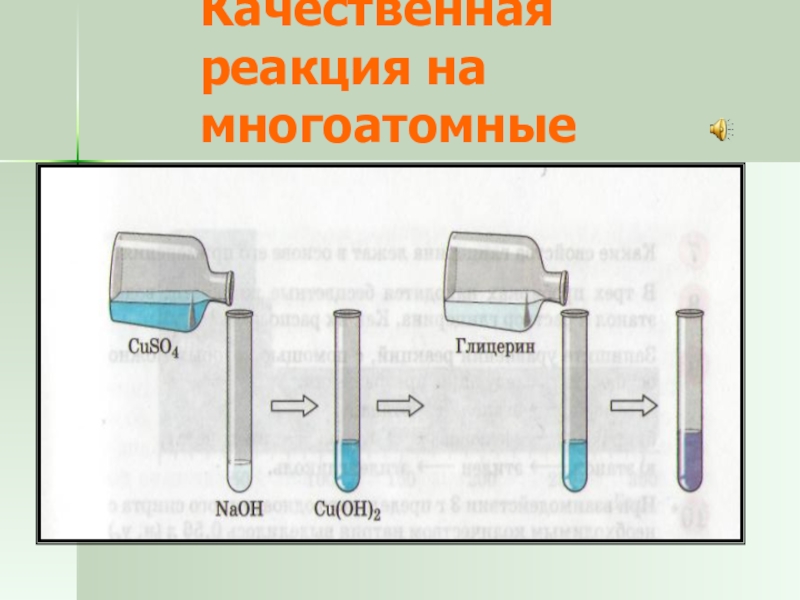
Слайд 39Качественная реакция на многоатомные спирты
Реакцией на многоатомные спирты является их взаимодействие
со свежеполученным осадком гидроксида меди (II), который растворяется с образованием яркого сине-фиолетового раствора.
Слайд 40Рефлексия:
Вино губит …
Если в трезвом состоянии снайпер 10 патронами выбивает
96 очков из 100 возможных, то после принятия рюмки водки – 26.
Производительность труда наборщиков, секретарей – референтов снижается на 25%, а число ошибок увеличивается на 30%.
Производительность труда наборщиков, секретарей – референтов снижается на 25%, а число ошибок увеличивается на 30%.
Слайд 41 «Вино губит телесное здоровье людей, губит умственные способности, губит
благосостояние семей и, что ужаснее всего, губит души людей и их потомство».
Л.Н. Толстой
Л.Н. Толстой
Слайд 56Рефлексия
Разрешили ли вы проблему, поставленную в начале урока?
Как вы можете
использовать полученные знания?
Изменилось ли ваше отношение к проблеме поднятой в фильме?
Изменилось ли ваше отношение к проблеме поднятой в фильме?
Слайд 57Домашнее задание
§ 35.
Эссе
«Вино сообщает каждому, кто пьёт, четыре качества:
сначала павлина, потом обезьяны, затем льва и наконец свиньи». Абу-ль-Фарадж