- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 11 класс по теме : Основные физические законы в химии.
Содержание
- 1. Презентация по химии 11 класс по теме : Основные физические законы в химии.
- 2. Цель: повторить основные законы стехиометрии – закон сохранения
- 3. ПовторимКарточка № 1
- 4. Тест по темам: «Строение атома. Периодический закон и Периодическая система химических элементов Д.И. Менделеева»
- 5. Повторим
- 6. Повторим
- 7. Эталон ответов
- 8. Новая темаДавайте рассмотрим реакции между метаном и
- 9. М.В.Ломоносов в 1748 г. впервые сформулировал, а
- 10. Формулировка закона Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ
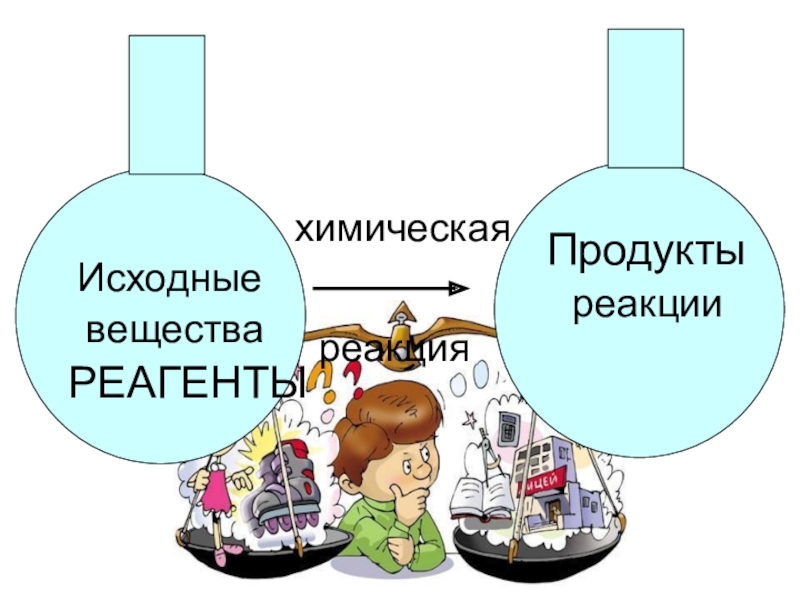
- 11. Исходные веществаРЕАГЕНТЫхимическаяреакцияПродуктыреакции
- 12. Атомы не появляются и не исчезают при химической реакции
- 13. Правила составления химических уравнений 1. В левой
- 14. а) N2 + 3H2 → 2NH3б) 2Al(OH)3
- 15. Новые вещества не получаются из ничего
- 16. Слайд 16
- 17. Слайд 17
- 18. Слайд 18
- 19. Слайд 19
- 20. Соотношение между массой и полной энергией выражает уравнение
- 21. Массы ядер можно измерить с высокой точностью при
- 22. Выводы по уроку:В чем сущность закона сохранения
- 23. Закрепление.Почему масса железной окалины больше массы железа?
- 24. Урок я усвоил на :Я знаюЯ умеюМне было интересноВызвало трудности Подведение итогов . Выставление оценок
- 25. Домашнее задание.Параграф 2, упр 3-4.
- 26. Спасибо за внимание !
- 27. Слайд 27
Слайд 1Урок № 3
Тема: « Основные физические законы в химии :Закон сохранения массы
Закон постоянства состава веществ.
Вещества молекулярного и немолекулярного строения».
Учитель биологии и химии
ГОШ I-III ступеней № 68
Бородина О.В.
Слайд 2
Цель: повторить основные законы стехиометрии – закон сохранения массы
веществ и закон
.
Задачи:
Образовательные:
Углубить знания учащихся о законе сохранения массы веществ, дать краткие
сведения об истории открытия закона и научной деятельности ученых в этой
области, рассмотреть значимость этого закона в химии.
Повторить закон постоянства состава веществ и научить применять для решения
задач.
Развивающие:
Развивать познавательный интерес к предмету.
Создать условия для овладения приемами изучения состава веществ.
Формировать умение проводить поиск, обработку и систематизацию информации.
Воспитательные:
Воспитывать толерантные отношения в группе, классе.
Тип урока: изучение нового материала.
Методы: словесный, наглядный, практический
Слайд 4Тест по темам: «Строение атома. Периодический закон и Периодическая система химических
Слайд 8Новая тема
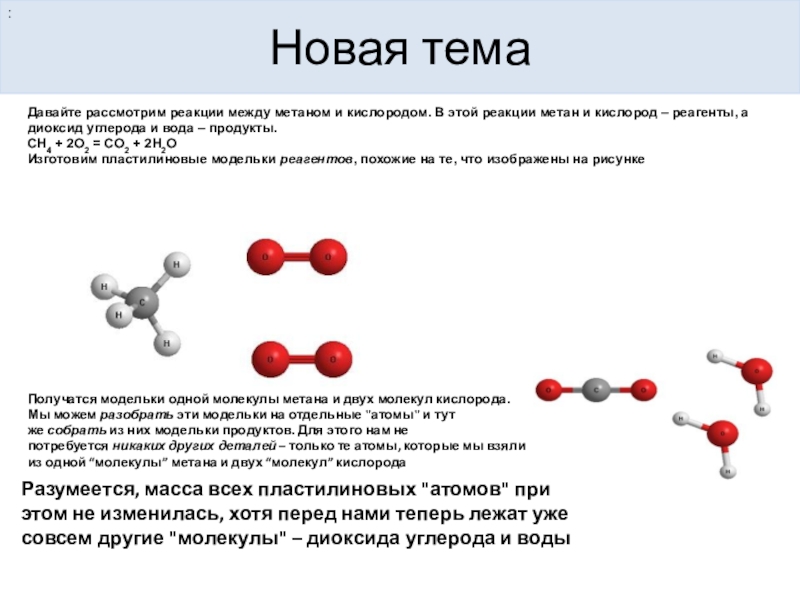
Давайте рассмотрим реакции между метаном и кислородом. В этой реакции
СН4 + 2О2 = СО2 + 2Н2О
Изготовим пластилиновые модельки реагентов, похожие на те, что изображены на рисунке
:
Получатся модельки одной молекулы метана и двух молекул кислорода. Мы можем разобрать эти модельки на отдельные "атомы" и тут же собрать из них модельки продуктов. Для этого нам не потребуется никаких других деталей – только те атомы, которые мы взяли из одной “молекулы” метана и двух “молекул” кислорода
Разумеется, масса всех пластилиновых "атомов" при этом не изменилась, хотя перед нами теперь лежат уже совсем другие "молекулы" – диоксида углерода и воды
Слайд 9М.В.Ломоносов в 1748 г. впервые
сформулировал, а в 1756 г.
экспериментально
сохранения массы веществ
А.Лавуазье в 1789 г
независимо от
Ломоносова к пришел
тем же выводам
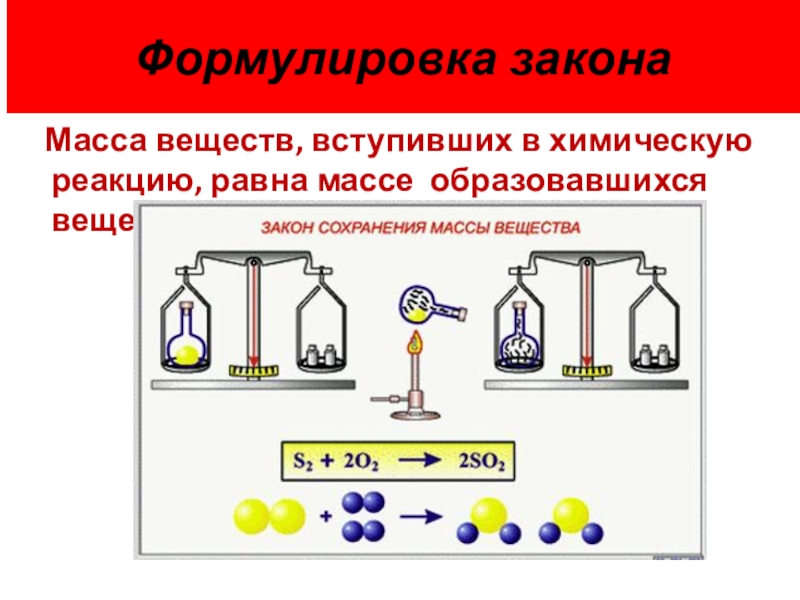
Слайд 10Формулировка закона
Масса веществ, вступивших в химическую реакцию, равна массе
Слайд 13Правила составления химических уравнений
1. В левой части уравнения записать
а) N2 + H2 →
б) Al(OH)3 →
в) Mg + HCl →
г) СaO + HNO3→
Слайд 14а) N2 + 3H2 → 2NH3
б) 2Al(OH)3 → Al2O3 + 3H2O
в)
г) СaO + 2HNO3→ Ca(NO3)2 + H2O
Слайд 15 Новые вещества не получаются из ничего и не могут обратиться
При химических реакциях происходит перегруппировка атомов
Масса веществ, вступивших в реакцию равна массе образовавшихся веществ
При составлении уравнений нужно соблюдать закон сохранения массы веществ
Выводы:
Слайд 20Соотношение между массой и полной энергией выражает уравнение Эйнштейна:
E = mc2
Где
m масса тела
с-скорость света в вакууме
Эйнштейн доказал эквивалентность массы и энергии. Масса и энергия, по Эйнштейну, являются выражением одной и той же сущности, и это дает основание говорить, что энергия = массе.
Слайд 21Массы ядер можно измерить с высокой точностью при помощи масс-спектрометра. Масса атомного ядра всегда оказывается
Слайд 22Выводы по уроку:
В чем сущность закона сохранения массы веществ?
Закон сохранения массы
Какое значение имеет закон сохранения массы веществ?
Слово учителя:
Уравнение реакции отражает материальный баланс вступивших в реакцию веществ (реагентов) и образовавшихся продуктов.
Слайд 23Закрепление.
Почему масса железной окалины больше массы железа? Какие вещества могут входить
Почему масса золы меньше массы сгоревшей древесины? (Углекислый газ, вода испаряются