- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по дисциплине ЕН.03. Химия на тему: Дисперсные системы. Методы получения, свойства
Содержание
- 1. Презентация по дисциплине ЕН.03. Химия на тему: Дисперсные системы. Методы получения, свойства
- 2. Дисперсная система — это система, в которой
- 3. Гомогенная (однородная) дисперсная система это система, в
- 4. Гетерогенная (неоднородная) дисперсная система это система, в
- 5. Степень дисперсности (D) это величина, обратная размеру
- 6. Классификация дисперсных систем.
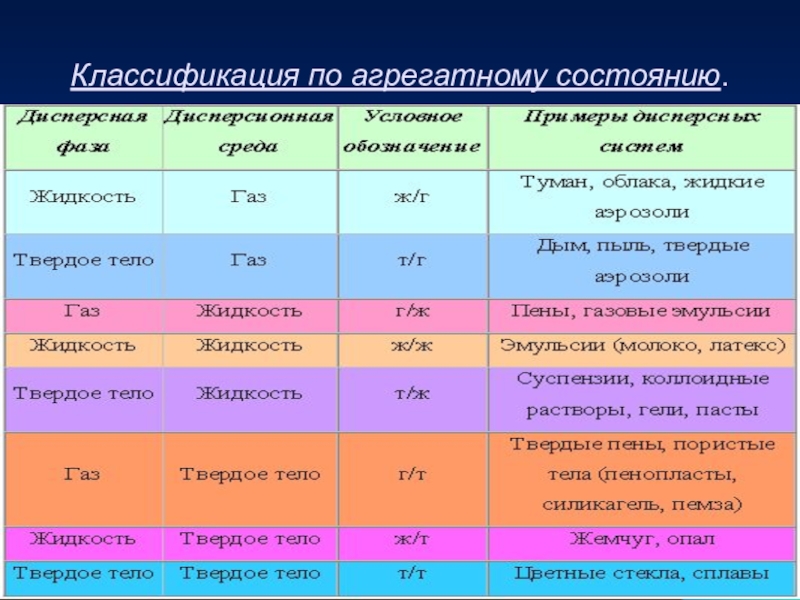
- 7. Классификация по агрегатному состоянию.
- 8. Лиофобные – это системы, в которых слабые
- 9. Коллоидные растворы (золи)Коллоидными растворами называют микрогетерогенные дисперсные
- 10. Условия образования коллоидных растворовмалая растворимость веществ дисперсной
- 11. Методы получения коллоидных растворов (золей)Конденсационные методы.Это методы
- 12. ДИСПЕРГАЦИОННЫЕ МЕТОДЫ: Механическое измельчение Ультразвуковое измельчение Электрическое измельчение Химическое измельчение (пептизация)
- 13. Конденсационный метод физическая конденсация Конденсация из паров замена растворителя Химическая конденсация: различные типы реакций
- 14. Строение коллоидной частицыAgNO3 + КI = AgI
- 15. Слайд 15
- 16. Методы очистки коллоидных растворов.Диализ – это очищение
Дисперсная система — это система, в которой мелкие частицы одной или нескольких веществ равномерно распределены между частицами другого вещества.Дисперсной фазой называют мелкие частицы вещества, которые распределены в системе.Дисперсионной средой называют вещество, в котором распределена дисперсная фаза.
Слайд 2Дисперсная система — это система, в которой мелкие частицы одной или
нескольких веществ равномерно распределены между частицами другого вещества.
Дисперсной фазой называют мелкие частицы вещества, которые распределены в системе.
Дисперсионной средой называют вещество, в котором распределена дисперсная фаза.
Слайд 3Гомогенная (однородная) дисперсная система
это система, в которой между дисперсной фазой
и дисперсионной средой нет поверхности раздела.
К таким системам принадлежат истинные растворы. Размеры молекул, ионов меньше, чем 1·10-9м. Такие системы термодинамически устойчивые и понятие дисперсности к ним не относится.
К таким системам принадлежат истинные растворы. Размеры молекул, ионов меньше, чем 1·10-9м. Такие системы термодинамически устойчивые и понятие дисперсности к ним не относится.
Слайд 4Гетерогенная (неоднородная) дисперсная система
это система, в которой частицы дисперсной фазы
имеют размер больше, чем 1·10-9м и составляют отдельную фазу от дисперсионной среды.
Слайд 5Степень дисперсности (D)
это величина, обратная размеру частицы(d)
D = 1/d
Чем
меньший размер частицы, тем большая дисперсность системы
Слайд 8
Лиофобные – это системы, в которых слабые силы межмолекулярного взаимодействия. К
ним принадлежат лиозоли, аэрозоли, эмульсии, пены. Лиофобные золи – это коллоидные растворы
Лиофильные – это системы, в которых интенсивное взаимодействие между фазой и средой. К ним принадлежат растворы высокомолекулярных соединений
Слайд 9Коллоидные растворы (золи)
Коллоидными растворами называют микрогетерогенные дисперсные системы с частицами размером
от 10-7 до 10-9м. Их характеризует не только наличие поверхности раздела между дисперсной фазой (каждой частицей) и дисперсионной средой (растворителем), но и малая устойчивость; коллоидные растворы не образуются самопроизвольно.
Слайд 10Условия образования коллоидных растворов
малая растворимость веществ дисперсной фазы в дисперсионной среде
соответственная
степень дисперсности вещества (d = 10-7-10-9 м)
наличие стабилизатора, который придает частицам дисперсной фазы одноименный заряд, что предупреждает их объединение (агрегацию).
наличие стабилизатора, который придает частицам дисперсной фазы одноименный заряд, что предупреждает их объединение (агрегацию).
Слайд 11Методы получения коллоидных растворов (золей)
Конденсационные методы.
Это методы получения золей путем укрупнения
микрочастиц
Конденсационные методы разделяют на физические и химические.
Диспергационные методы.
Это методы дробления больших частиц до коллоидной степени дисперсности.
Конденсационные методы разделяют на физические и химические.
Диспергационные методы.
Это методы дробления больших частиц до коллоидной степени дисперсности.
Слайд 12ДИСПЕРГАЦИОННЫЕ МЕТОДЫ:
Механическое измельчение
Ультразвуковое измельчение
Электрическое измельчение
Химическое измельчение (пептизация)
Слайд 13Конденсационный метод
физическая конденсация
Конденсация из паров
замена растворителя
Химическая конденсация:
различные типы реакций
Слайд 14Строение коллоидной частицы
AgNO3 + КI = AgI + KNO3
(mAgI) —агрегат
[(mAgI) nAg+]n+—
ядро
{[(mAgI)nAg+]n+(n-x)NO3-}x+ —гранула
{[(mAgI) nAg+]n+(n-x)NO3-}x+х NO3- - мицелла
{[(mAgI)nAg+]n+(n-x)NO3-}x+ —гранула
{[(mAgI) nAg+]n+(n-x)NO3-}x+х NO3- - мицелла
Слайд 16Методы очистки коллоидных растворов.
Диализ – это очищение коллоидных
растворов через полупроницаемую
мембрану, которая омывается
растворителем.
Схема диализатора
Электродиализ – это процесс очистки
золей от примесей электролитов
в электрическом поле, которое
ускоряет движение ионов.
Схема электродиализатора
Ультрафильтрация – это метод очистки коллоидных растворов путем фильтрования их под давлением через специальные пленки – ультрафильтры.












![Презентация по дисциплине ЕН.03. Химия на тему: Дисперсные системы. Методы получения, свойства Строение коллоидной частицыAgNO3 + КI = AgI + KNO3(mAgI) —агрегат[(mAgI) nAg+]n+— Строение коллоидной частицыAgNO3 + КI = AgI + KNO3(mAgI) —агрегат[(mAgI) nAg+]n+— ядро{[(mAgI)nAg+]n+(n-x)NO3-}x+ —гранула{[(mAgI) nAg+]n+(n-x)NO3-}x+х NO3- - мицелла](/img/thumbs/29e5a2bbf404331a57c7f76e76b6ee77-800x.jpg)







