- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку-семинару Комплексные соединения
Содержание
- 1. Презентация к уроку-семинару Комплексные соединения
- 2. Цель урока: изучение химии комплексных соединенийЗадачи:-закрепить знания
- 3. 1. Центральный атом или ион (чаще -
- 4. Допуск в мир комплексов1.Комплексообразователь2. Лиганд3.А.Вернер4.Координационное число5. Донор6. Акцептор7. Ионная8. Внешняя сфера9. Внутренняя сфера10.Аква, амин
- 5. Первые красители - растения и животныеИндия –
- 6. Андрей Либавий– первый синтетический красительМ.В.Ломоносов – желтая
- 7. 3CoCI2 +2 K3 [Fe (CN)6 ] =
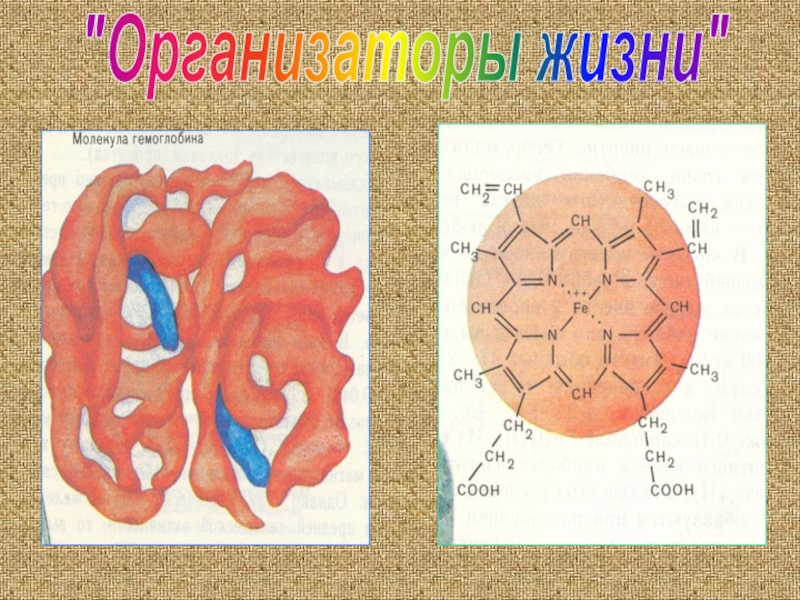
- 8. "Организаторы жизни"
- 9. "Организаторы жизни"
- 10. Na3[AlF6]Ответ: Na+3[Al+3F-6]K[MgCl3]Na[Al(OH)4]Na4[Fe(CN)6]Na3[Al(OH)6][Cu(NH3)4]Cl2Ответ: Na+[Al+3(OH)-4]Ответ: K+[Mg+2Cl-3]Ответ:Na+4[Fe+2(CN)-6]Ответ:Na+3[Al+3(OH)-6]Ответ:[Cu+2(NH3)04]Cl-2«Суха теория без практики»«Рассчитайте степень окисления иона-комплексообразователя»
- 11. «Суха теория без практики»Задания:1. а) Назовите комплексные
- 12. «Суха теория без практики» Гексацианоферрат (II) калияТетрагидроксоцинкат барияХлорид тетрааммин кобальта(II)Гексагидроксоалюминат калия[Zn(H2O)4]SO4 (К4[Fe(CN)6])Na+3[Al+3(OH)-6][Ag (NH3 )2 ]Cl-[Cu(NH3)4]SO4Na3[Fe(CN)6]«Сверим ответы»
- 13. 1.«Многоликий аммиак» -получение гидроксида тетрааммин меди (II)CuCl2+2NH3
- 14. «Пропуск из мира комплексов»«Что не успели, доделаем
- 15. Строение комплексов
- 16. Строение комплексовНазвания некоторых лигандов
Слайд 1Комплексные соединения
урок-семинар
Автор: Тулупова Татьяна Алексеевна
учитель химии высшей
квалификационной категории
ГБОУ СОШ
м.р. Волжский Самарской области
Слайд 2Цель урока: изучение химии комплексных соединений
Задачи:
-закрепить знания учащихся о строении и
познакомить со способами получения и важнейшими областями применения этих веществ;
-раскрыть на примере комплексных соединений идеи многообразия, взаимосвязи органических и неорганических веществ, их роли в окружающем мире;
-развивать у учащихся умение самостоятельно добывать знания и уметь ориентироваться в сложном многообразии окружающего мира
Комплексные соединения
Слайд 31. Центральный атом или ион (чаще - d металл)
2.Молекула или ион,
3.Автор координационной теории
4.Количество лигандов, входящих в состав комплексного иона
5.Атом или ион, имеющий свободные пары электронов
6. Атом или ион, имеющий свободные орбитали
7.Вид химической связи между внешней и внутренней сферами комплекса
8.Ионы, связанные с комплексным ионом ионной связью
9.Ион, состоящий из d- металла и лигандов
10.Названия лигандов: H2O, NH3
«Допуск в мир комплексов»
диктант
Слайд 4Допуск в мир комплексов
1.Комплексообразователь
2. Лиганд
3.А.Вернер
4.Координационное число
5. Донор
6. Акцептор
7. Ионная
8. Внешняя сфера
9.
10.Аква, амин
Слайд 5Первые красители - растения и животные
Индия – индиго
Средиземное море –
Восток – крокус –шафран
Индия – марена - крапп
Слайд 6
Андрей Либавий–
первый синтетический краситель
М.В.Ломоносов –
желтая кровяная соль
Турнбуль – «турнбулева
П.Суханов и И.Беляев-
патент на красители
Первые синтезы
Слайд 73CoCI2 +2 K3 [Fe (CN)6 ] = Co 3 [Fe(CN )6]2+6
красный
3NiCI2 + 2K3 [Fe (CN)6 ] = Ni 3 [Fe(CN )6]2++6KCI
желтый
3 FeCI 2 +2K3 [Fe (CN)6 ] = Fe 3 [Fe(CN)6 ]2+ 6KCI
темно – синий «турнбулева синь»
2CoCI2 + K4 [Fe (CN)6] = Co 2 [Fe(CN )6] +4 KCI
коричневый
2NiCI2 + K4 [Fe (CN)6] = Ni 2 [Fe(CN )6]+4 KCI
зеленый
4FeCI 3 +3K4[Fe (CN)6 ] = Fe 4 [Fe(CN)6]3 +12 KCI
темно – синий «берлинская лазурь»
Комплексы - красители
Слайд 10Na3[AlF6]
Ответ: Na+3[Al+3F-6]
K[MgCl3]
Na[Al(OH)4]
Na4[Fe(CN)6]
Na3[Al(OH)6]
[Cu(NH3)4]Cl2
Ответ: Na+[Al+3(OH)-4]
Ответ: K+[Mg+2Cl-3]
Ответ:Na+4[Fe+2(CN)-6]
Ответ:Na+3[Al+3(OH)-6]
Ответ:[Cu+2(NH3)04]Cl-2
«Суха теория без практики»
«Рассчитайте степень окисления иона-комплексообразователя»
Слайд 11«Суха теория без практики»
Задания:
1. а) Назовите комплексные соединения:
а) Na4[Fe(CN)6]; б)
2.Составьте формулы комплексов по частям и назовите
(при затруднении смотри в справочник - опорный конспект):
а)Ag+, NH3 , Cl- , к.ч=2 ; б) Zn2+, H2O, (SO4)2-, к.ч=4; в) K+, (CN)-, Fe3+,к.ч =6.
3.Составь формулу комплекса по названию:
а) гексацианоферрат (II) калия; б) гексагидроксоалюминат натрия;
в) сульфат тетрааммин меди (II).
4.Выведи формулу комплекса, которую в страшном секрете хранил
мастер Турнбуль - решение задачи на вывод молекулярной формулы
вещества по следующим данным: М=329г/моль; W(K)=35,56%;
W(Fe)=17,02%; W(С)=21, 88%; остальное- азот. (К4[Fe(CN)6])
Слайд 12«Суха теория без практики»
Гексацианоферрат (II) калия
Тетрагидроксоцинкат бария
Хлорид тетрааммин кобальта(II)
Гексагидроксоалюминат калия
[Zn(H2O)4]SO4
Na+3[Al+3(OH)-6]
[Ag (NH3 )2 ]Cl-
[Cu(NH3)4]SO4
Na3[Fe(CN)6]
«Сверим ответы»
Слайд 131.«Многоликий аммиак» -
получение гидроксида тетрааммин меди (II)
CuCl2+2NH3 +2H2O = Cu(OH)2↓+NH4Cl
Cu(OH)2 +
«Пробуем сами творить чудеса»
Лабораторная работа
2.«Сами синтезируем, сами красим» -
получение турнбулевой сини и окрашивание ткани
полученным красителем
3 FeCI2 +2K3(Fe(CN)6 )= Fe3[(Fe(CN)6)2] + 6KCI
Слайд 14«Пропуск из мира комплексов»
«Что не успели, доделаем дома »
Задание уровня А:
2. Задания уровня В: Na3AlF6- криолит, вещество, применяемое
при выплавке алюминия для понижения температуры плавки.
Назовите комплекс по правилам номенклатуры и разберите
по составу. Дайте характеристику комплекса.
3.Задание уровня С: CuSO4 5H2O – медный купорос, ядохимикат
для защиты садов и огородов от вредителей. Зная, что к.ч. ионов
меди равно 4, напишите формулу этого комплексного соединения
и назовите его по правилам номенклатуры. Успеха!






![Презентация к уроку-семинару Комплексные соединения 3CoCI2 +2 K3 [Fe (CN)6 ] = Co 3 [Fe(CN )6]2+6 3CoCI2 +2 K3 [Fe (CN)6 ] = Co 3 [Fe(CN )6]2+6 KCI](/img/tmb/4/311464/d6bed5a076211f0b17175c1a3b92bfb4-800x.jpg)

![Презентация к уроку-семинару Комплексные соединения Na3[AlF6]Ответ: Na+3[Al+3F-6]K[MgCl3]Na[Al(OH)4]Na4[Fe(CN)6]Na3[Al(OH)6][Cu(NH3)4]Cl2Ответ: Na+[Al+3(OH)-4]Ответ: K+[Mg+2Cl-3]Ответ:Na+4[Fe+2(CN)-6]Ответ:Na+3[Al+3(OH)-6]Ответ:[Cu+2(NH3)04]Cl-2«Суха теория без практики»«Рассчитайте степень окисления иона-комплексообразователя» Na3[AlF6]Ответ: Na+3[Al+3F-6]K[MgCl3]Na[Al(OH)4]Na4[Fe(CN)6]Na3[Al(OH)6][Cu(NH3)4]Cl2Ответ: Na+[Al+3(OH)-4]Ответ: K+[Mg+2Cl-3]Ответ:Na+4[Fe+2(CN)-6]Ответ:Na+3[Al+3(OH)-6]Ответ:[Cu+2(NH3)04]Cl-2«Суха теория без практики»«Рассчитайте степень окисления иона-комплексообразователя»](/img/tmb/4/311464/bf148c7c2f49d281485c7aa21bda81c7-800x.jpg)
![Презентация к уроку-семинару Комплексные соединения «Суха теория без практики»Задания:1. а) Назовите комплексные соединения: а) Na4[Fe(CN)6]; б) «Суха теория без практики»Задания:1. а) Назовите комплексные соединения: а) Na4[Fe(CN)6]; б) Ba[Zn(OH)4]; в) [Co(NH3)4]Cl2 ; г)К[Al(OH)6]2.Составьте формулы](/img/thumbs/12c4cd0f2db8cfe0d8b3e71faff4c18c-800x.jpg)
![Презентация к уроку-семинару Комплексные соединения «Суха теория без практики» Гексацианоферрат (II) калияТетрагидроксоцинкат барияХлорид тетрааммин кобальта(II)Гексагидроксоалюминат калия[Zn(H2O)4]SO4 (К4[Fe(CN)6])Na+3[Al+3(OH)-6][Ag (NH3 )2 ]Cl-[Cu(NH3)4]SO4Na3[Fe(CN)6]«Сверим ответы» «Суха теория без практики» Гексацианоферрат (II) калияТетрагидроксоцинкат барияХлорид тетрааммин кобальта(II)Гексагидроксоалюминат калия[Zn(H2O)4]SO4 (К4[Fe(CN)6])Na+3[Al+3(OH)-6][Ag (NH3 )2 ]Cl-[Cu(NH3)4]SO4Na3[Fe(CN)6]«Сверим ответы»](/img/tmb/4/311464/f2745c0c352b3df2f5654d87eeb42fd5-800x.jpg)
2«Пробуем сами творить чудеса»Лабораторная](/img/thumbs/1f751eab60f502156f94b8c9403d531d-800x.jpg)
![Презентация к уроку-семинару Комплексные соединения «Пропуск из мира комплексов»«Что не успели, доделаем дома »Задание уровня А: «Пропуск из мира комплексов»«Что не успели, доделаем дома »Задание уровня А: разберите комплекс Na3[Cr(OH)6] по составу и](/img/tmb/4/311464/93795d023a2e0d180442cbd5e01c1ada-800x.jpg)







