№ 188 г. Новосибирска
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку по химии Алкены, 10 класс
Содержание
- 1. Презентация к уроку по химии Алкены, 10 класс
- 2. Алкены – непредельные углеводороды, содержащие в молекуле
- 3. Физические свойства алкеновТемпературы плавления и кипения алкенов
- 4. Гомологический ряд этен (этилен) C2H4пропен C3H6бутен C4H8пентен C5H10гексен C6H12гептен C7H14октен C8H16нонен C9H18децен C10H20
- 5. Номенклатура алкеновВыбрать самую длинную углеродную цепьПронумеровать углероды
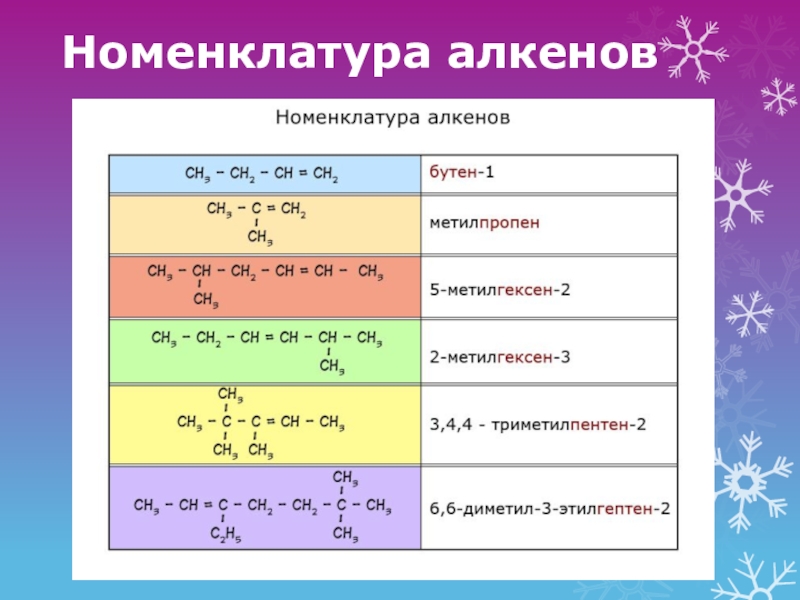
- 6. Номенклатура алкенов
- 7. Изомерия алкенов 1) Изомерия углеродного скелета
- 8. Получение алкенов 1) Основным промышленным источником получения
- 9. Получение алкенов 4) Дегидрогалогенирование (отщепление HHal) из
- 10. Химические свойства1. Присоединение галогенов, галогеноводородов происходит по
- 11. Применение алкеновАлкены широко используются в химической промышленности
- 12. Контроль знаний
Алкены – непредельные углеводороды, содержащие в молекуле кроме одинарных связей, одну двойную углерод - углеродную связь.Общая формула: CnH2n., где n = 2,3 ….Особенности строения:- незамкнутая цепочка атомов углерода- одна С=С связь
Слайд 1Алкены
Выполнил учитель химии
высшей квалификационной категории
Зайцева Наталья Александровна
МБОУ СОШ
Слайд 2Алкены – непредельные углеводороды, содержащие в молекуле кроме одинарных связей, одну
двойную углерод - углеродную связь.
Общая формула:
CnH2n., где n = 2,3 ….
Особенности строения:
- незамкнутая цепочка атомов углерода
- одна С=С связь
Слайд 3Физические свойства алкенов
Температуры плавления и кипения алкенов увеличиваются с молекулярной массой
и длиной главной углеродной цепи.
При нормальных условиях алкены
с C2H4 до C4H8 — газы;
с C5H10 до C17H34 — жидкости,
после C18H36 — твёрдые тела.
Алкены не растворяются в воде, но хорошо растворяются в органических растворителях
При нормальных условиях алкены
с C2H4 до C4H8 — газы;
с C5H10 до C17H34 — жидкости,
после C18H36 — твёрдые тела.
Алкены не растворяются в воде, но хорошо растворяются в органических растворителях
Слайд 4Гомологический ряд
этен (этилен) C2H4
пропен C3H6
бутен C4H8
пентен C5H10
гексен C6H12
гептен C7H14
октен C8H16
нонен C9H18
децен C10H20
Слайд 5Номенклатура алкенов
Выбрать самую длинную углеродную цепь
Пронумеровать углероды с того конца, где
ближе расположен двойная связь. Если двойная связь расположена по середине, то нумерация начинается с того конца где ближе расположен радикал
3. Назвать радикал указав место расположения радикала
(название радикала образуется от названия соответствующего алкана с заменой суффикса – ан на суффикс – ил; если группы повторяются, то перечисляют цифры, указывающие их положение, а число одинаковых групп указывают приставками ди-, три-, тетра-. Если группы неодинаковые, то их названия перечисляются в алфавитном порядке)
4. Назвать длинную углеродную цепь
5. Указать место расположения двойной связи в конце названия алкена
3. Назвать радикал указав место расположения радикала
(название радикала образуется от названия соответствующего алкана с заменой суффикса – ан на суффикс – ил; если группы повторяются, то перечисляют цифры, указывающие их положение, а число одинаковых групп указывают приставками ди-, три-, тетра-. Если группы неодинаковые, то их названия перечисляются в алфавитном порядке)
4. Назвать длинную углеродную цепь
5. Указать место расположения двойной связи в конце названия алкена
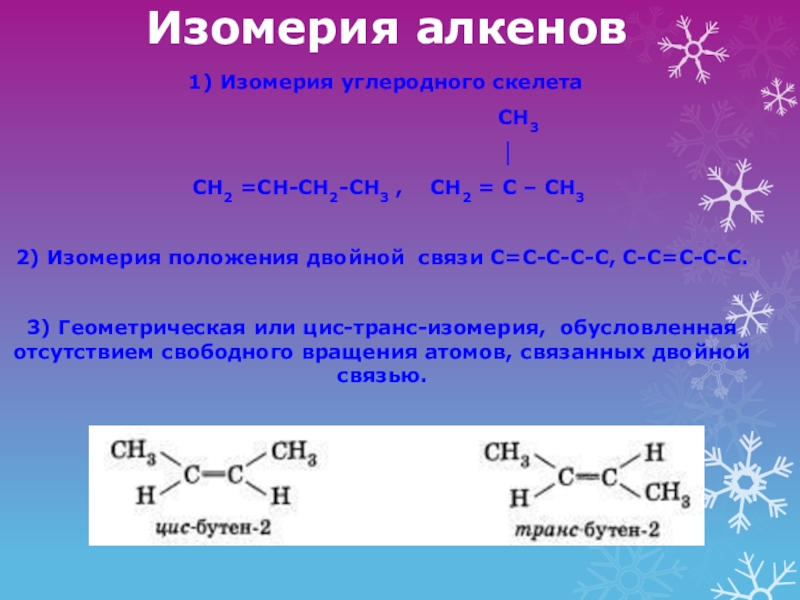
Слайд 7Изомерия алкенов
1) Изомерия углеродного скелета
СН3
│
СН2 =СН-СН2-СН3 , СН2 = С – СН3
2) Изомерия положения двойной связи С=С-С-С-С, С-С=С-С-С.
3) Геометрическая или цис-транс-изомерия, обусловленная отсутствием свободного вращения атомов, связанных двойной связью.
Слайд 8Получение алкенов
1) Основным промышленным источником получения первых четырех членов ряда
алкенов являются газы крекинга и пиролиза нефтепродуктов, а также газы коксования угля (этилен, пропилен).
2)Дегидрогенизация алканов при повышенной температуре с катализатором.
300°C, Cr2O3
CH3–CH2–CH2–CH3 → CH2=CH–CH2–CH3(бутен-1) + H2
CH3–CH=CH–CH3(бутен-2) + H2
3) Дегидратация (отщепление воды) спиртов при нагревании с водоотнимающими средствами (концентрированная серная или фосфорная кислоты) или при пропускании паров спирта над катализатором (окись алюминия). t°,Al2O3
CH3–CH2–OH(этанол) → CH2=CH2 + H2O
2)Дегидрогенизация алканов при повышенной температуре с катализатором.
300°C, Cr2O3
CH3–CH2–CH2–CH3 → CH2=CH–CH2–CH3(бутен-1) + H2
CH3–CH=CH–CH3(бутен-2) + H2
3) Дегидратация (отщепление воды) спиртов при нагревании с водоотнимающими средствами (концентрированная серная или фосфорная кислоты) или при пропускании паров спирта над катализатором (окись алюминия). t°,Al2O3
CH3–CH2–OH(этанол) → CH2=CH2 + H2O
Слайд 9Получение алкенов
4) Дегидрогалогенирование (отщепление HHal) из галогенопроизводных при действии спиртового
раствора щелочи (оответствует правилу Зайцева):
CH3–CH–CH2–CH3 + NaOH(спирт p-p) → CH3–CH=CH– CH3 + NaBr + H2O
|
Br
5) Дегалогенирование (отщепление двух атомов галогена от соседних атомов углерода) при нагревании дигалогенидов с активными металлами:
CH2–CH –CH3 + Mg → CH2=CH–CH3 + MgBr2
| |
Br Br
CH3–CH–CH2–CH3 + NaOH(спирт p-p) → CH3–CH=CH– CH3 + NaBr + H2O
|
Br
5) Дегалогенирование (отщепление двух атомов галогена от соседних атомов углерода) при нагревании дигалогенидов с активными металлами:
CH2–CH –CH3 + Mg → CH2=CH–CH3 + MgBr2
| |
Br Br
Слайд 10Химические свойства
1. Присоединение галогенов, галогеноводородов происходит по правилу Марковникова (вещества, содержащие
водород присоединяются к непредельным углеводородам, таким образом, что атом водорода становится к гидрогенизированному атому углерода, а остаток молекулы к наименее гидрогнизированному атому углерода.
CH3- CH = CH2 + HBr → CH3- CHBr - CH3
CH3- CH = CH2 + Br2 (Br-Br) → CH3- CHBr - CH2 Br
CH2 = CH2 + H2.→ CH3 - CH3
2. Горение: CnH2n+ O2 → CO2 + H2O
3. Полимеризация: происходит соединение большого количества молекул алкенов в одну цепочку с разрывом двойных связей:
CH2 = CH2 + CH2 = CH2 + CH2 = CH2 + CH2 = CH2 …..→ - CH2 - CH2 -CH2 -CH2 - CH2 -CH2 - CH2 -CH2-
4. Присоединение воды с образованием спирта:
CH2 = CH2 + H2O.→ CH3 - CH2 - OH
5 Отщепление: дегидрирование (отщепление двух атомов водорода):
C2H4 → C2H2 + H2
CH3- CH = CH2 + HBr → CH3- CHBr - CH3
CH3- CH = CH2 + Br2 (Br-Br) → CH3- CHBr - CH2 Br
CH2 = CH2 + H2.→ CH3 - CH3
2. Горение: CnH2n+ O2 → CO2 + H2O
3. Полимеризация: происходит соединение большого количества молекул алкенов в одну цепочку с разрывом двойных связей:
CH2 = CH2 + CH2 = CH2 + CH2 = CH2 + CH2 = CH2 …..→ - CH2 - CH2 -CH2 -CH2 - CH2 -CH2 - CH2 -CH2-
4. Присоединение воды с образованием спирта:
CH2 = CH2 + H2O.→ CH3 - CH2 - OH
5 Отщепление: дегидрирование (отщепление двух атомов водорода):
C2H4 → C2H2 + H2
Слайд 11Применение алкенов
Алкены широко используются в химической промышленности как сырье для получения
разнообразных органических веществ и материалов.
Этен является исходным веществом для производства этанола, этиленгликоля, эпоксидов, дихлорэтана. Большое количество этена перерабатывается в полиэтилен, который используется для изготовления упаковочной пленки, посуды, труб, электроизоляционных материалов.
Из пропена получают глицерин, ацетон, изопропанол, растворители. Полимеризацией пропена получают полипропилен, который по многим показателям превосходит полиэтилен: имеет более высокую температуру плавления, химическую устойчивость.
В настоящее время из полимеров — аналогов полиэтилена производят волокна, обладающие уникальными свойствами. Так, например, волокно из полипропилена прочнее всех известных синтетических волокон.
Материалы, изготовленные из этих волокон, являются перспективными и находят все большее применение в разных областях человеческой деятельности.
Этен является исходным веществом для производства этанола, этиленгликоля, эпоксидов, дихлорэтана. Большое количество этена перерабатывается в полиэтилен, который используется для изготовления упаковочной пленки, посуды, труб, электроизоляционных материалов.
Из пропена получают глицерин, ацетон, изопропанол, растворители. Полимеризацией пропена получают полипропилен, который по многим показателям превосходит полиэтилен: имеет более высокую температуру плавления, химическую устойчивость.
В настоящее время из полимеров — аналогов полиэтилена производят волокна, обладающие уникальными свойствами. Так, например, волокно из полипропилена прочнее всех известных синтетических волокон.
Материалы, изготовленные из этих волокон, являются перспективными и находят все большее применение в разных областях человеческой деятельности.