- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку Кислоты 8 класс
Содержание
- 1. Презентация к уроку Кислоты 8 класс
- 2. Выполните задания: Из предложенного перечня веществ
- 3. K2O , Fe(OH)2, CO2 , H2SO4 , NaOH, Al2O3, Cu(OH)2, HCl, N2O5.
- 4. Тема урока:Кислоты
- 5. Слайд 5
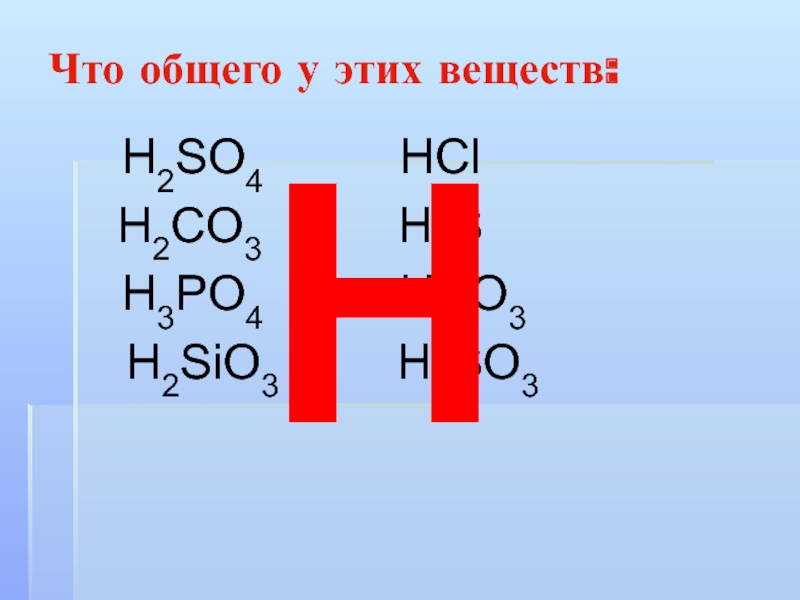
- 6. Что общего у этих веществ: Н2SO4
- 7. Что такое кислоты? Сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка
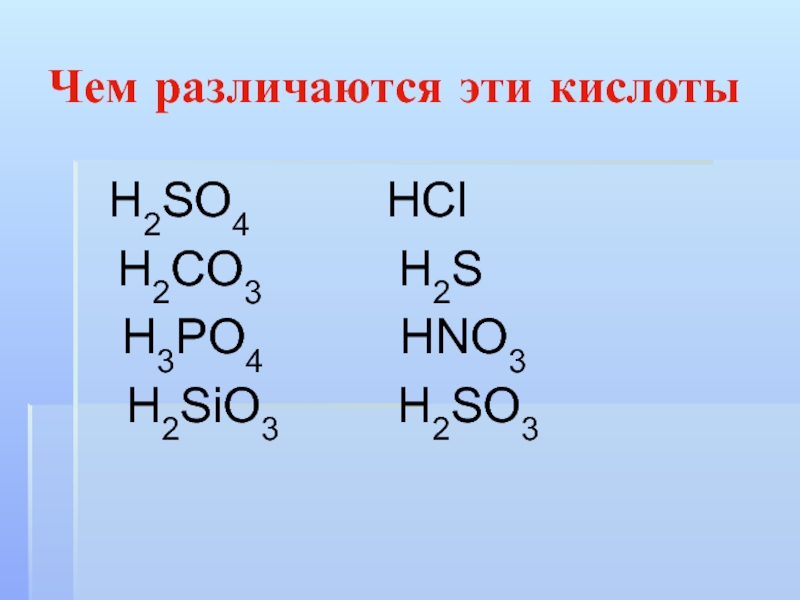
- 8. Чем различаются эти кислоты Н2SO4
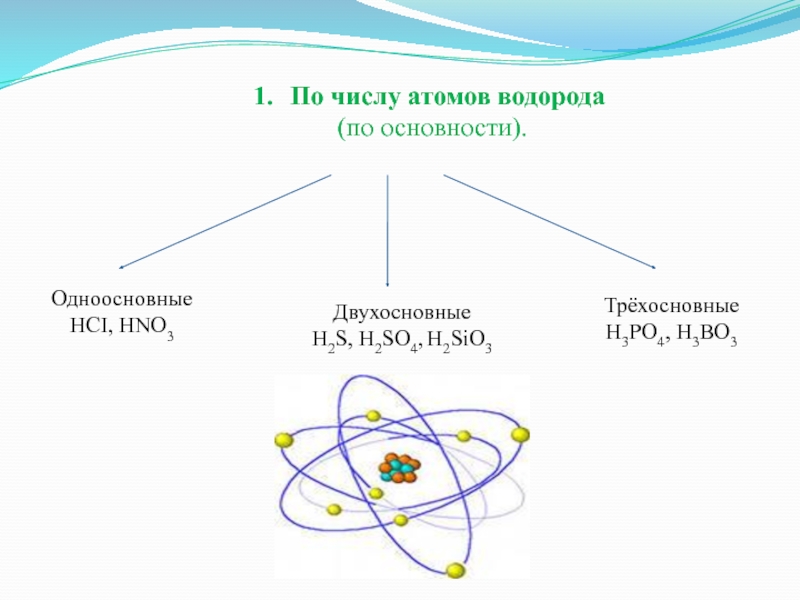
- 9. По числу атомов водорода(по основности).ОдноосновныеHCI, HNO3ТрёхосновныеH3PO4, H3BO3ДвухосновныеH2S, H2SO4, H2SiO3
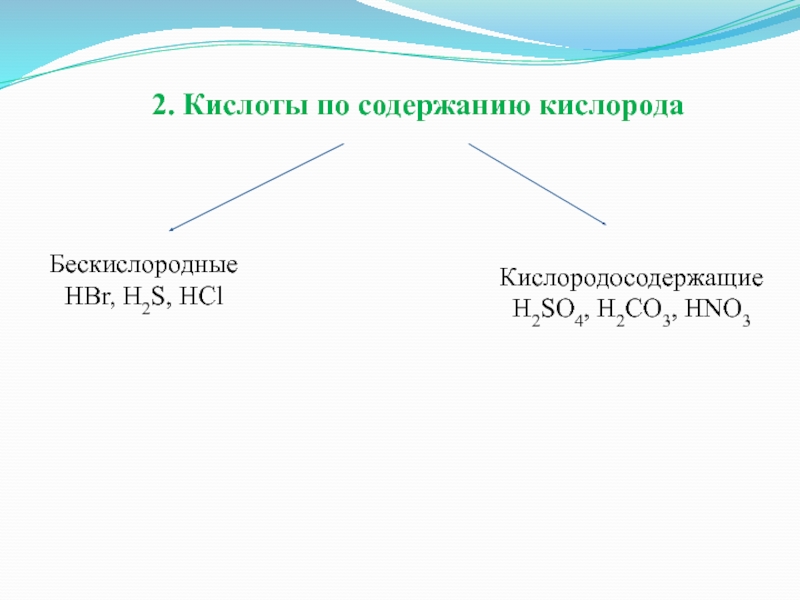
- 10. 2. Кислоты по содержанию кислородаБескислородныеHBr, H2S, HClКислородосодержащиеH2SO4, H2CO3, HNO3
- 11. 3. Растворимость кислот.Обратите внимание на таблицу растворимости
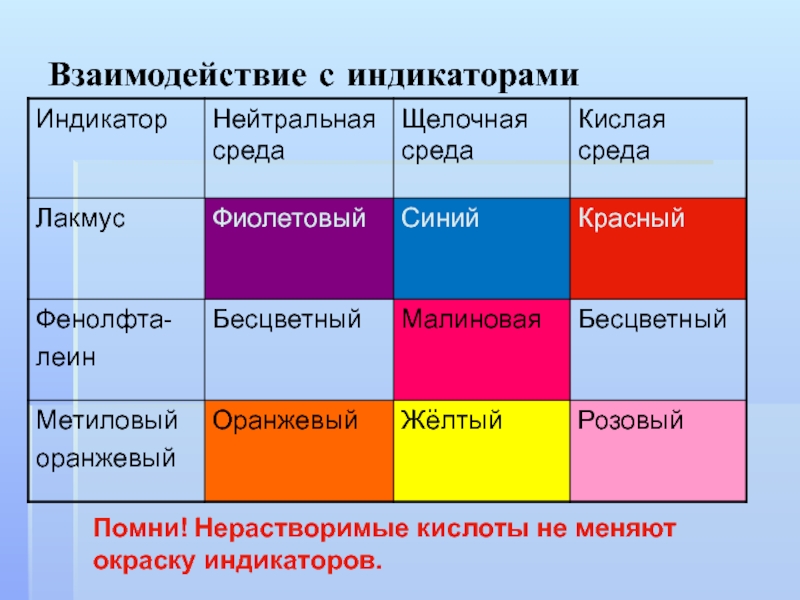
- 12. Взаимодействие с индикаторамиПомни! Нерастворимые кислоты не меняют окраску индикаторов.
- 13. Задание 1 Используя таблицу растворимости кислот, оснований
- 14. Задание 2 «Третий лишний»: В
- 15. Домашняя работа 1. П. 20,
- 16. Подведём итог урока:Что нового вы узнали на
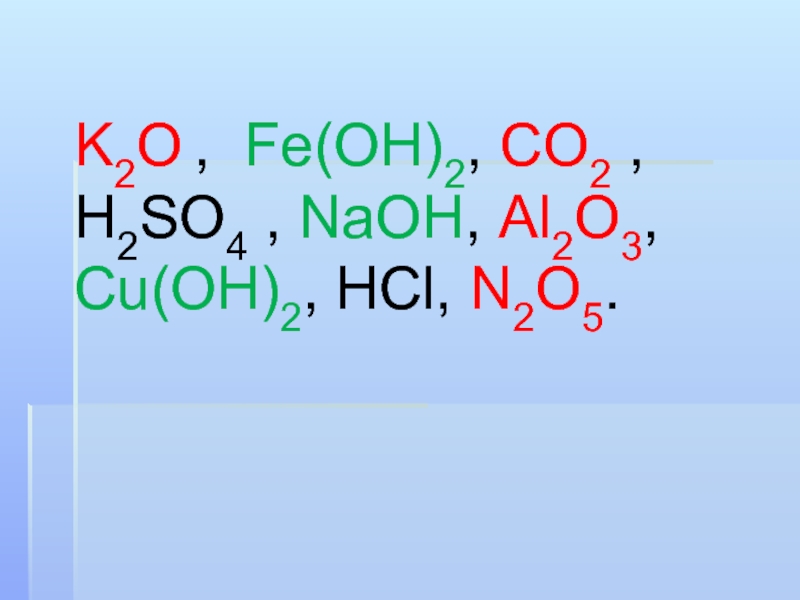
Выполните задания: Из предложенного перечня веществ подчеркните отдельно формулы оксидов и оснований, в соответствии с известной вам классификацией, и дайте им названия: K2O , Fe(OH)2, CO2 , H2SO4 , NaOH, Al2O3, Cu(OH)2, HCl, N2O5.
Слайд 2Выполните задания:
Из предложенного перечня веществ подчеркните отдельно формулы оксидов и
оснований, в соответствии с известной вам классификацией, и дайте им названия:
K2O , Fe(OH)2, CO2 , H2SO4 , NaOH, Al2O3, Cu(OH)2, HCl, N2O5.
K2O , Fe(OH)2, CO2 , H2SO4 , NaOH, Al2O3, Cu(OH)2, HCl, N2O5.
Слайд 5 ЗАДАЧИ УРОКА:
сформировать понятие
о кислотах;
уяснить их состав, номенклатуру,
рассмотреть их классификацию по разным признакам;
- узнать, как действуют индикаторы на кислоты;
- более подробно познакомиться с отдельными представителями кислот,
- узнать роль кислот в народном хозяйстве и в быту
уяснить их состав, номенклатуру,
рассмотреть их классификацию по разным признакам;
- узнать, как действуют индикаторы на кислоты;
- более подробно познакомиться с отдельными представителями кислот,
- узнать роль кислот в народном хозяйстве и в быту
Слайд 7Что такое кислоты?
Сложные вещества, молекулы которых состоят из атомов водорода
и кислотного остатка
Слайд 9По числу атомов водорода
(по основности).
Одноосновные
HCI, HNO3
Трёхосновные
H3PO4, H3BO3
Двухосновные
H2S, H2SO4, H2SiO3
Слайд 102. Кислоты по содержанию кислорода
Бескислородные
HBr, H2S, HCl
Кислородосодержащие
H2SO4, H2CO3, HNO3
Слайд 113. Растворимость кислот.
Обратите внимание на таблицу растворимости кислот (в учебнике). Какой
вывод вы можете сделать? (Единственная нерастворимая кислота – кремниевая H2SO3)
Слайд 13Задание 1
Используя таблицу растворимости кислот, оснований и солей в воде,
составьте формулы разных кислот, дайте им названия, определите тип химической связи.
Н, Н2, Н3 , S, NО2, РО4, СI, SО3
Н, Н2, Н3 , S, NО2, РО4, СI, SО3
Слайд 14Задание 2
«Третий лишний»:
В каждой строчке найти лишнюю формулу:
Н2S, Н2 SО4 , Н2SО3,
Н2СО3, Н3 РО4, Н2 SО4
Н2СО3, Н3 РО4, Н2 SО4
Слайд 15Домашняя работа
1. П. 20, упр. №3, стр. 107
2. Задача №4, стр.107
3. Задание по выбору:
- Подготовить сообщение :
1. «Кислотные дожди»
2. «Кислоты в природе и их применение в быту»
- Составить кроссворд по теме «Кислоты»
3. Задание по выбору:
- Подготовить сообщение :
1. «Кислотные дожди»
2. «Кислоты в природе и их применение в быту»
- Составить кроссворд по теме «Кислоты»
Слайд 16Подведём итог урока:
Что нового вы узнали на уроке?
Что было самым
сложным на уроке и почему?
Как вы считаете, где могут пригодиться вам новые знания?
Оцените, насколько вам удалось достичь поставленной цели.
Как вы считаете, где могут пригодиться вам новые знания?
Оцените, насколько вам удалось достичь поставленной цели.