- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии в 9 классе по теме Водород
Содержание
- 1. Презентация к уроку химии в 9 классе по теме Водород
- 2. ЦЕЛЬ УРОКА Изучить водород, как химический элемент и как простое вещество
- 3. План урока:Положение в периодической системе, строение атомаНахождение в природе, получениеСвойства водородаПрименениеН 1s1водород
- 4. 1. Положение в периодической системе химических элементов
- 5. Почему водород является элементом главной подгруппы?Первой группы:На
- 6. 2. Нахождение в природе:Нахождение в природеВ водеВо
- 7. Лабораторный способ получения водорода
- 8. Получение водорода в лаборатории1. Zn + 2HCI
- 9. Промышленный способ получения водорода 1. Конверсией водяных
- 10. Водород простое веществоМолекулярная формула: Химическая связь: Схема
- 11. 3. Свойства водородаФизические:Агрегатное состояние:Цвет:Запах:Легче или тяжелее воздуха?Растворимость
- 12. 3. Свойства водородафизические:химические:1)2Н2 + О2 = 2Н2О2)Н2
- 13. 4. Применение водорода
- 14. Водородная бомба Оружие большой разрушительной
- 15. 4. Применение водорода Водород используется
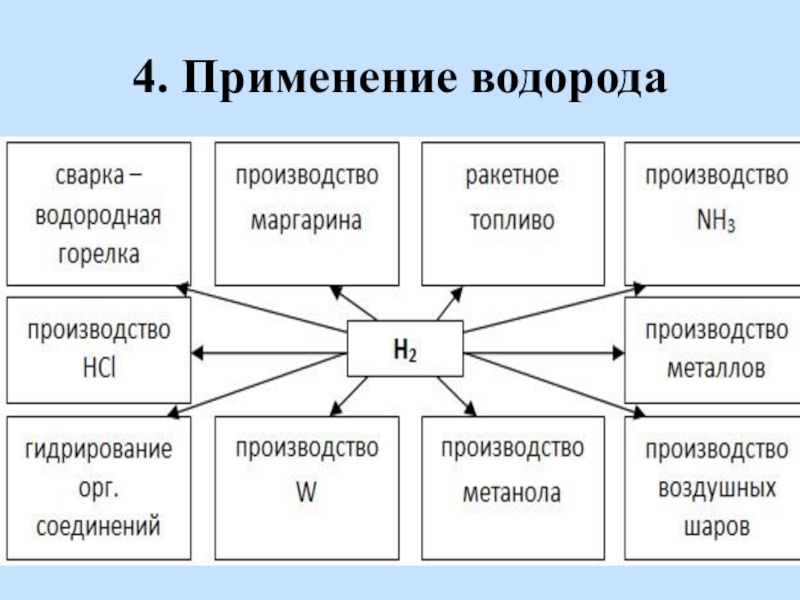
- 16. 4. Применение водорода
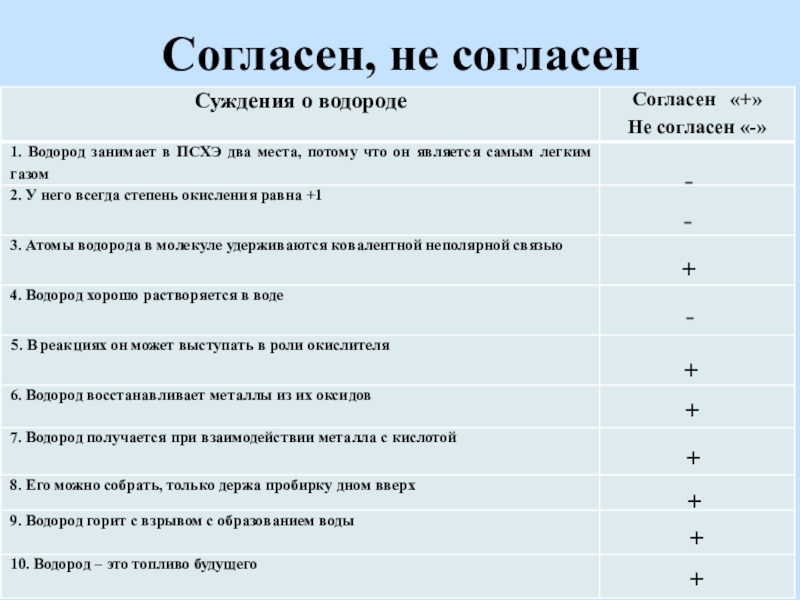
- 17. Согласен, не согласен+---++++++
- 18. Домашнее задание§17 изучить, подготовится к тесту, Задания
Слайд 3План урока:
Положение в периодической системе, строение атома
Нахождение в природе, получение
Свойства водорода
Применение
Н
водород
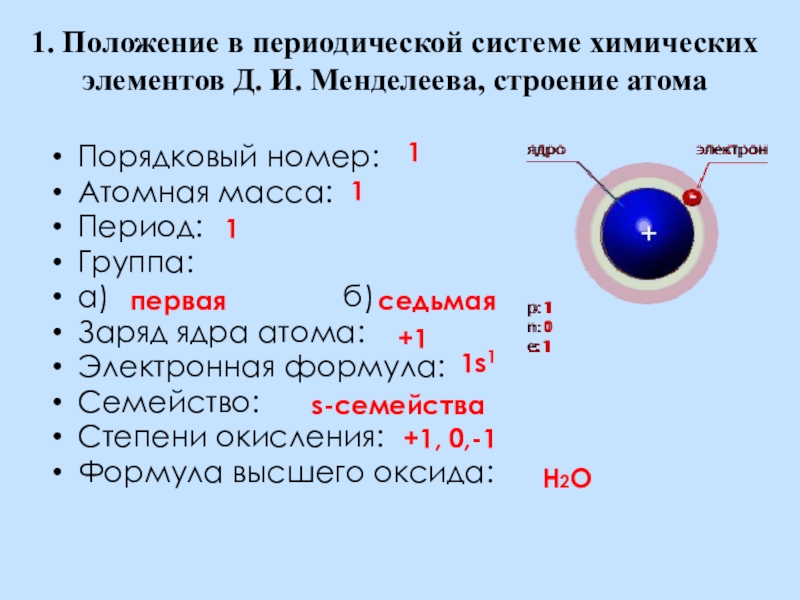
Слайд 41. Положение в периодической системе химических элементов Д. И. Менделеева, строение
Порядковый номер:
Атомная масса:
Период:
Группа:
а) б)
Заряд ядра атома:
Электронная формула:
Семейство:
Степени окисления:
Формула высшего оксида:
1
1
1
первая
седьмая
+1
1s1
s-семейства
+1, 0,-1
Н2О
Слайд 5Почему водород является элементом главной подгруппы?
Первой группы:
На внешнем единственном энергетическом уровне
С неметаллами реагирует как щелочной металл, проявляя восстановительные свойства
Седьмой группы:
До устойчивого состояния атома не достает один электрон, как в атомах галогенов
С металлами реагирует как галоген, проявляя
окислительные свойства
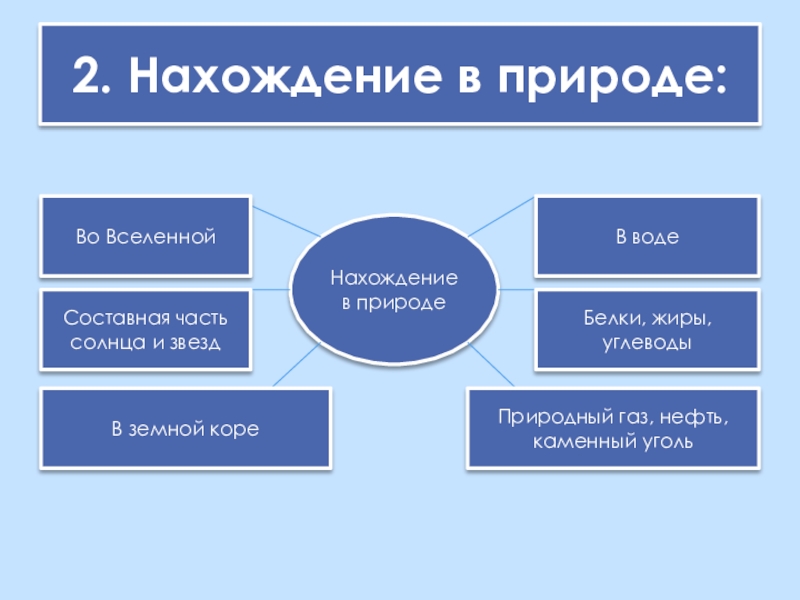
Слайд 62. Нахождение в природе:
Нахождение в природе
В воде
Во Вселенной
Составная часть солнца и
Белки, жиры, углеводы
В земной коре
Природный газ, нефть, каменный уголь
Слайд 8Получение водорода в лаборатории
1. Zn + 2HCI = ZnCI2 + H2
2.
3. 2AI + 2NaOH + 6H2O =2Na(AI(OH)4) + 3H2
4. 2AI + 6H2O = 2AI(OH)3 + 3H2
Слайд 9Промышленный способ получения водорода
1. Конверсией водяных паров:
с углеродом:
С + Н2О
с метаном:
СН4 + Н2О = СО + 3Н2
2. Разложением воды под действием электрического тока:
2Н2О = 2Н2 + О2
Слайд 10Водород простое вещество
Молекулярная формула:
Химическая связь:
Схема образования химической связи:
электронная формула:
структурная формула:
Молярная масса:
Н2
ковалентная неполярная
Н (:) Н
Н – Н
М(Н2)=2г/моль
Слайд 113. Свойства водорода
Физические:
Агрегатное состояние:
Цвет:
Запах:
Легче или тяжелее
воздуха?
Растворимость в воде:
Химические:
1)2Н2 +
2)Н2 + Сl2 =
3)H2 + S =
4)3H2 + N2 =
5)H2 + CuO =
6)H2 + Ca =
Чем является водород в этих реакциях?
Слайд 123. Свойства водорода
физические:
химические:
1)2Н2 + О2 = 2Н2О
2)Н2 + Сl2 = 2НСl
3)H2
4)3H2 + N2 = 2NH3
аммиак
5)H2 + CuO = Cu + H2O
6)H2 + Ca = CaH2
c 1-5 – восстановитель,
в 6 – окислитель
самый легкий газ
бесцветный
в воде малорастворим
без запаха
легче воздуха в 14,5 раз
темп. кип. = -253С
Слайд 14Водородная бомба
Оружие большой разрушительной силы (порядка мегатонн в
процессам, протекающим
на Солнце и
других звездах.
Слайд 154. Применение водорода
Водород используется для наполнения метеорологических зондов
Слайд 18Домашнее задание
§17 изучить, подготовится к тесту,
Задания № 1, 4 на
Дополнительное задание:
Подготовить презентацию по изотопам водорода.