- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии в 10кл на тему Бензол
Содержание
- 1. Презентация к уроку химии в 10кл на тему Бензол
- 2. Решим задачуОпределите формулу углеводорода, плотность паров которого
- 3. Из истории открытия.В 1681 году при нагревании
- 4. Этот вопрос исследовал М.Фарадей.На дне железных баллонов,
- 5. Майкл Фарадей (1791 - 1867) Английский физик
- 6. Фридрих Август Кекуле 1829 - 1896Немецкий химик-органик.
- 7. Слайд 7
- 8. Слайд 8
- 9. Отношение бензола к бромной воде и перманганату калия
- 10. Образование σ-связей в молекуле бензолаАтомы углерода в
- 11. Образование π-системы в молекуле бензола Каждый атом
- 12. Таким образом, в молекуле бензола осуществляется круговое
- 13. Словарь Ароматические углеводороды (арены) – это углеводороды
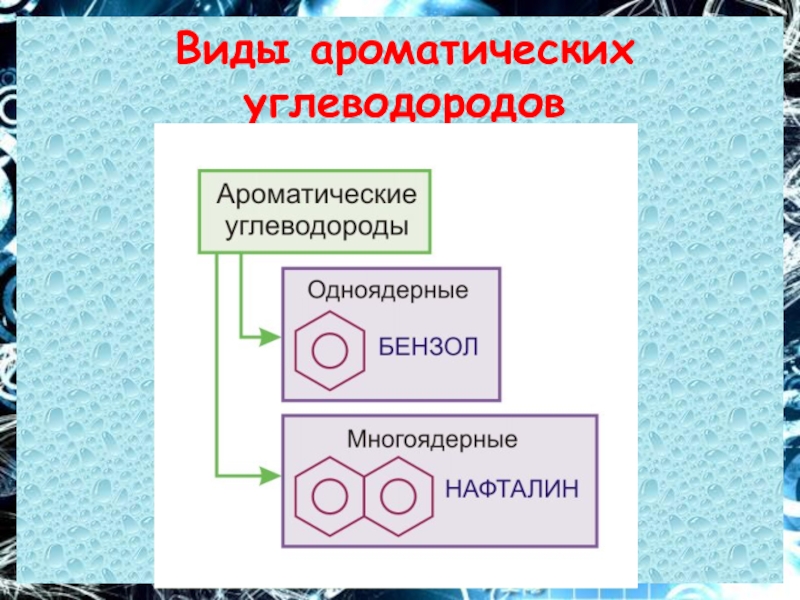
- 14. Виды ароматических углеводородов
- 15. Гомологи бензола
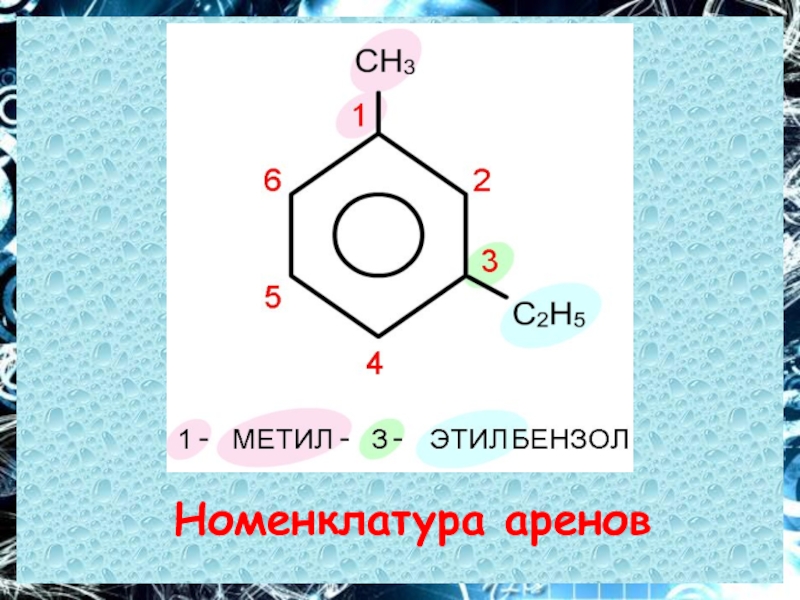
- 16. Номенклатура аренов
- 17. Физические свойстваБензол – бесцветная, летучая, огнеопасная жидкость
- 18. Химические свойстваРеакции окисленияГорение
- 19. Химические свойстваРеакции окисленияМягкое окислениеБензол не обесцвечивает раствор перманганата калия
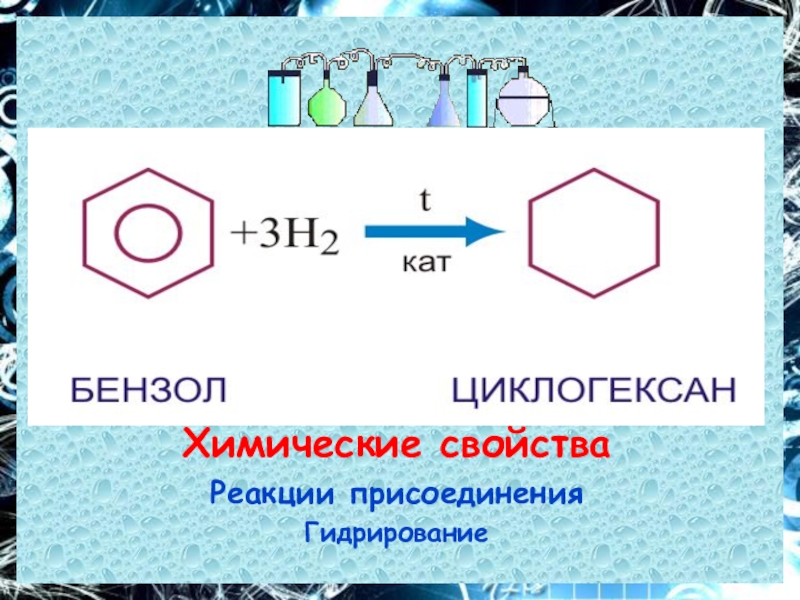
- 20. Химические свойстваРеакции присоединенияГидрирование
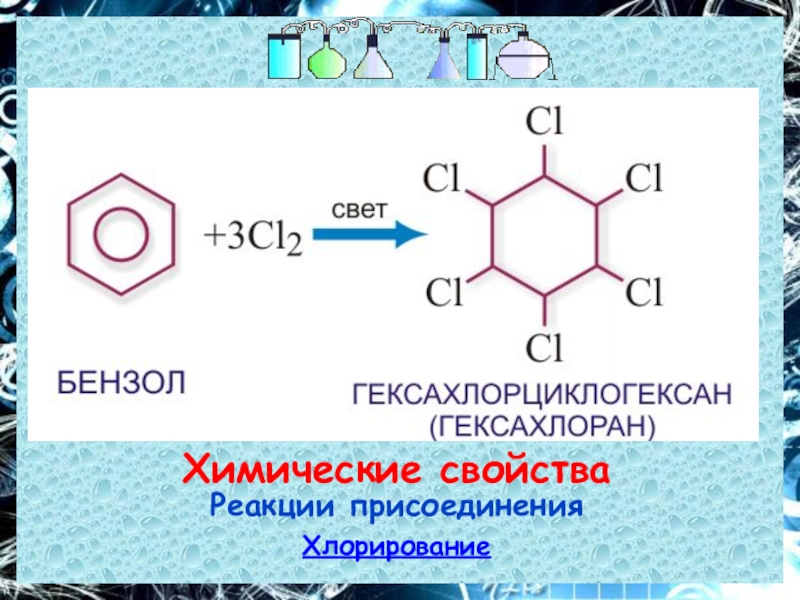
- 21. Химические свойстваРеакции присоединенияХлорирование
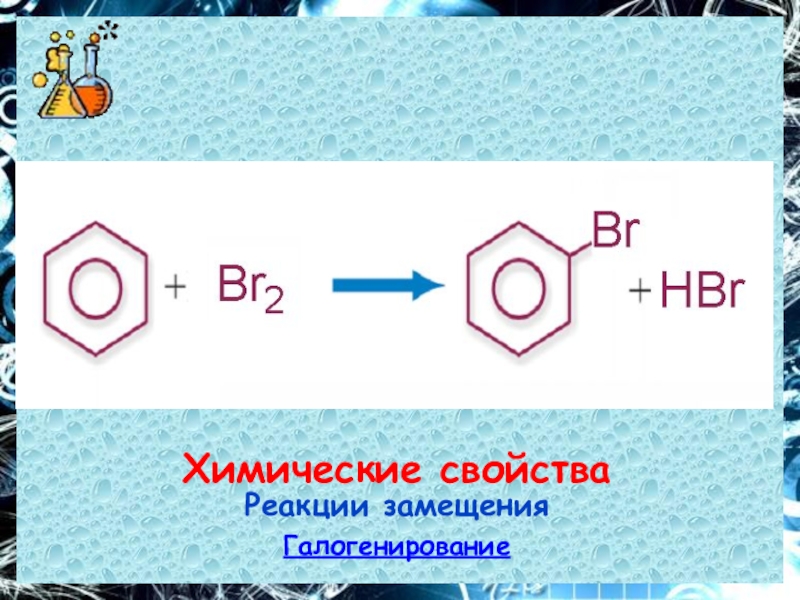
- 22. Химические свойстваРеакции замещенияГалогенирование
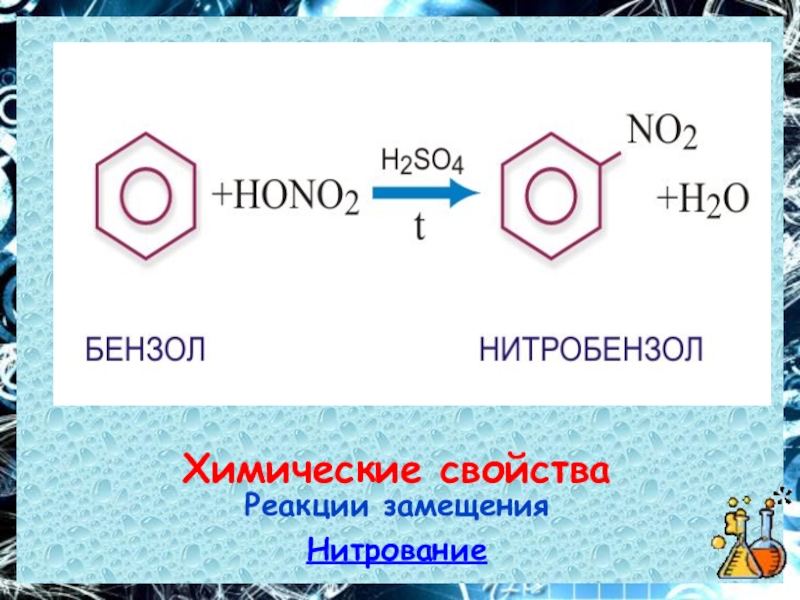
- 23. Химические свойстваРеакции замещенияНитрование
- 24. Тест.1. Общая формула ароматических углеводородов: 1) CnH2n-2;
- 25. 6. Состояние гибридизации атомов углерода в молекуле
Решим задачуОпределите формулу углеводорода, плотность паров которого по водороду равна 39. Массовая доля углерода в веществе составляет 92,3%
Слайд 2Решим задачу
Определите формулу углеводорода, плотность паров которого по водороду равна 39.
Массовая доля углерода в веществе составляет 92,3%
Слайд 3Из истории открытия.
В 1681 году при нагревании каменного угля без доступа
воздуха был получен светильный газ,
В 1792 году начала работать промышленная установка по его производству,
В 1814 году в Лондоне целый квартал освещался этим газом, но было отмечено, что в холодное время года газовые фонари давали тусклое освещение.
В 1792 году начала работать промышленная установка по его производству,
В 1814 году в Лондоне целый квартал освещался этим газом, но было отмечено, что в холодное время года газовые фонари давали тусклое освещение.
Слайд 4Этот вопрос исследовал М.Фарадей.
На дне железных баллонов, в которых под давлением
хранили светильный газ, он обнаружил жидкость и вывел ее состав.
Слайд 5Майкл Фарадей (1791 - 1867)
Английский физик и химик, член Лондонского
королевского общества. В 1823 г. впервые получил жидкие хлор, сероводород, оксид углерода(IV), аммиак, оксид азота(IV). В 1825 г. открыл бензол, изучил его физические и некоторые химические свойства. Положил начало исследованиям каучука. В 1833 - 1836 гг. установил количественные законы электролиза.
Слайд 6Фридрих Август Кекуле
1829 - 1896
Немецкий химик-органик. Предложил структурную формулу молекулы бензола.
С целью проверки гипотезы о равноценности всех шести атомов водорода в молекуле бензола получил его галоген-, нитро-, амино-, и карбоксипроизводные.
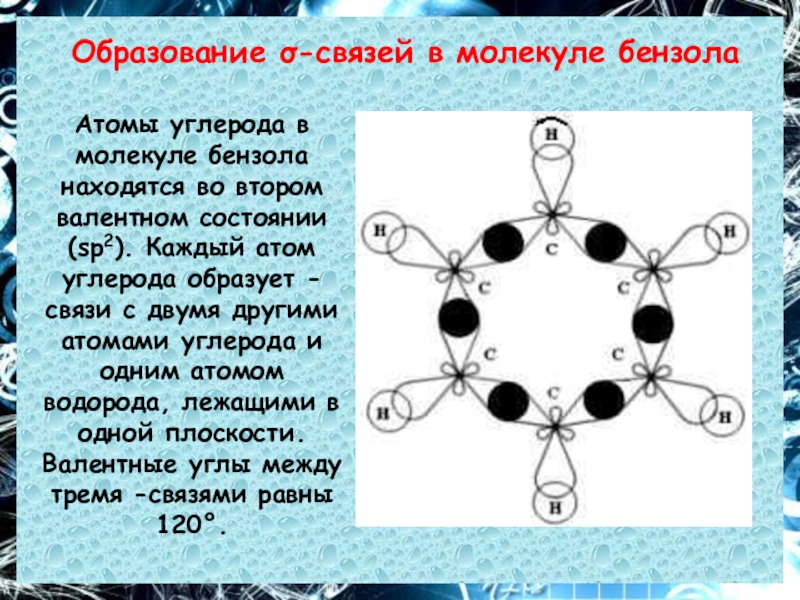
Слайд 10Образование σ-связей в молекуле бензола
Атомы углерода в молекуле бензола находятся во
втором валентном состоянии (sp2). Каждый атом углерода образует -связи с двумя другими атомами углерода и одним атомом водорода, лежащими в одной плоскости. Валентные углы между тремя -связями равны 120°.
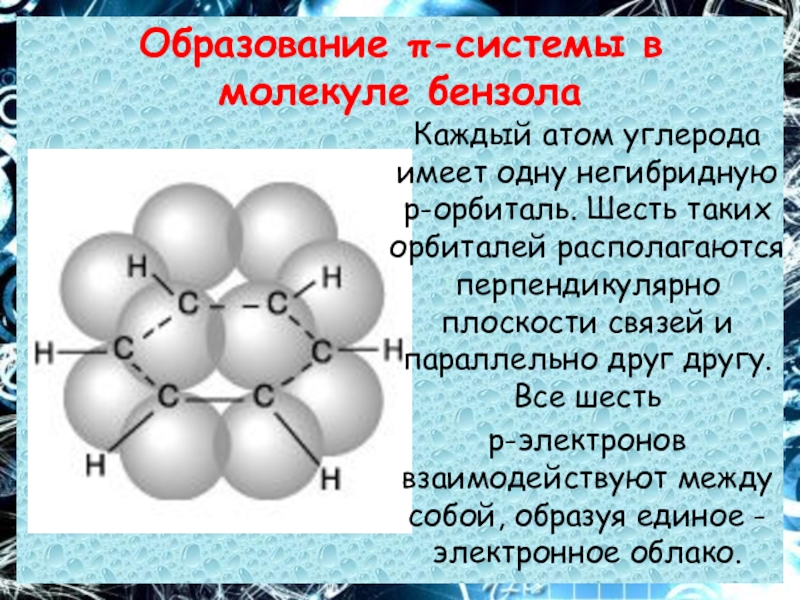
Слайд 11Образование π-системы в молекуле бензола
Каждый атом углерода имеет одну негибридную
р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскости связей и параллельно друг другу. Все шесть
р-электронов взаимодействуют между собой, образуя единое -электронное облако.
р-электронов взаимодействуют между собой, образуя единое -электронное облако.
Слайд 12Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая -электронная плотность
в этой сопряженной системе располагается над и под плоскостью кольца.
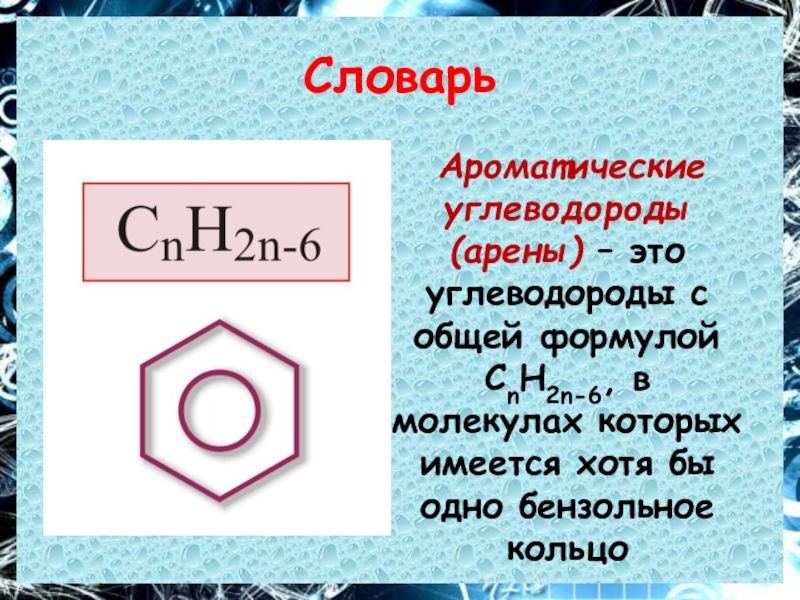
Слайд 13Словарь
Ароматические углеводороды (арены) – это углеводороды с общей формулой СnH2n-6,
в молекулах которых имеется хотя бы одно бензольное кольцо
Слайд 17Физические свойства
Бензол – бесцветная, летучая, огнеопасная жидкость с неприятным запахом. Он
легче воды ( =0,88 г/см3) и с ней не смешивается, но растворим в органических растворителях, и сам хорошо растворяет многие вещества. Бензол кипит при 80,1 С, при охлаждении легко застывает в белую кристаллическую массу. Бензол и его пары ядовиты. Систематическое вдыхание его паров вызывает анемию и лейкемию.
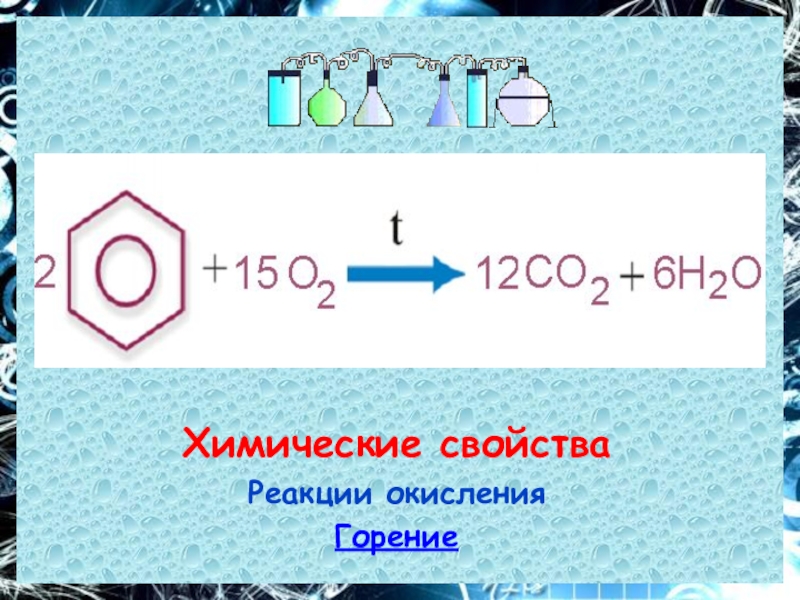
Слайд 19Химические свойства
Реакции окисления
Мягкое окисление
Бензол не обесцвечивает раствор перманганата калия
Слайд 24Тест.
1. Общая формула ароматических углеводородов:
1) CnH2n-2;
3) CnH2n;
2) CnH2n-6; 4) CnH2n+2.
2.Бензолу не свойственно:
1) жидкое агрегатное состояние;
2) характерный запах;
3) температура кипения 80,1º С;
4) хорошая растворимость в воде.
3. Расстояние между атомами углерода в бензоле сокращается за счет:
1) циклического строения молекулы;
2) расположения гибридных орбиталей в одной плоскости;
3) влияние π-электронного облака;
4) равномерного распределения электронной плотности.
4. Вещества с общей формулой CnH2n-6 относятся к классу:
1) алканов; 3) алкинов;
2) алкенов; 4) аренов.
5. В молекуле бензола шесть атомов углерода образуют:
1) правильный шестиугольник;
2) неправильный шестиугольник;
3) треугольник с боковыми ответвлениями;
4) квадрат с боковыми ответвлениями.
2) CnH2n-6; 4) CnH2n+2.
2.Бензолу не свойственно:
1) жидкое агрегатное состояние;
2) характерный запах;
3) температура кипения 80,1º С;
4) хорошая растворимость в воде.
3. Расстояние между атомами углерода в бензоле сокращается за счет:
1) циклического строения молекулы;
2) расположения гибридных орбиталей в одной плоскости;
3) влияние π-электронного облака;
4) равномерного распределения электронной плотности.
4. Вещества с общей формулой CnH2n-6 относятся к классу:
1) алканов; 3) алкинов;
2) алкенов; 4) аренов.
5. В молекуле бензола шесть атомов углерода образуют:
1) правильный шестиугольник;
2) неправильный шестиугольник;
3) треугольник с боковыми ответвлениями;
4) квадрат с боковыми ответвлениями.
Слайд 256. Состояние гибридизации атомов углерода в молекуле бензола:
1) sp;
3) sp3;
2) sp2; 4) sp и sp2.
7. При хлорировании бензола на сильном свету получается:
1) хлорбензол;
2) 1, 2, 3-трихлорбензол;
3) бромбензол;
4) гексахлорциклогексан.
8. При взаимодействии бензола с бромом в присутствии катализатора (FeBr3) получается:
1) бромбензол; 2) гексабромциклогексан;
3) 1, 3, 5-трибромбензол; 4) 1, 2-дибромбензол.
9. Бензол, как и непредельные углеводороды, вступает в реакции:
1) полимеризации; 3) окисление раствором перманганата калия;
2) гидрогалогенирования; 4) гидрирования.
2) sp2; 4) sp и sp2.
7. При хлорировании бензола на сильном свету получается:
1) хлорбензол;
2) 1, 2, 3-трихлорбензол;
3) бромбензол;
4) гексахлорциклогексан.
8. При взаимодействии бензола с бромом в присутствии катализатора (FeBr3) получается:
1) бромбензол; 2) гексабромциклогексан;
3) 1, 3, 5-трибромбензол; 4) 1, 2-дибромбензол.
9. Бензол, как и непредельные углеводороды, вступает в реакции:
1) полимеризации; 3) окисление раствором перманганата калия;
2) гидрогалогенирования; 4) гидрирования.