- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии по теме Кремний и его соединения 9 класс
Содержание
- 1. Презентация к уроку химии по теме Кремний и его соединения 9 класс
- 2. Закончите предложения, начиная каждый новый ответ заглавной
- 3. Речной песок, кварцевый песок, кремнезем – SiO2
- 4. Минералы, состоящие из оксида кремния
- 5. Кристалл кварца
- 6. Кремний
- 7. Электронное строение атома кремнияSi+14282Р = 14ē = 14N = 14841s22s22p63s23p2Электронная формула -Валентные возможности –II;IV
- 8. Свойства атомаSi0- 4евосстановитель+ 4еокислительSi+4Si-4 Кремний, отдавая все
- 9. ПОЛУЧЕНИЕ КРЕМНИЯSiO2+C=Si+СО 2SiO2+2Mg=Si+2MgО SiO2 → Mg2Si → SiH4 → SiSiO2+4Mg=Mg2Si+2MgО Mg2Si+4H2O=SiH4+2Mg(ОH) 2 SiH4=Si+2H 2
- 10. Способ получения кремния в чистом виде разработан
- 11. Физические свойства кремнияКремний - неметалл, существует в
- 12. Химические свойства кремнияХимически кремний малоактивен. При комнатной
- 13. Химические свойства кремнияс хлором, бромом и йодом —
- 14. Химические свойства кремнияПри нагревании до 400 –
- 15. Взаимодействие кремния с щелочамиSi + 2NaOH +
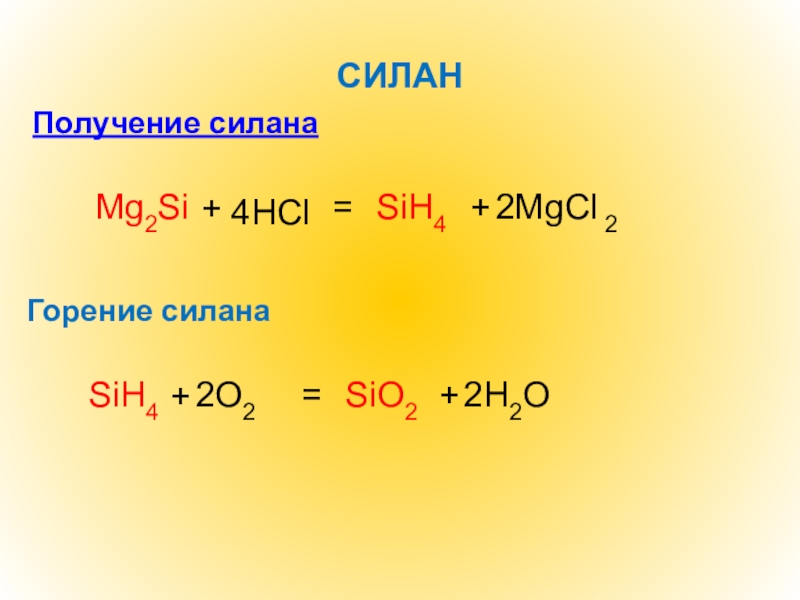
- 16. СИЛАНПолучение силанаMg2Si+=SiH4+2MgCl 2 Горение силанаSiH4+2О2=SiО2+2H2O4HCl
- 17. Биологическая роль кремнияКремний в больших количествах концентрируют
- 18. Кремний играет важную роль в
- 19. Домашнее задание§ 31, упражнение 2.Подумать над вопросом:Почему
- 20. Урок завершенСпасибо за сотрудничество
Закончите предложения, начиная каждый новый ответ заглавной буквой с красной строкиПоложительно заряженный ионЭлемент 5 периода ПСХЭ, щелочной металлЛантаноид, в ядре его атома 63 протонаАвтор периодического законаВещества, которые не проводят электрический токРазновидность атомов элементов с одинаковым зарядом
Слайд 1Презентация
к уроку химии по теме «Кремний и его соединения»
9 класс
Подготовила:
учитель химии Донскеева Г.А.
Слайд 2Закончите предложения, начиная каждый новый ответ заглавной буквой с красной строки
Положительно
заряженный ион
Элемент 5 периода ПСХЭ, щелочной металл
Лантаноид, в ядре его атома 63 протона
Автор периодического закона
Вещества, которые не проводят электрический ток
Разновидность атомов элементов с одинаковым зарядом ядра
Твёрдое вещество серого цвета, галоген
Элемент 5 периода ПСХЭ, щелочной металл
Лантаноид, в ядре его атома 63 протона
Автор периодического закона
Вещества, которые не проводят электрический ток
Разновидность атомов элементов с одинаковым зарядом ядра
Твёрдое вещество серого цвета, галоген
Слайд 7
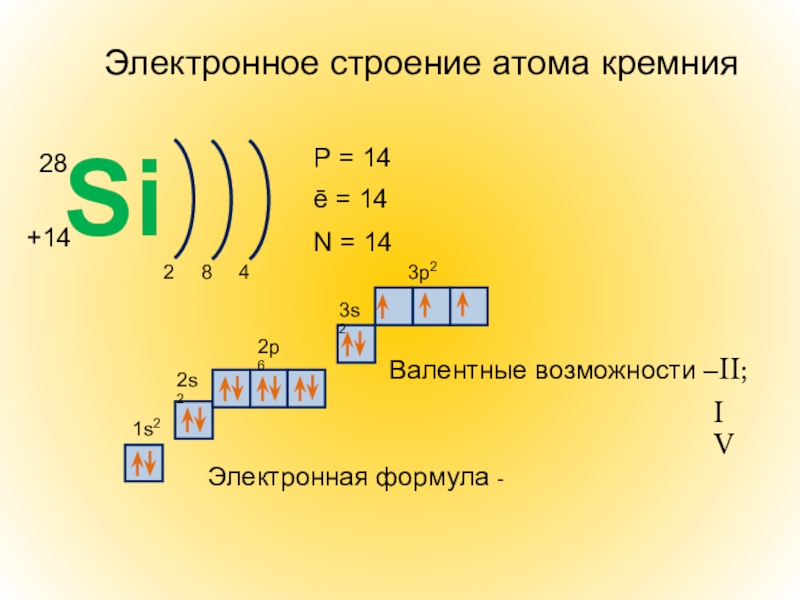
Электронное строение атома кремния
Si
+14
28
2
Р = 14
ē = 14
N = 14
8
4
1s2
2s2
2p6
3s2
3p2
Электронная формула
-
Валентные возможности –II;
IV
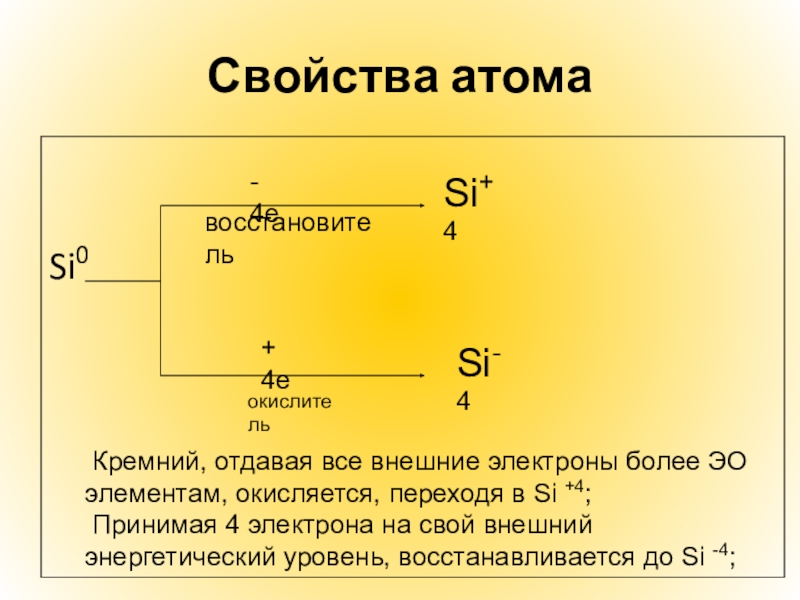
Слайд 8Свойства атома
Si0
- 4е
восстановитель
+ 4е
окислитель
Si+4
Si-4
Кремний, отдавая все внешние электроны более ЭО
элементам, окисляется, переходя в Si +4;
Принимая 4 электрона на свой внешний энергетический уровень, восстанавливается до Si -4;
Принимая 4 электрона на свой внешний энергетический уровень, восстанавливается до Si -4;
Слайд 9ПОЛУЧЕНИЕ КРЕМНИЯ
SiO2
+
C
=
Si
+
СО 2
SiO2
+
2Mg
=
Si
+
2MgО
SiO2 → Mg2Si → SiH4 → Si
SiO2
+
4Mg
=
Mg2Si
+
2MgО
Mg2Si
+
4H2O
=
SiH4
+
2Mg(ОH)
2
SiH4
=
Si
+
2H 2
Слайд 10
Способ получения кремния
в чистом виде разработан
Николаем Николаевичем
Бекетовым.
Кремний
в России производится
на заводах:
г. Каменск - Уральский (Свердловская область)
г. Шелех (Иркутская область).
на заводах:
г. Каменск - Уральский (Свердловская область)
г. Шелех (Иркутская область).
Слайд 11Физические свойства кремния
Кремний - неметалл, существует в кристаллическом и аморфном состоянии.
Кристаллическая решетка гранецентрированная типа алмаза, но из – за большей длины связи между Si – Si, твердость кремния значительно меньше, чем алмаза
Слайд 12Химические свойства кремния
Химически кремний малоактивен.
При комнатной температуре реагирует только c
фтором, образуя летучий фторид кремния:
Si + 2F2= SiF4
Si + 2F2= SiF4
Слайд 13Химические свойства кремния
с хлором, бромом и йодом —
с образованием соответствующих
легко
летучих хлорид кремния и бромид кремния
Si + 2Cl2 = SiCl4
Si + 2Br2 = SiBr4
Si + 2Cl2 = SiCl4
Si + 2Br2 = SiBr4
Слайд 14Химические свойства кремния
При нагревании до 400 – 5000С кремний реагирует с
кислородом с образованием оксида кремния (IV):
Si + O2 = SiO2
Si + O2 = SiO2
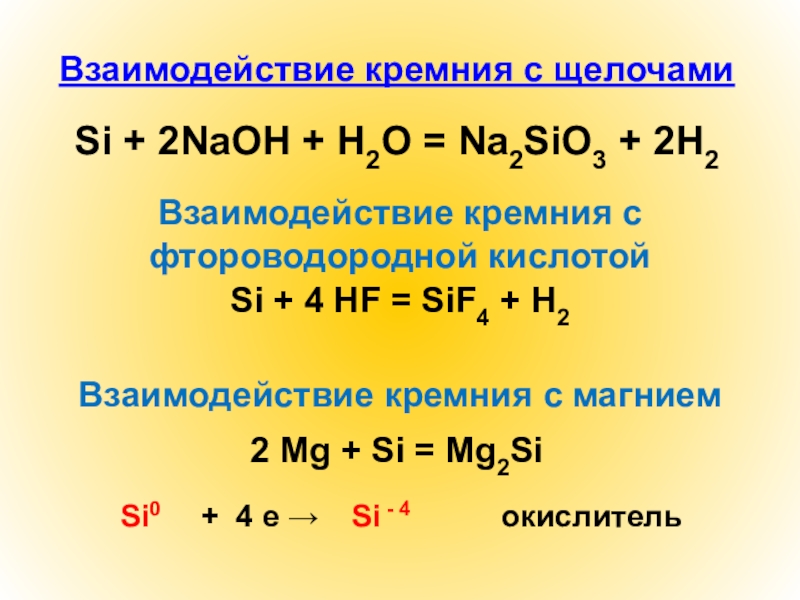
Слайд 15Взаимодействие кремния с щелочами
Si + 2NaOH + H2O = Na2SiO3 +
2H2
Взаимодействие кремния с фтороводородной кислотой
Si + 4 HF = SiF4 + H2
Взаимодействие кремния с магнием
2 Mg + Si = Mg2Si
Si0
+ 4 е →
Si - 4
окислитель
Слайд 17Биологическая роль кремния
Кремний в больших количествах концентрируют морские организмы —диатомовые водоросли,
радиолярии, губки. Много кремния в хвощах и злаках, особенно в рисе и бамбуке.
Мышечная ткань человека содержит (1-2)·10-2% кремния, костная ткань — 17·10-4%, кровь — 3,9 мг/л. С пищей в организм человека ежедневно поступает до 1 г кремния.
Мышечная ткань человека содержит (1-2)·10-2% кремния, костная ткань — 17·10-4%, кровь — 3,9 мг/л. С пищей в организм человека ежедневно поступает до 1 г кремния.
радиолярии
Диатомовые водоросли
Слайд 18 Кремний играет важную роль в процессе минерализации костной ткани; необходим
для поддержания эластичности стенки артерий, оказывает положительное влияние на иммунитет и замедляет процессы старения в тканях организма человека.
. С возрастом его уровень в организме снижается, поэтому у пожилых людей потребность в кремнии, как правило, повышается. Улучшают усвоение кремния организмом наличие кальция, магния, марганца и калия.
Продукты содержащие кремний
Слайд 19Домашнее задание
§ 31, упражнение 2.
Подумать над вопросом:
Почему углерод называют основным элементом
живой природы, а кремний – основным элементом неживой природы?