- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку химии 9 класс Азотная кислота и нитраты
Содержание
- 1. Презентация к уроку химии 9 класс Азотная кислота и нитраты
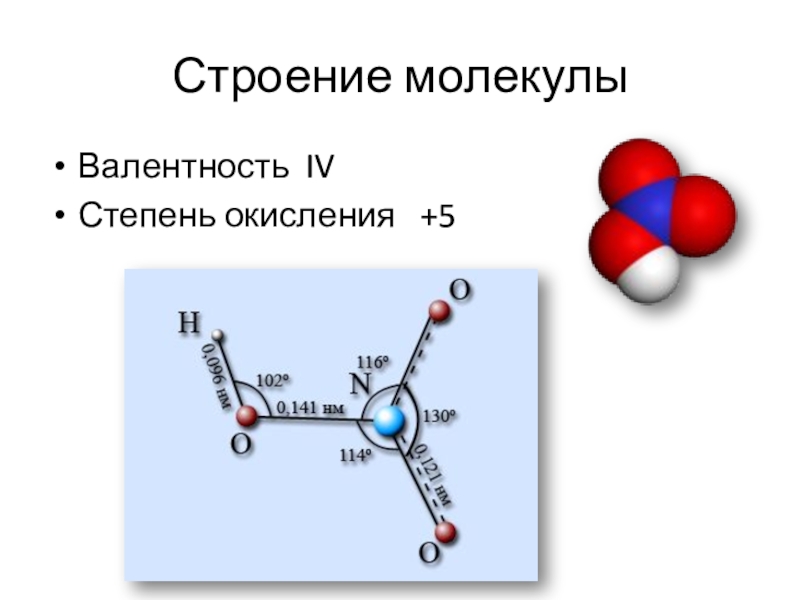
- 2. Строение молекулыВалентность IVСтепень окисления +5
- 3. Физические свойства Бесцветная жидкость, дымящая на воздухе.
- 4. Слайд 4
- 5. Взаимодействие азотной кислоты с белкамиПри взаимодействии концентрированной
- 6. «Царская водка»«Царской водкой» называется смесь концентрированных азотной
- 7. «Меланж» Смесь HNO3 концентрации 100% и H2SO4 концентрации 96% при их соотношении по объему 9:1
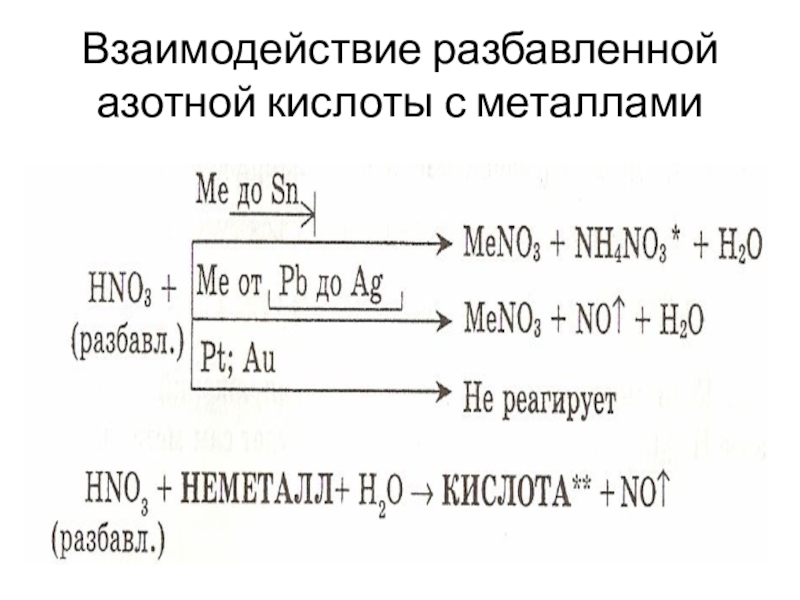
- 8. Взаимодействие разбавленной азотной кислоты с металлами
- 9. Слайд 9
- 10. Взаимодействие с неметалламиПри взаимодействии с неметаллами образуется
- 11. Соли азотной кислоты – нитраты (селитры)
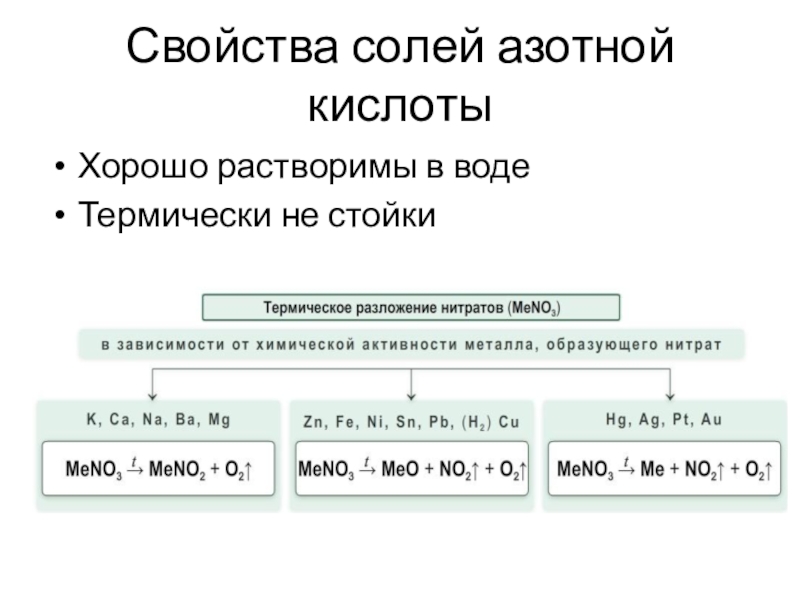
- 12. Свойства солей азотной кислотыХорошо растворимы в водеТермически не стойки
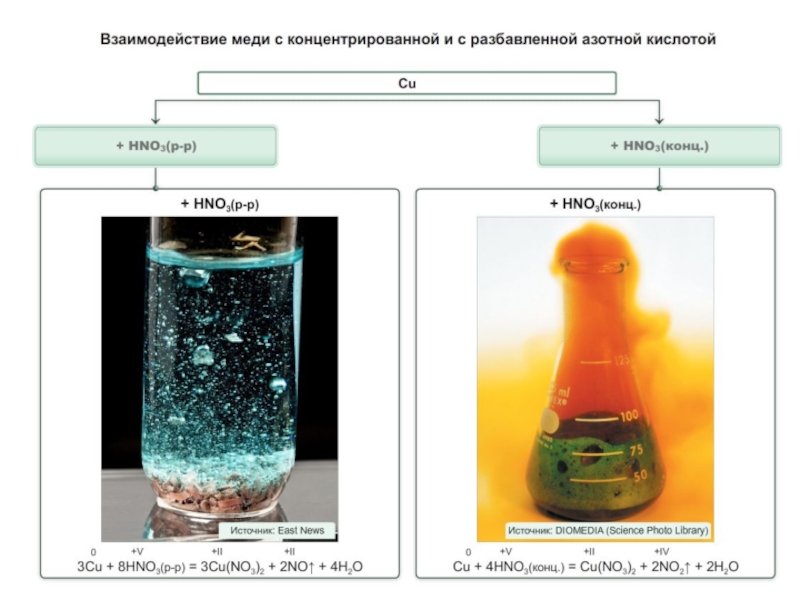
- 13. Сильные электролиты, проявляют все свойства солейCu(NO3)2 +
- 14. Качественная реакция на нитрат-ионЧтобы определить, содержатся ли
- 15. Слайд 15
Строение молекулыВалентность IVСтепень окисления +5
Слайд 3Физические свойства
Бесцветная жидкость, дымящая на воздухе.
Едкий запах.
Желтый цвет
концентрированной кислоты -разложение с образованием NO2
4HNO3 = 4NO2↑ + 2H2O + O2↑
Гигроскопична.
С водой смешивается в любых соотношениях.
4HNO3 = 4NO2↑ + 2H2O + O2↑
Гигроскопична.
С водой смешивается в любых соотношениях.
Слайд 5Взаимодействие азотной кислоты с белками
При взаимодействии концентрированной азотной кислоты с белками
образуются вещества жёлтого цвета. Поэтому, при попадании азотной кислоты на кожу, остаются жёлтые пятна.
Ксантопротеиновая реакция
Под действием азотной кислоты воспламеняются бумага, масло, древесина, уголь.
Ксантопротеиновая реакция
Под действием азотной кислоты воспламеняются бумага, масло, древесина, уголь.
Слайд 6«Царская водка»
«Царской водкой» называется смесь концентрированных азотной и соляной кислот. Окислительная
способность этой смеси превосходит окислительную способность чистой азотной кислоты. В «царской водке» растворяются даже золото и платина. Ещё более активна смесь концентрированных азотной и плавиковой кислот.
Слайд 7«Меланж»
Смесь HNO3 концентрации 100% и H2SO4 концентрации 96% при их
соотношении по объему 9:1
Слайд 10Взаимодействие с неметаллами
При взаимодействии с неметаллами образуется кислота, в которой у
неметалла высшая степень окисления, и продукт по схеме:
NO неMe + HNO3 NO2
P + 5HNO3(к.) H3PO4 + 5NO2 + H2O
3P + 5HNO3(р) + 2H2O 3H3PO4 + 5NO
NO неMe + HNO3 NO2
P + 5HNO3(к.) H3PO4 + 5NO2 + H2O
3P + 5HNO3(р) + 2H2O 3H3PO4 + 5NO
Слайд 13Сильные электролиты,
проявляют все свойства солей
Cu(NO3)2 + 2KOH = Cu(OH)2↓ + 2KNO3
AgNO3
+ NaCl = AgCl↓ + NaNO3
Pb(NO3)2 + Zn = Pb + Zn(NO3)2
Ba(NO3)2 + H2SO4 = BaSO4↓ + 2HNO3
Pb(NO3)2 + Zn = Pb + Zn(NO3)2
Ba(NO3)2 + H2SO4 = BaSO4↓ + 2HNO3
Слайд 14Качественная реакция на нитрат-ион
Чтобы определить, содержатся ли в исследуемом растворе нитрат
ионы NO3, к исследуемому раствору добавляют концентрированную серную кислоту и немного медных стружек, раствор подогревают. Выделение бурого газа является характерным признаком данной реакции.
NaNO3 + H2SO4(конц.) = NaHSO4 + HNO3
t
4HNO3 + Cu = Cu(NO3)2 + 2NO2↑ + 2H2O
NaNO3 + H2SO4(конц.) = NaHSO4 + HNO3
t
4HNO3 + Cu = Cu(NO3)2 + 2NO2↑ + 2H2O