- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку Алюминий и его соединения
Содержание
- 1. Презентация к уроку Алюминий и его соединения
- 2. «Другого ничего в природе нет. Ни
- 3. Сравнение строения атомов Na, Mg и
- 4. Слайд 4
- 5. Задания для работы в группах І группа:
- 6. Скажи мне - и я забуду, покажи
- 7. Реактивы для лабораторных опытов
- 8. Блок - схемаАмфотерность – это способность вещества
- 9. Получение алюминия В 1825 году Х.Эрстед
- 10. Сплавы алюминия Дюралюминий – 94% Al; 4%
- 11. Применение алюминия
- 12. Кому не жаль «денег»
- 13. Объявление Потерялся породистый оксид, принадлежащий жильцу третьего подъезда.
- 14. «Нигде нет покоя» Когда Алюминий пришел в кафе,
- 15. Решить задачуРассчитайте объем водорода, выделившегося при взаимодействии
«Другого ничего в природе нет. Ни здесь, ни там в космических глубинах. Все от песчинок малых до планет – Из элементов состоит единых»
Слайд 2«Другого ничего в природе нет. Ни здесь, ни там в космических глубинах. Все
от песчинок малых до планет –
Из элементов состоит единых»
Степан Щипачев
«Читая Менделеева»
Слайд 3Сравнение строения атомов
Na, Mg и Al
Сходство: одинаковое число энергетических уровней
(3)
Отличия: - разный заряд ядра атома
- различное число электронов на последнем энергетическом уровне.
Отличия: - разный заряд ядра атома
- различное число электронов на последнем энергетическом уровне.
Слайд 5Задания для работы в группах
І группа: Нахождение алюминия в природе, содержание
в земной коре, получение.
ІІ группа: Химические свойства алюминия (взаимодействие с неметаллами).
ІІІ группа: Взаимодействие с кислотами и щелочами.
IV группа: Применение алюминия и его сплавов.
ІІ группа: Химические свойства алюминия (взаимодействие с неметаллами).
ІІІ группа: Взаимодействие с кислотами и щелочами.
IV группа: Применение алюминия и его сплавов.
Слайд 6Скажи мне - и я забуду, покажи мне - и я
запомню, дай сделать - и я пойму.
(Китайская притча)
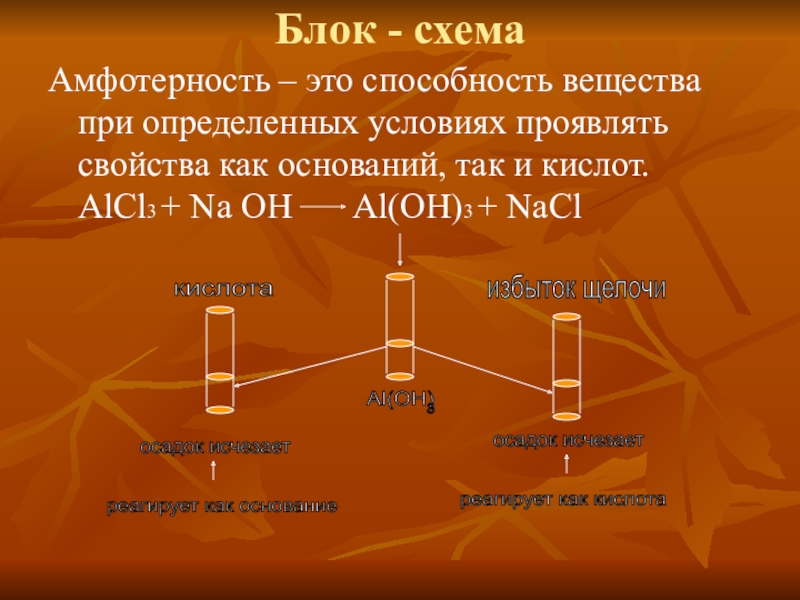
Слайд 8Блок - схема
Амфотерность – это способность вещества при определенных условиях проявлять
свойства как оснований, так и кислот. AlCl3 + Na OH Al(OH)3 + NaCl
кислота
избыток щелочи
осадок исчезает
осадок исчезает
Al(OH)
3
реагирует как основание
реагирует как кислота
Слайд 9Получение алюминия
В 1825 году Х.Эрстед получил алюминий химическим путем: при
взаимодействии хлорида алюминия с металлическим калием.
Первые кусочки металла были величиной с булавочную головку.
Впервые слиток алюминия был представлен на Парижской выставке в 1855 году. Один килограмм его стоил баснословно дорого – 1000 золотых рублей.
Первые кусочки металла были величиной с булавочную головку.
Впервые слиток алюминия был представлен на Парижской выставке в 1855 году. Один килограмм его стоил баснословно дорого – 1000 золотых рублей.
Слайд 10Сплавы алюминия
Дюралюминий – 94% Al; 4% Cu; 0,5% Mg;
Mn; Si; Fe.
Близок к стали по прочности, но легче её в 3 раза (самолетостроение).
Силумин – 85-90% Al; 10-14% Si; 0,1% Na.
Пригоден для литья (авто и машиностроение)
Гидроналий – 90% Al; 10% Mg.
Не подвергается коррозии в морской воде (кораблестроение).
Близок к стали по прочности, но легче её в 3 раза (самолетостроение).
Силумин – 85-90% Al; 10-14% Si; 0,1% Na.
Пригоден для литья (авто и машиностроение)
Гидроналий – 90% Al; 10% Mg.
Не подвергается коррозии в морской воде (кораблестроение).
Слайд 12Кому не жаль «денег»
Однажды два приятеля
Алюминий и Железо поздно возвращались домой. И вдруг на них неожиданно напал грабитель Хлор, который потребовал выложить кошельки с электронами.
Как вы считаете, какой из приятелей легче расстанется с кошельком? Объясните почему?
Как вы считаете, какой из приятелей легче расстанется с кошельком? Объясните почему?
Слайд 13Объявление
Потерялся породистый оксид, принадлежащий жильцу третьего подъезда. Особые приметы: имеет молекулярную
массу 102.
Прошу вернуть за вознаграждение.(Если Вы сможете найти этот оксид и указать его химический характер, то приходите за вознаграждением).
Прошу вернуть за вознаграждение.(Если Вы сможете найти этот оксид и указать его химический характер, то приходите за вознаграждением).
Слайд 14«Нигде нет покоя»
Когда Алюминий пришел в кафе, там уже сидели: Кислород,
Хлорид натрия в растворе, разбавленная Серная кислота, Гидроксид калия и концентрированная Азотная кислота.
Присутствие каких посетителей кафе испортило ему настроение? Почему? Подтвердите ответ уравнениями реакций.
Присутствие каких посетителей кафе испортило ему настроение? Почему? Подтвердите ответ уравнениями реакций.
Слайд 15Решить задачу
Рассчитайте объем водорода, выделившегося при взаимодействии алюминия с 200г раствора
гидроксида натрия, если массовая доля щелочи в нем 25%.