химии
Евстратова Лариса Фёдоровна
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к проекту Коррозия металлов
Содержание
- 1. Презентация к проекту Коррозия металлов
- 2. Востребованность данной работыВостребованность данной темы заключается в
- 3. План работыОбщая характеристика металлов.Теоретическая часть.Экспериментальная работа.Заключение.
- 4. Общая характеристика металлов.Из 110 химических элементов-88 металлы.Все
- 5. Химические свойства металлов.Химические свойства металлов определяются слабой
- 6. Взаимодействие металлов с водными растворами солей менее активных металлов можно иллюстрировать примером: Fe+CuS04=FeS04+Cu
- 7. Что же такое коррозияНаиболее распространенная проблема металлов
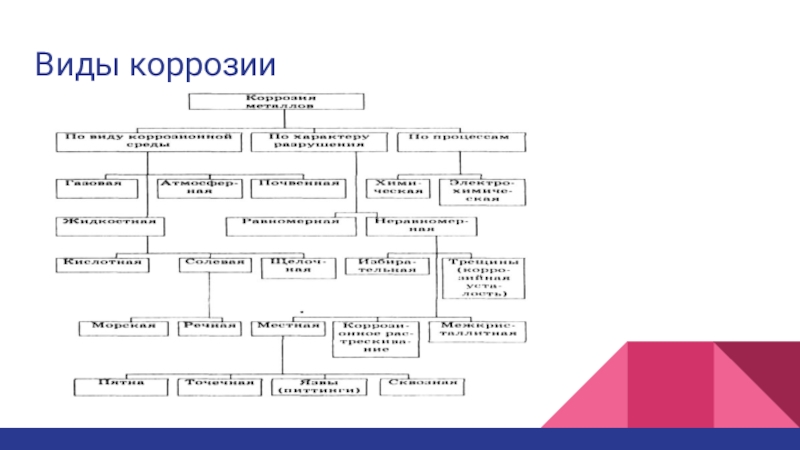
- 8. Виды коррозии
- 9. Экспериментальная работаЧто бы изучить коррозию мы проделали
- 10. Первый ОпытЖелезный гвоздь погруженный в сухой песок не проявлял признаков коррозии.
- 11. Второй опытЖелезный гвоздь погруженный в воду и растительное масло не проявлял признаков коррозии.
- 12. Третий опытЖелезный гвоздь погруженный в воду заржавел.
- 13. Четвертый опытЖелезный гвоздь погруженный в раствор хлорида натрия сильно заржавел
- 14. Пятый опытЖелезный гвоздь обвитый медной проволкой защитил ее от коррозии. Так как медь менее активный металл
- 15. Шестой опытЖелезный гвоздь с цинком не подвергся
- 16. Седьмой опытЖелезный гвоздь покрытый лаком не проявлял признаков коррозии
- 17. Заключение Металл служит примером прочности. Недаром,
Востребованность данной работыВостребованность данной темы заключается в том, что работа носит познавательное, воспитательное и образовательное значение в области химии и повседневной жизни. Мы провели большую подготовительную работу: поиск информации, обработку, выделение самого главного, интересного, занимательного по
Слайд 1Проектная работа
по химии
Коррозия металлов
МКОУ Бобровская СОШ №2
Выполнил ученик 9 Класса
Козлов Семён
Учитель
Слайд 2Востребованность данной работы
Востребованность данной темы заключается в том, что работа носит
познавательное, воспитательное и образовательное значение в области химии и повседневной жизни. Мы провели большую подготовительную работу: поиск информации, обработку, выделение самого главного, интересного, занимательного по данной теме. В первой части излагается теоретический материал, во второй части проводится экспериментальная работа по выяснению коррозии металлов в различных экологических условиях.
Ученик делает выводы, как можно защитить металлы от разрушения.
Ученик делает выводы, как можно защитить металлы от разрушения.
Слайд 3План работы
Общая характеристика металлов.
Теоретическая часть.
Экспериментальная работа.
Заключение.
Слайд 4Общая характеристика металлов.
Из 110 химических элементов-88 металлы.
Все металлы имеют металлические кристаллические
решетки. Она обусловила важнейшие физические свойства металлов: пластичность, электро- и теплопроводность, металлический блеск.
Слайд 5Химические свойства металлов.
Химические свойства металлов определяются слабой связью валентных электронов с
ядром атома. Атомы сравнительно легко отдают их, превращаясь при этом в положительно заряженные ионы. Поэтому металлы являются хорошими восстановителями. В этом их главное и химическое свойство.
Слайд 6Взаимодействие металлов с водными растворами солей менее активных металлов можно иллюстрировать
примером:
Fe+CuS04=FeS04+Cu
Fe+CuS04=FeS04+Cu
Слайд 7Что же такое коррозия
Наиболее распространенная проблема металлов это коррозия. Термин коррозия
происходит от латинского «corrosio», что означает разъедать, разрушать. Среда в котором металл подвергается коррозии называется коррозийной или агрессивной средой. В случае с металлами, говоря об их коррозии, имеют виду нежелательный процесс взаимодействия металла со средой. Коррозийный процесс является самопроизвольным.
Слайд 9Экспериментальная работа
Что бы изучить коррозию мы проделали экспериментальную работу.
Суть данного эксперимента
заключается в прослеживании протекания коррозии в разных средах.
Слайд 11Второй опыт
Железный гвоздь погруженный в воду и растительное масло не проявлял
признаков коррозии.
Слайд 14Пятый опыт
Железный гвоздь обвитый медной проволкой защитил ее от коррозии. Так
как медь менее активный металл
Слайд 15Шестой опыт
Железный гвоздь с цинком не подвергся коррозии
Здесь проявляется свойства протектора
Более
активный металл принимает коррозию на себя
Слайд 17Заключение
Металл служит примером прочности. Недаром, когда хотят подчеркнуть это
свойство, говорят: «Прочный как сталь». С понятием «металл» связано представление о чем-то неизменном, прочном, твердом. Но это не всегда так. Под влиянием внешней среды металлы окисляются и в результате разрушаются. Это и называется коррозией.
Все они, за исключением золота, серебра и платины, встречаются в природе в виде соединений, которые образуют минералы и горные породы. Существование металлов в свободном состоянии энергетически менее выгодно. Чтобы получить их в чистом виде, необходимо затратить энергию, в основном тепловую. Из естественного природного состояния их переводят в металлическое.
Любой коррозионный процесс является многостадийным. Защита от коррозии является одной из важнейших проблем, имеющей большое значение для народного хозяйства.
В связи с этим необходимо:
1.Изучать условия возникновения и развития коррозии;
2.Определять скорость развития процессов коррозии в различных агрессивных средах и при наличии различных сопутствующих физических факторов;
3.Определять методы применения противокоррозионных защитных покрытий, в первую очередь лакокрасочных.
Зная законы химии, сущность коррозии, можно надежно защитить металлы от разрушения. Коррозия – это природное явление, а природу надо знать, понимать, охранять и использовать ее законы в своих целях.
Любой коррозионный процесс является многостадийным. Защита от коррозии является одной из важнейших проблем, имеющей большое значение для народного хозяйства.
В связи с этим необходимо:
1.Изучать условия возникновения и развития коррозии;
2.Определять скорость развития процессов коррозии в различных агрессивных средах и при наличии различных сопутствующих физических факторов;
3.Определять методы применения противокоррозионных защитных покрытий, в первую очередь лакокрасочных.
Зная законы химии, сущность коррозии, можно надежно защитить металлы от разрушения. Коррозия – это природное явление, а природу надо знать, понимать, охранять и использовать ее законы в своих целях.