- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Кислоты, их классификация и свойства
Содержание
- 1. Кислоты, их классификация и свойства
- 2. Кислоты (по виду кислотного остатка)
- 3. Кислоты (по виду кислотного остатка)мкислотный остатокне содержит кислородабескислородные
- 4. Кислоты (по виду кислотного остатка)мкислотный остатокне содержит кислородабескислородныемкислородосодержащие кислотный остаток содержит кислород
- 5. Кислоты (по виду кислотного остатка)мкислотный остатокне содержит
- 6. Кислоты (по виду кислотного остатка)мкислотный остатокне содержит
- 7. Кислоты (по заряду кислотных остатков)
- 8. одноосновныеКислоты (по заряду кислотных остатков)
- 9. одноосновныедвухосновныеКислоты (по заряду кислотных остатков)
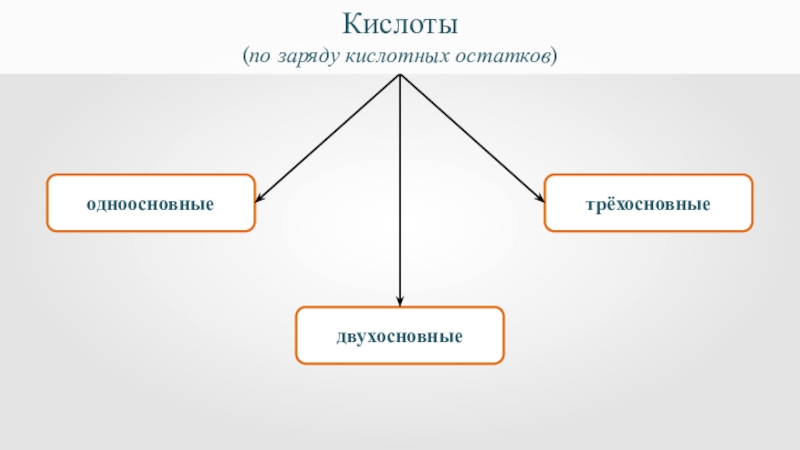
- 10. одноосновныедвухосновныетрёхосновныеКислоты (по заряду кислотных остатков)
- 11. Одноосновные кислотыЗаряд кислотного остатка -1, который соответственно соединяется с одним атомом водорода.
- 12. Одноосновные кислотыЗаряд кислотного остатка -1, который соответственно
- 13. Двухосновные кислотыЗаряд кислотного остатка -2, который соответственно соединяется с двумя атомами водорода.
- 14. Двухосновные кислотыЗаряд кислотного остатка -2, который соответственно
- 15. Трёхосновные кислотыЗаряд кислотного остатка -3, который соответственно соединяется с тремя атомами водорода.
- 16. Трёхосновные кислотыЗаряд кислотного остатка -3, который соответственно соединяется с тремя атомами водорода.H3PO4 — фосфорная кислота.
- 17. Кислоты (по растворимости в воде)
- 18. растворимыеКислоты (по растворимости в воде)
- 19. растворимыенерастворимыеКислоты (по растворимости в воде)
- 20. растворимыенерастворимыеКислоты (по растворимости в воде)Сернистая кислота (H2SO3) и угольная кислота (H2CO3) существуют только в водных растворах.
- 21. Растворимые кислоты:H2SO4 — серная кислота,H2S — сероводородная кислота,HNO3 — азотная кислота.Кислоты (по растворимости в воде)
- 22. Растворимые кислоты:H2SO4 — серная кислота,H2S — сероводородная
- 23. Кислоты (летучесть)
- 24. Кислоты (летучесть)летучие
- 25. Кислоты (летучесть)летучиенелетучие
- 26. Кислоты (летучесть)летучиенелетучиеH2S — сероводородная кислота,HCl — хлороводородная
- 27. Кислоты (летучесть)летучиенелетучиеH2S — сероводородная кислота,HCl — хлороводородная
- 28. Кислоты (по степени электролитической диссоциации )
- 29. Кислоты (по степени электролитической диссоциации )сильные
- 30. Кислоты (по степени электролитической диссоциации )сильныеслабые
- 31. Кислоты (по степени электролитической диссоциации )сильныеслабыеH2SO4 —
- 32. Кислоты (по степени электролитической диссоциации )сильныеслабыеH2SO4 —
- 33. Стабильность кислоты — это степень устойчивости её состава при обычных условиях.
- 34. Кислоты (по стабильности )
- 35. Кислоты (по стабильности )стабильные
- 36. Кислоты (по стабильности )стабильныенестабильные
- 37. Кислоты (по стабильности )стабильныенестабильныеH2SO4 — серная кислота,H3PO4
- 38. Кислоты (по стабильности )стабильныенестабильныеH2SO4 — серная кислота,H3PO4
- 39. Кислоты (по агрегатному состоянию)твёрдыекремниевая кислота (H2SiO3)Майя Пчёлка
- 40. Кислоты (по агрегатному состоянию)твёрдыекремниевая кислота (H2SiO3)Майя Пчёлкажидкиесерная кислота (H2SO4)
- 41. Кислоты (по агрегатному состоянию)твёрдыекремниевая кислота (H2SiO3)Майя Пчёлкажидкиесерная кислота (H2SO4)хлороводородная кислота (HCl)газообразные
- 42. Газообразные кислоты (HCl, HBr, H2S) при обычных условиях могут существовать в водных растворах.
- 43. Слабые кислоты(H2SO3, H2CO3 ) легко разлагаются на газ и воду, существуют тольков водных растворах.молекула угольной кислоты
- 44. Летучесть — это способность кислоты испаряться при
- 45. Большинство кислот не имеют окраски. Только хромовая
- 46. Кислоты классифицируются в зависимости от их свойств,
Слайд 1
Кислоты — это сложные вещества, молекулы которых состоят из атомов водорода
Слайд 4
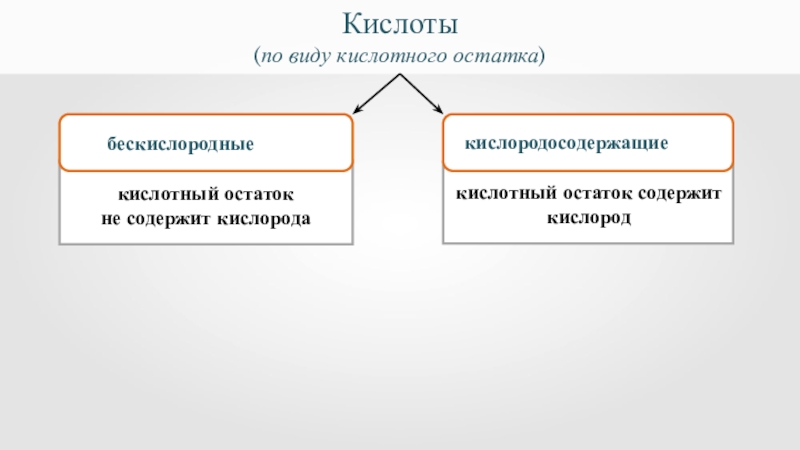
Кислоты
(по виду кислотного остатка)
м
кислотный остаток
не содержит кислорода
бескислородные
м
кислородосодержащие
кислотный остаток содержит
Слайд 5
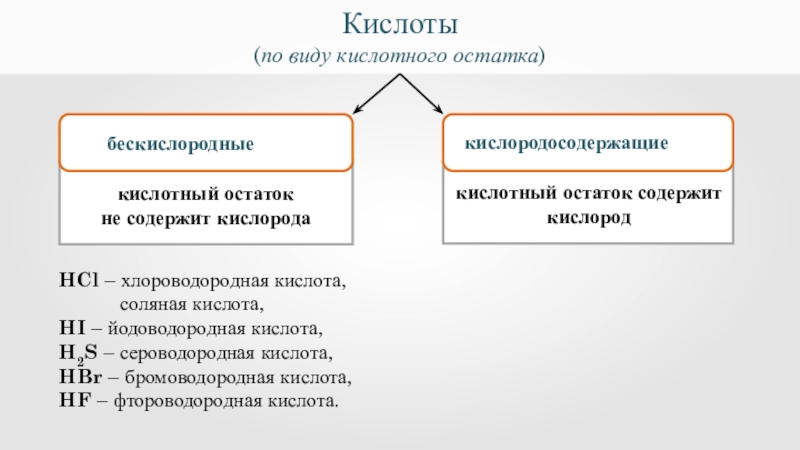
Кислоты
(по виду кислотного остатка)
м
кислотный остаток
не содержит кислорода
бескислородные
м
кислородосодержащие
кислотный остаток содержит
HCl – хлороводородная кислота,
соляная кислота,
HI – йодоводородная кислота,
H2S – сероводородная кислота,
HBr – бромоводородная кислота,
HF – фтороводородная кислота.
Слайд 6
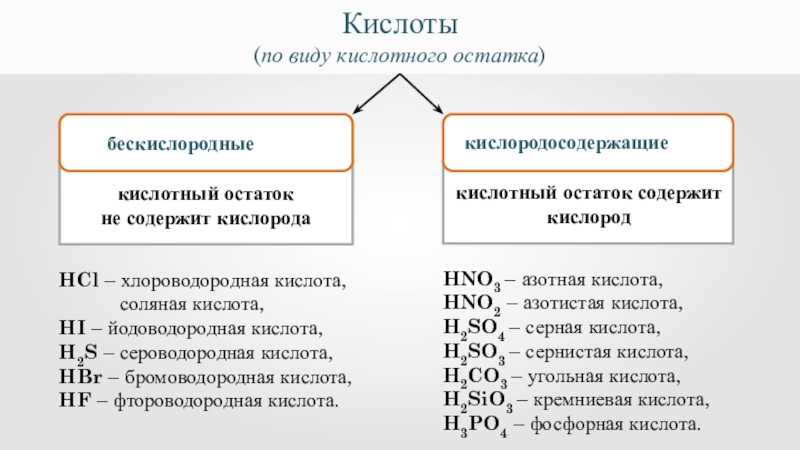
Кислоты
(по виду кислотного остатка)
м
кислотный остаток
не содержит кислорода
бескислородные
м
кислородосодержащие
кислотный остаток содержит
HCl – хлороводородная кислота,
соляная кислота,
HI – йодоводородная кислота,
H2S – сероводородная кислота,
HBr – бромоводородная кислота,
HF – фтороводородная кислота.
HNO3 – азотная кислота,
HNO2 – азотистая кислота,
H2SO4 – серная кислота,
H2SO3 – сернистая кислота,
H2CO3 – угольная кислота,
H2SiO3 – кремниевая кислота,
H3PO4 – фосфорная кислота.
Слайд 11
Одноосновные кислоты
Заряд кислотного остатка -1, который соответственно соединяется с одним атомом
Слайд 12
Одноосновные кислоты
Заряд кислотного остатка -1, который соответственно соединяется с одним атомом
HCl — cоляная кислота,
HNO3 — азотная кислота.
Слайд 13
Двухосновные кислоты
Заряд кислотного остатка -2, который соответственно соединяется с двумя атомами
Слайд 14
Двухосновные кислоты
Заряд кислотного остатка -2, который соответственно соединяется с двумя атомами
H2SO4 — серная кислота,
H2CO3 — угольная кислота.
Слайд 15
Трёхосновные кислоты
Заряд кислотного остатка -3, который соответственно соединяется с тремя атомами
Слайд 16
Трёхосновные кислоты
Заряд кислотного остатка -3, который соответственно соединяется с тремя атомами
H3PO4 — фосфорная кислота.
Слайд 20растворимые
нерастворимые
Кислоты
(по растворимости в воде)
Сернистая кислота (H2SO3) и угольная кислота (H2CO3)
Слайд 21Растворимые кислоты:
H2SO4 — серная кислота,
H2S — сероводородная кислота,
HNO3 — азотная кислота.
Кислоты
(по растворимости в воде)
Слайд 22Растворимые кислоты:
H2SO4 — серная кислота,
H2S — сероводородная кислота,
HNO3 — азотная кислота.
Кислоты
(по растворимости в воде)
Нерастворимые:
H2SiO3 — кремниевая кислота.
Слайд 26
Кислоты
(летучесть)
летучие
нелетучие
H2S — сероводородная кислота,
HCl — хлороводородная кислота,
HNO3 — азотная кислота.
Слайд 27
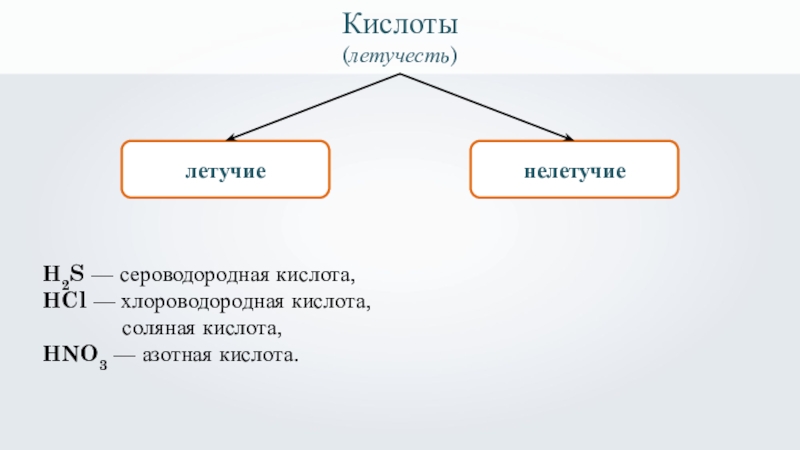
Кислоты
(летучесть)
летучие
нелетучие
H2S — сероводородная кислота,
HCl — хлороводородная кислота,
HNO3 — азотная кислота.
H2SO4 — серная кислота,
H2SiO3 — кремниевая кислота,
H3PO4 — фосфорная кислота.
Слайд 31
Кислоты
(по степени электролитической диссоциации )
сильные
слабые
H2SO4 — серная кислота,
HCl — хлороводородная
соляная кислота,
HNO3 — азотная кислота.
Слайд 32
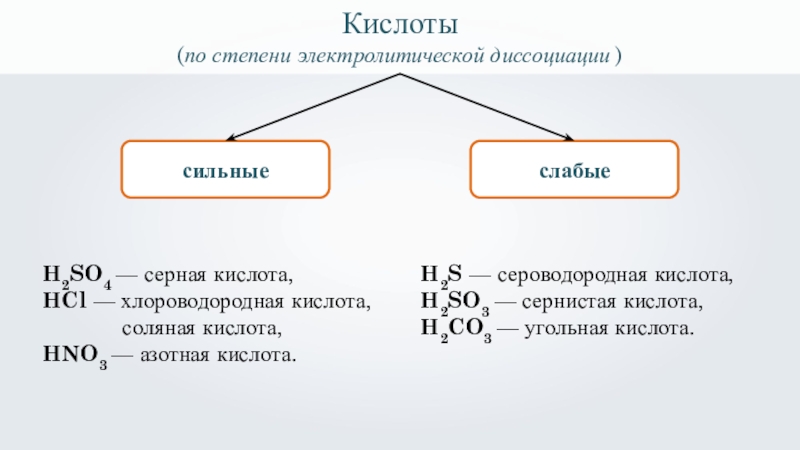
Кислоты
(по степени электролитической диссоциации )
сильные
слабые
H2SO4 — серная кислота,
HCl — хлороводородная
соляная кислота,
HNO3 — азотная кислота.
H2S — сероводородная кислота,
H2SO3 — сернистая кислота,
H2CO3 — угольная кислота.
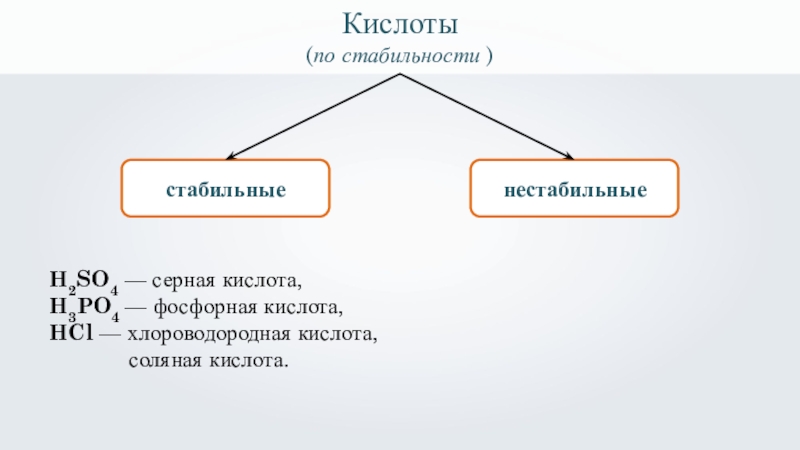
Слайд 37
Кислоты
(по стабильности )
стабильные
нестабильные
H2SO4 — серная кислота,
H3PO4 — фосфорная кислота,
HCl —
соляная кислота.
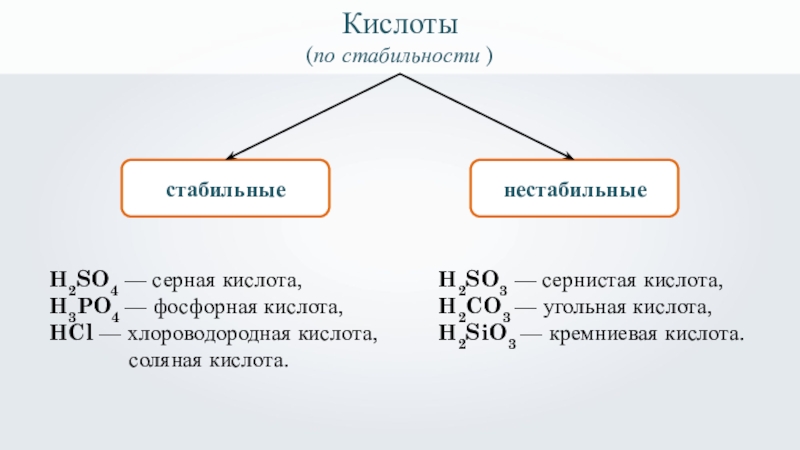
Слайд 38
Кислоты
(по стабильности )
стабильные
нестабильные
H2SO4 — серная кислота,
H3PO4 — фосфорная кислота,
HCl —
соляная кислота.
H2SO3 — сернистая кислота,
H2CO3 — угольная кислота,
H2SiO3 — кремниевая кислота.
Слайд 40
Кислоты
(по агрегатному состоянию)
твёрдые
кремниевая кислота (H2SiO3)
Майя Пчёлка
жидкие
серная кислота (H2SO4)
Слайд 41
Кислоты
(по агрегатному состоянию)
твёрдые
кремниевая кислота (H2SiO3)
Майя Пчёлка
жидкие
серная кислота (H2SO4)
хлороводородная кислота (HCl)
газообразные
Слайд 42
Газообразные кислоты (HCl, HBr, H2S) при обычных условиях могут существовать в
Слайд 43
Слабые кислоты
(H2SO3, H2CO3 ) легко разлагаются на газ и воду, существуют
в водных растворах.
молекула угольной кислоты
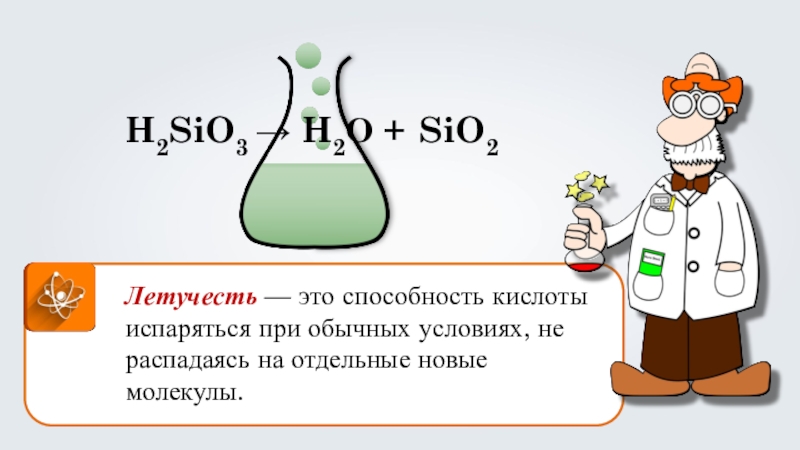
Слайд 44
Летучесть — это способность кислоты испаряться при обычных условиях, не распадаясь
H2SiO3 → H2О + SiO2
Слайд 45Большинство кислот не имеют окраски. Только хромовая кислота (H2CrO4) имеет жёлтую
Слайд 46
Кислоты классифицируются в зависимости от их свойств, но все они объединены
Катионы водорода, входящие в кислоты, обуславливают их общие свойства:
кислый вкус, изменение окраски индикаторов и взаимодействие с другими веществами.