и свойства
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Кислоты, их классификация и свойства
Содержание
- 1. Кислоты, их классификация и свойства
- 2. Понятие кислотыКислоты как класс химических соединений, обладающих
- 3. Кислоты
- 4. Кислоты
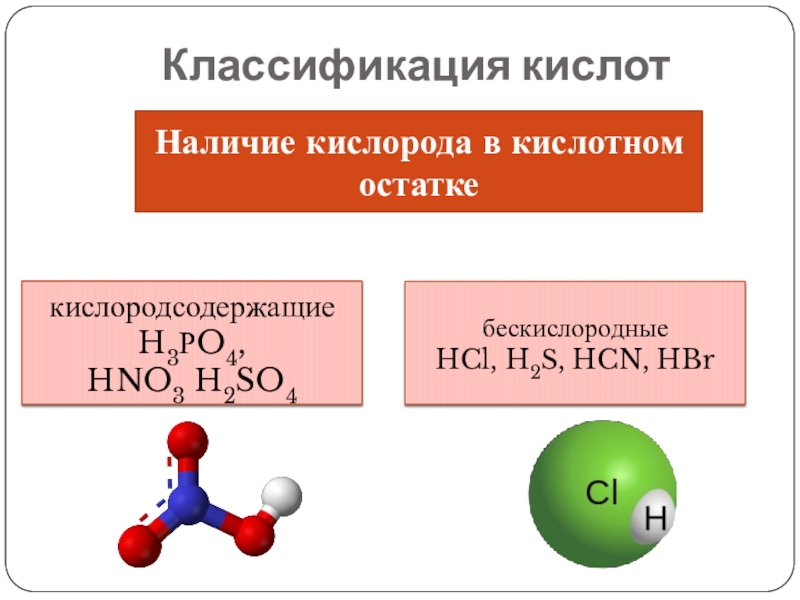
- 5. Классификация кислотНаличие кислорода в кислотном остаткекислородсодержащие H3РO4, HNO3 H2SO4бескислородные HCl, H2S, HCN, HBr
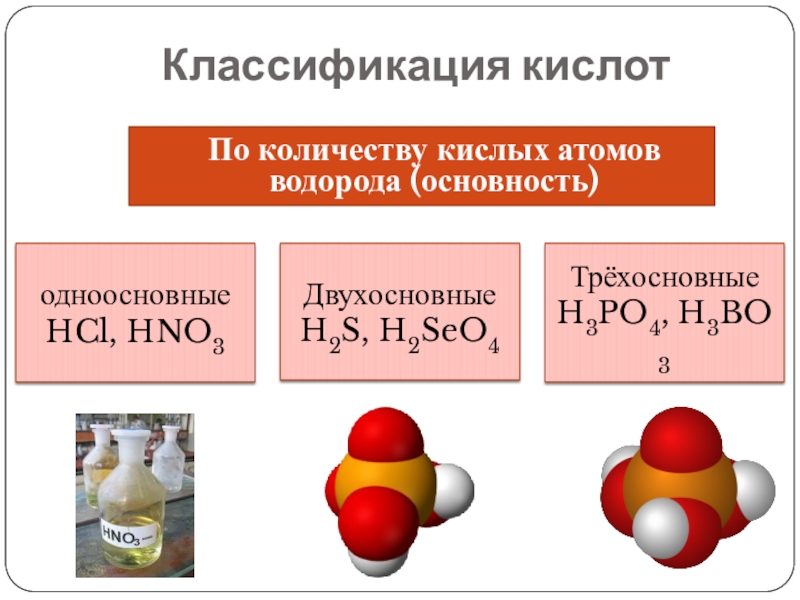
- 6. Классификация кислотПо количеству кислых атомов водорода (основность)одноосновные HCl, HNO3ДвухосновныеH2S, H2SeO4ТрёхосновныеH3PO4, H3BO3
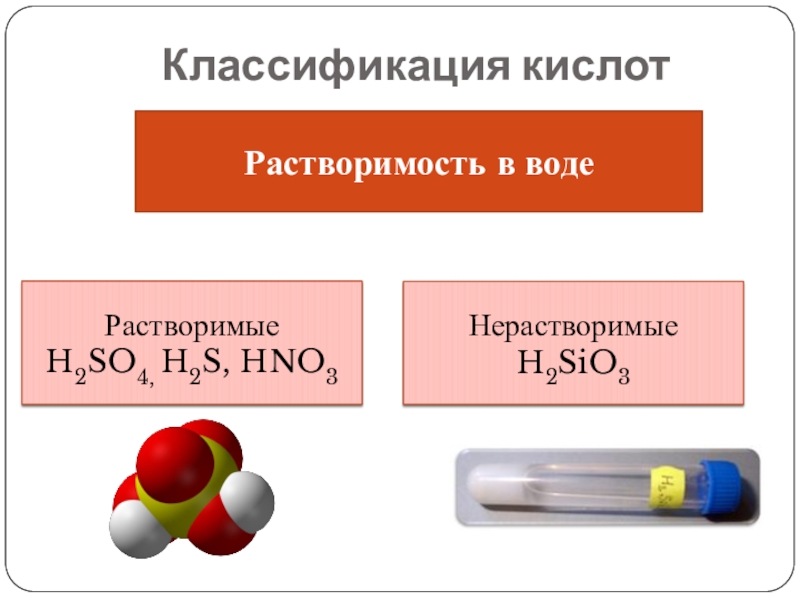
- 7. Классификация кислотРастворимость в водеРастворимыеH2SO4, H2S, HNO3НерастворимыеH2SiO3
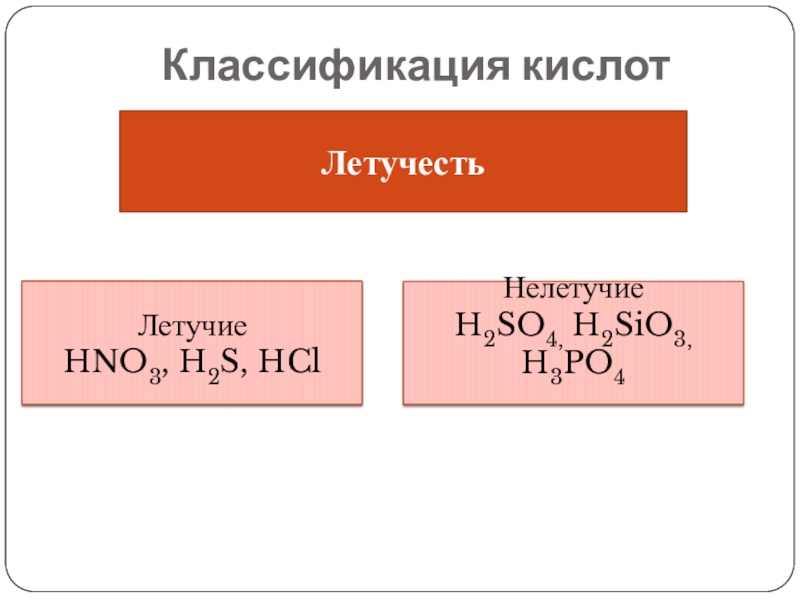
- 8. Классификация кислотЛетучестьЛетучие HNO3, H2S, HClНелетучие H2SO4, H2SiO3, H3PO4
- 9. Классификация кислотСтепень электрической диссоциации (по силе)Сильные — диссоциируют
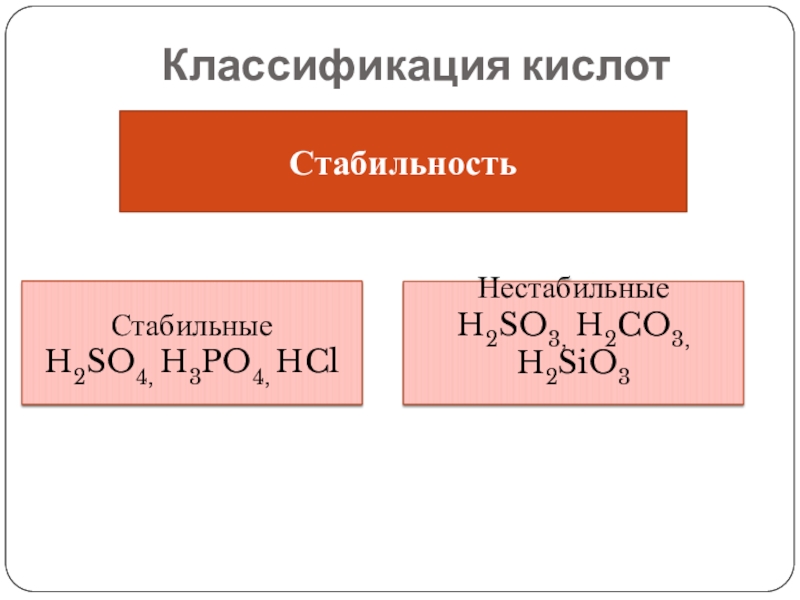
- 10. Классификация кислотСтабильностьСтабильные H2SO4, H3PO4, HCl НестабильныеH2SO3, H2CO3, H2SiO3
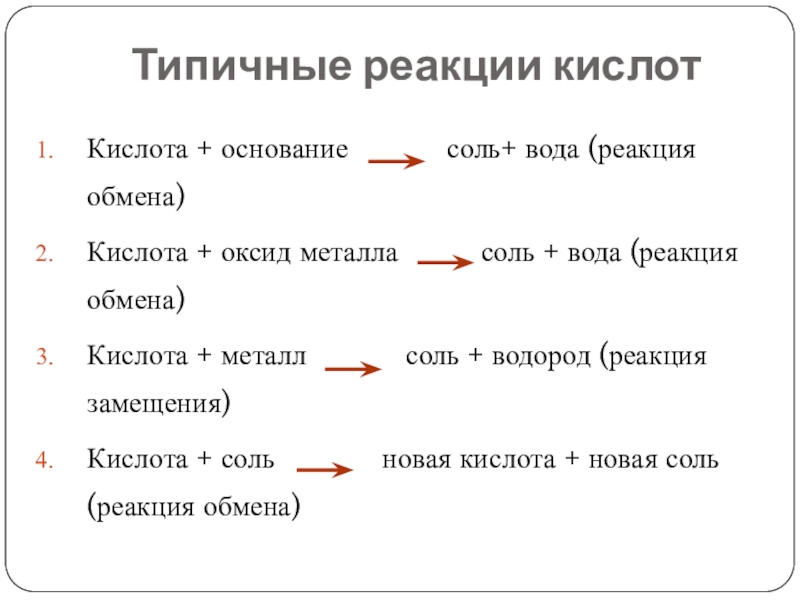
- 11. Типичные реакции кислотКислота + основание
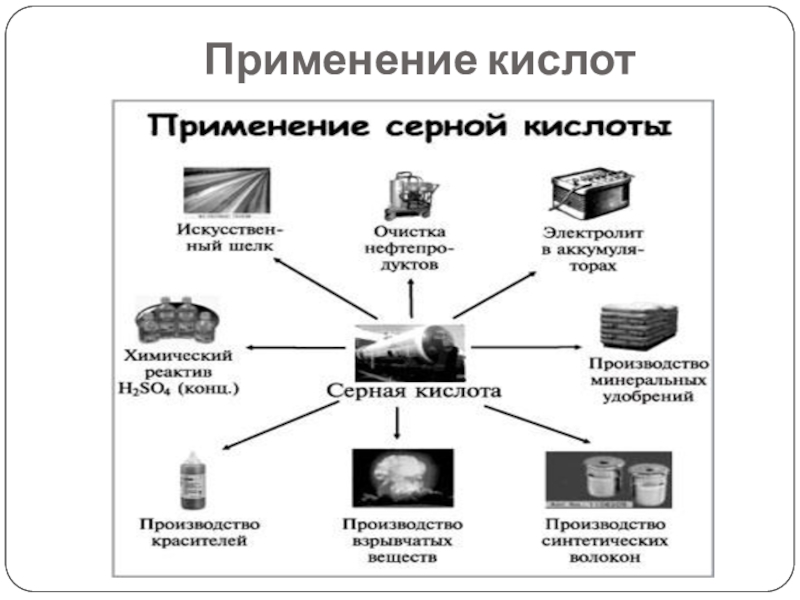
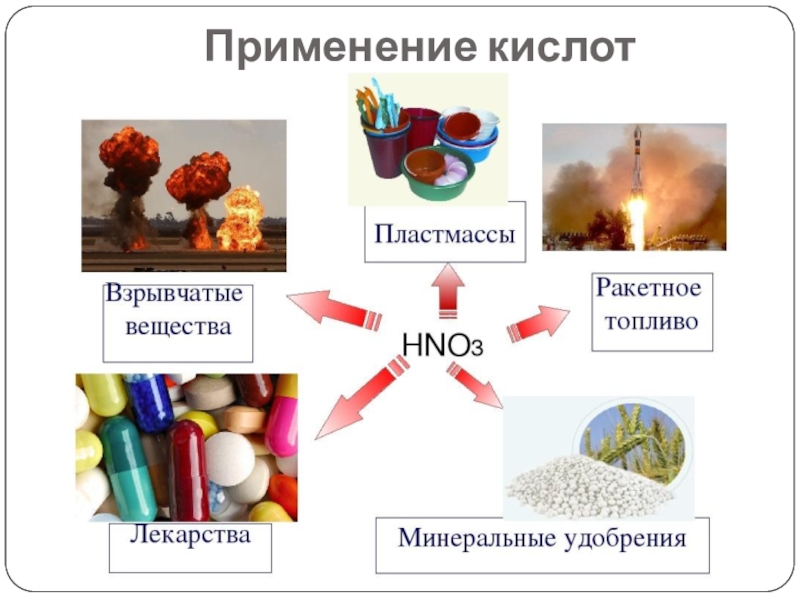
- 12. Применение кислот
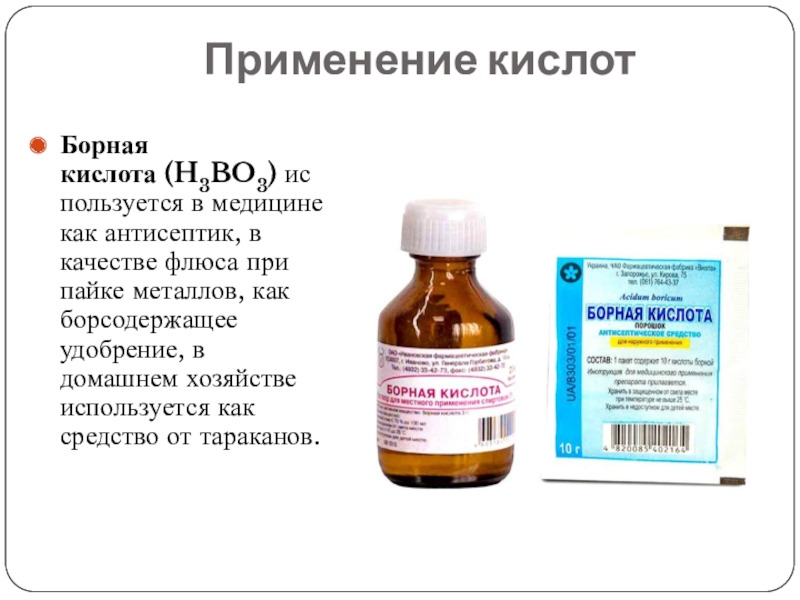
- 13. Применение кислотБорная кислота (H3BO3) используется в медицине как антисептик,
- 14. Применение кислотШироко известны в домашнем использовании при выпечке уксусная и лимонная кислоты. Также в быту их используют для удаления накипи.
- 15. Применение кислотЗнакомая всем с детства аскорбиновая кислота, более
- 16. Применение кислот
- 17. Закрепление нового материала1. Формула двухосновной кислородосодержащей кислоты
Понятие кислотыКислоты как класс химических соединений, обладающих рядом близких свойств, известны с древнейших времён.Кислоты (неорганические, минеральные) — это сложные соединения состоящие из катиона водорода (H+) и аниона кислотного остатка(SO32-, SO42-, NO3— и т.д).
Слайд 2Понятие кислоты
Кислоты как класс химических соединений, обладающих рядом близких свойств, известны
с древнейших времён.
Кислоты (неорганические, минеральные) — это сложные соединения состоящие из катиона водорода (H+) и аниона кислотного остатка(SO32-, SO42-, NO3— и т.д).
Кислоты (неорганические, минеральные) — это сложные соединения состоящие из катиона водорода (H+) и аниона кислотного остатка(SO32-, SO42-, NO3— и т.д).
Слайд 5Классификация кислот
Наличие кислорода в кислотном остатке
кислородсодержащие
H3РO4, HNO3 H2SO4
бескислородные HCl, H2S, HCN, HBr
Слайд 6Классификация кислот
По количеству кислых атомов водорода (основность)
одноосновные
HCl, HNO3
Двухосновные
H2S, H2SeO4
Трёхосновные
H3PO4, H3BO3
Слайд 9Классификация кислот
Степень электрической диссоциации (по силе)
Сильные — диссоциируют практически полностью, константы диссоциации больше 1⋅10−3
HNO3,
H2SO4, HCl
Слабые — константа диссоциации меньше 1⋅10−3 (уксусная кислота Kд= 1,7⋅10−5).
H2S, , H2SO3, , H2CO3
Слайд 10Классификация кислот
Стабильность
Стабильные
H2SO4, H3PO4, HCl
Нестабильные
H2SO3, H2CO3, H2SiO3
Слайд 11Типичные реакции кислот
Кислота + основание соль+
вода (реакция обмена)
Кислота + оксид металла соль + вода (реакция обмена)
Кислота + металл соль + водород (реакция замещения)
Кислота + соль новая кислота + новая соль (реакция обмена)
Кислота + оксид металла соль + вода (реакция обмена)
Кислота + металл соль + водород (реакция замещения)
Кислота + соль новая кислота + новая соль (реакция обмена)
Слайд 13Применение кислот
Борная кислота (H3BO3) используется в медицине как антисептик, в качестве флюса при
пайке металлов, как борсодержащее удобрение, в домашнем хозяйстве используется как средство от тараканов.
Слайд 14Применение кислот
Широко известны в домашнем использовании при выпечке уксусная и лимонная кислоты. Также в быту
их используют для удаления накипи.
Слайд 15Применение кислот
Знакомая всем с детства аскорбиновая кислота, более известная в народе как витамин
С, применяется при лечении простудных заболеваний.
Слайд 17Закрепление нового материала
1. Формула двухосновной кислородосодержащей кислоты
а) H2SO4
б) HCl в) HNO3 г) H3PO4
2) Ряд формул, в котором все вещества – кислоты
а) HCl, CaCl2, H2SO4 б) NaOH, H2S, H2CO3
в) HI, P2O5, H3PO4 г) HNO2, HCl, HF
3) Формула двухосновной бескислородной кислоты
а) H2S б) HCl в) HNO3 г) H3PO4
4) Кислота – слабый электролит
а) азотная б) соляная в) серная г) сернистая
2) Ряд формул, в котором все вещества – кислоты
а) HCl, CaCl2, H2SO4 б) NaOH, H2S, H2CO3
в) HI, P2O5, H3PO4 г) HNO2, HCl, HF
3) Формула двухосновной бескислородной кислоты
а) H2S б) HCl в) HNO3 г) H3PO4
4) Кислота – слабый электролит
а) азотная б) соляная в) серная г) сернистая