- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Исследовательская работа учащихся по теме Сравнительная характеристика адсорбционных свойств различных веществ
Содержание
- 1. Исследовательская работа учащихся по теме Сравнительная характеристика адсорбционных свойств различных веществ
- 2. Актуальность темы Адсорбционные явления чрезвычайно
- 3. Что такое адсорбция? Какие вещества называются адсорбентами?
- 4. Цель работы: Изучение характеристик адсорбционных свойств различных веществ
- 5. Задачи исследования:Изучить сущность процесса адсорбции, её классификацию
- 6. Гипотеза исследования: Если предложенные вещества являются адсорбентами, то они обладают различными адсорбционными способностями
- 7. Объект исследования: АдсорбентыПредмет исследования: Адсорбция и десорбция
- 8. Странная болезнь Ньютона
- 9. Версия отравления Наполеона
- 10. Из историиТ.Е. Ловиц в 1785 году открыл
- 11. Что же такое адсорбция?Адсорбция – это процесс
- 12. Адсорбирующееся вещество – адсорбатАдсорбирующее вещество - адсорбентУгольДревесные опилкиУксусПоглотительПоглощаемое вещество
- 13. Классификация адсорбции АдсорбцияФизическаяХимическая (хемосорбция)Молекулы сохраняют свою
- 14. Механизм адсорбции У твердого тела отдельные его
- 15. Что же такое десорбция?Десорбция - это обратный
- 16. Практическая часть
- 17. О п ы т 1. «Избирательная адсорбция
- 18. О п ы т 2. «Поглощение запаха различными адсорбентами»
- 19. О п ы т 2. «Поглощение
- 20. Иллюстрации к опыту №2
- 21. О п ы т 3. «Обесцвечивание растворов бриллиантового зеленого и йода активированным углем»
- 22. О п ы т 3. «Обесцвечивание
- 23. Иллюстрации к опыту №3
- 24. О п ы т 4. «Поглощение воды
- 25. О п ы т 4. «Поглощение воды
- 26. Иллюстрации к опыту №4Силикагель без водыСиликагель в виде гранулСиликагель в виде порошка
- 27. О п ы т 5. «Обесцвечивание раствора бриллиантового зеленого различными адсорбентами»Спустя 30 минутСпустя сутки
- 28. О п ы т 5. «Обесцвечивание раствора
- 29. Иллюстрации к опыту №5Спустя 30 минутСпустя сутки
- 30. О п ы т 6. «Обесцвечивание раствора бриллиантового зеленого различными адсорбатами»В момент добавления активированного угляСпустя сутки
- 31. О п ы т 6. «Обесцвечивание раствора
- 32. Иллюстрации к опыту №6В момент добавления активированного угляСпустя сутки
- 33. Практическое значение адсорбции При помощи различных твердых
- 34. Практическое значение адсорбцииНа этом свойстве основано использование
- 35. Выводы:Адсорбционные явления чрезвычайно широко распространены в живой
- 36. Информационные источники:Грег С., Синг К. Адсорбция, удельная
- 37. Информационные источники:http://www.xumuk.ru/encyklopedia/43.htmlhttp://www.chemport.ru/data/chemipedia/article_35.htmlhttp://traditio-ru.org/wiki/Адсорбцияhttp://allforchildren.ru/sci/sci016.phphttp://www.diagram.com.ua/tests/himija/himija006.shtmlhttp://www.ngpedia.ru/id564837p1.htmlhttp://www.ngpedia.ru/id217095p1.htmlhttp://humbio.ru/humbio/tarantul_sl/000000de.htm
- 38. Спасибо за внимание!
Слайд 2Актуальность темы
Адсорбционные явления чрезвычайно широко распространены в живой
Слайд 3Что такое адсорбция? Какие вещества называются адсорбентами? Какие вещества обладают высокой
Как используется это явление в быту и промышленности?
Слайд 5Задачи исследования:
Изучить сущность процесса адсорбции, её классификацию и механизм её проявления
Сравнить
Ознакомиться с использованием данного явления в быту и промышленности
Слайд 6Гипотеза исследования:
Если предложенные вещества являются адсорбентами, то они
Слайд 7Объект исследования: Адсорбенты
Предмет исследования: Адсорбция и десорбция веществ
В ходе исследования была
Слайд 10Из истории
Т.Е. Ловиц в 1785 году открыл явление адсорбции углем в
Товий Егорович Ловиц
Слайд 11Что же такое адсорбция?
Адсорбция – это процесс поглощения вещества из раствора
Слайд 12Адсорбирующееся вещество – адсорбат
Адсорбирующее вещество - адсорбент
Уголь
Древесные опилки
Уксус
Поглотитель
Поглощаемое вещество
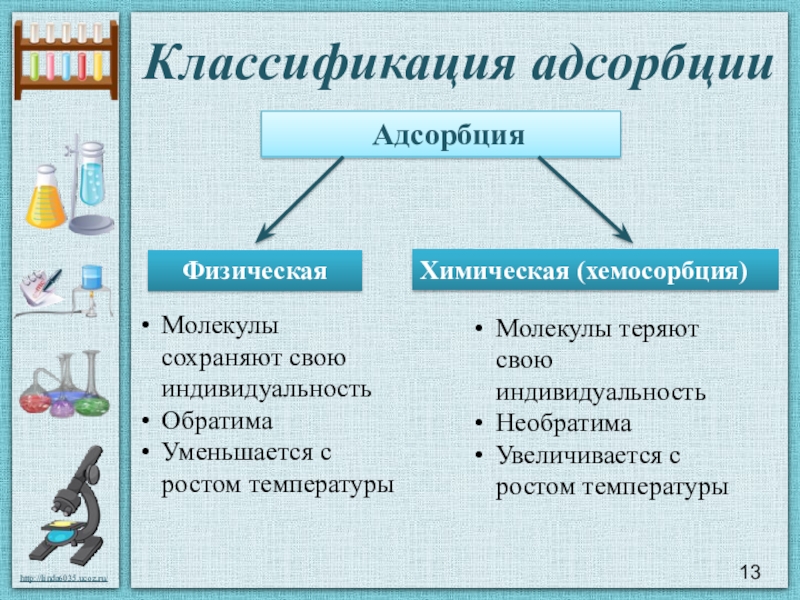
Слайд 13Классификация адсорбции
Адсорбция
Физическая
Химическая (хемосорбция)
Молекулы сохраняют свою индивидуальность
Обратима
Уменьшается с ростом температуры
Молекулы теряют
Необратима
Увеличивается с ростом температуры
Слайд 14Механизм адсорбции
У твердого тела отдельные его частицы расположены в определенном
Частица А окружена другими такими же частицами равномерно со всех сторон.
Силовое поле частицы Б с внешней стороны не компенсировано. На поверхности остается свободное силовое поле, за счет которого к твердому телу и могут притягиваться частицы тех или других веществ из соприкасающегося с ним газа или раствора.
Слайд 15Что же такое десорбция?
Десорбция - это обратный процесс адсорбции. Она происходит
Адсорбция
Десорбция
Слайд 17О п ы т 1.
«Избирательная адсорбция газов активированным углем»
Оборудование и реактивы:
Ход работы:
Cu + 4HNO3 (конц.) = Cu(NO3)2 + 2H2O + 2NO2
Вывод: Активированный уголь – обладает избирательной адсорбционной способностью газов.
Слайд 19О п ы т 2.
«Поглощение запаха различными адсорбентами»
Вывод: Лучшим адсорбентом являются кукурузные палочки.
Слайд 22О п ы т 3. «Обесцвечивание растворов бриллиантового зеленого и йода
Оборудование и реактивы: Пробирка (2 шт.), раствор бриллиантового зеленого, раствор йода, активированный уголь (2 шт.), вода.
Ход работы: В одну из пробирок добавили каплю йода, в другую – «зеленки». Затем поместили по таблетке в каждую пробирку и наблюдали явление адсорбции. Спустя 5 минут йод полностью обесцветился, а «зеленка» только спустя сутки.
Вывод: Лучшим адсорбатом является йод.
Слайд 24О п ы т 4.
«Поглощение воды силикагелем»
Силикагель без воды
Силикагель в виде
Силикагель в виде порошка
Слайд 25О п ы т 4.
«Поглощение воды силикагелем»
Оборудование и реактивы: силикагель в
Слайд 27О п ы т 5.
«Обесцвечивание раствора бриллиантового зеленого различными адсорбентами»
Спустя 30
Спустя сутки
Слайд 28О п ы т 5.
«Обесцвечивание раствора бриллиантового зеленого различными адсорбентами»
Слайд 30О п ы т 6.
«Обесцвечивание раствора бриллиантового зеленого различными адсорбатами»
В момент
Спустя сутки
Слайд 31О п ы т 6.
«Обесцвечивание раствора бриллиантового зеленого различными адсорбатами»
Слайд 33Практическое значение адсорбции
При помощи различных твердых адсорбентов производится улавливанье ценных паров
Адсорбцией извлекают малые количества веществ, растворенных в больших объемах жидкости.
Используются при крашении волокон, при обогащении полезных ископаемых. Ионообменная адсорбция нашла широкие применения в пищевой промышленности.
Слайд 34Практическое значение адсорбции
На этом свойстве основано использование активированного угля в противогазах.
Слайд 35Выводы:
Адсорбционные явления чрезвычайно широко распространены в живой и неживой природе.
Адсорбция
В зависимости от природы адсорбционных сил различают физическую и химическую адсорбцию (хемосорбция).
Различные вещества обладают различными адсорбционными способностями, что и показали результаты проделанных опытов.
Слайд 36Информационные источники:
Грег С., Синг К. Адсорбция, удельная поверхность, пористость. М.: Мир,
Кельцев Н.В. Основы адсорбционной техники. М.: Химия, 1984. 592с.
Киселев А.В. Межмолекулярные взаимодействия в адсорбции и хроматографии. М.: Высш. шк., 1986;
Романков П.Г., Лепилин В.Н. Непрерывная адсорбция паров и газов. - Л.: Химия, 1968. - 228 с.
Стефан Брунауэр. Адсорбция газов и паров, том I, Физическая адсорбция, пер. с англ. Под редакцией М.М. Дубинина. - М.: ИЛ, 1948. - 783 с.