- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Химия пәні бойынша презентация Химиялық тепе -теңдік
Содержание
- 1. Химия пәні бойынша презентация Химиялық тепе -теңдік
- 2. Слайд 2
- 3. а А + b В ↔ с
- 4. Ле -Шателье принципі химиялық тепе –теңдікте тұрған
- 5. Тепе- теңдікке сер етуші фактор - ҚЫСЫМN2
- 6. Гистограмма влияния давления на молярную долю азота,
- 7. Слайд 7
- 8. ҚЫСЫМР ↑, көлемі аз бағытқа ығысадыР ↓, көлемі көп бағытқа ығысады
- 9. Төмендегі реакцияда қысымды азайтқанда реакция бағыты қай
- 10. Тепе- теңдікке сер етуші фактор - ТЕМПЕРАТУРАN2
- 11. Влияние температуры на содержание реагирующих веществ и
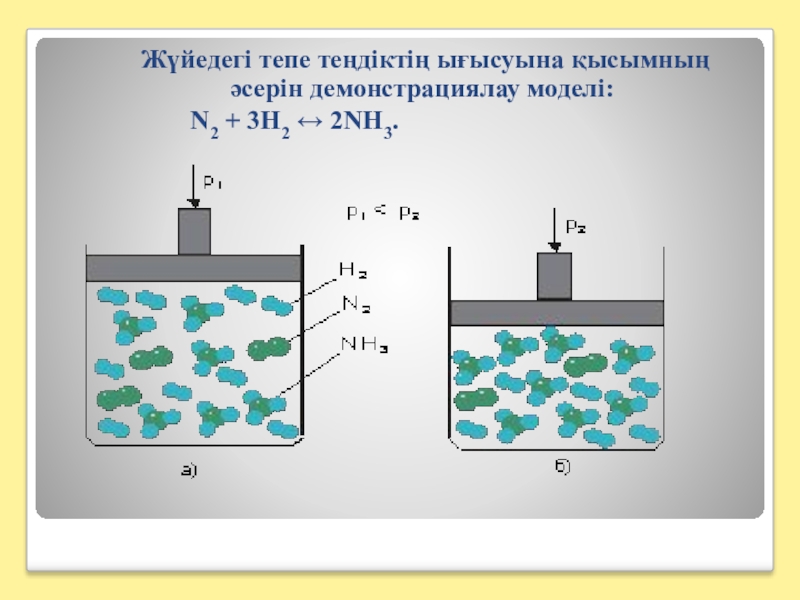
- 12. Жүйедегі тепе теңдіктің ығысуына
- 13. ТЕМПЕРАТУРА t↑, эндотермиялық реакция бағытына ығысады t↓, экзотермиялық реакция бағытына ығысады
- 14. Слайд 14
- 15. КОНЦЕНТРАЦИЯ Реагенттердің концентрациясын ↑, өнімдер түзілу жағына Өнімдер концентрациясын ↑, реагенттер түзілу жағына
- 16. Тепе- теңдікке катализатор әсері
- 17. Слайд 17
- 18. Слайд 18
- 19. Слайд 19
- 20. Назарларыңызға рахмет!!!
Слайд 2
1) NaOH + HCl → NaCl + H2O;
2) H2 + I2 → 2HI;
3) C + O2 → CO2;
4) CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
5) N2 + 3H2 → 2NH3
6) С6Н12 → С6Н6 + 3Н2
Қайтымды реакцияларды анықта?
Слайд 3а А + b В ↔ с С + d D,
Тура және кері реакциялардың жылдамдығы теңескен жүйе күйін химиялық тепе –теңдік деп атайды
Слайд 4Ле -Шателье принципі
химиялық тепе –теңдікте тұрған жүйе күйіне сыртқы факторлардың
Анри Луи Ле Шателье (1850–1936)
Слайд 5Тепе- теңдікке сер етуші фактор - ҚЫСЫМ
N2 + 3H2
1көлем 3 көлем 2 көлем
4 көлем > 2 көлем
Слайд 6Гистограмма влияния давления на молярную долю азота, водорода и аммиака
Влияние давления
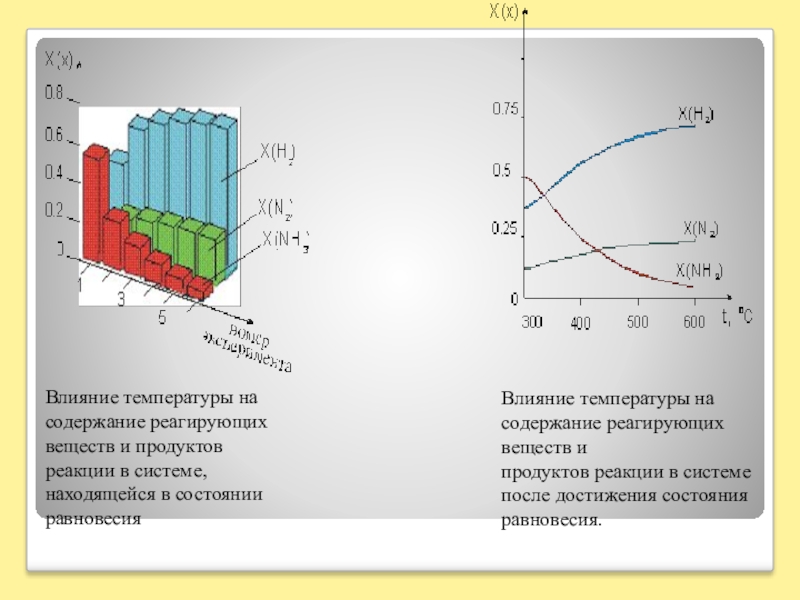
Слайд 11Влияние температуры на содержание реагирующих веществ и продуктов реакции в системе,
Влияние температуры на содержание реагирующих веществ и
продуктов реакции в системе после достижения состояния равновесия.
Слайд 12 Жүйедегі тепе теңдіктің ығысуына температураның әсерін демонстрациялау моделі:
Слайд 13ТЕМПЕРАТУРА
t↑, эндотермиялық реакция бағытына ығысады
t↓, экзотермиялық реакция бағытына ығысады
Слайд 15КОНЦЕНТРАЦИЯ
Реагенттердің концентрациясын ↑, өнімдер түзілу жағына
Өнімдер концентрациясын ↑, реагенттер
Слайд 16 Тепе- теңдікке катализатор әсері
Катализатор бірдей дәрежеде тура және кері реакциялардың жылдамдығын арттырады.
Бірақ тепе- теңдіктің ығысуына әсер етпейді