- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Химические свойства и применение кислорода. Оксиды. Круговорот кислорода в природе
Содержание
- 1. Химические свойства и применение кислорода. Оксиды. Круговорот кислорода в природе
- 2. Установите соответствие между способом получения кислорода и уравнением химической реакцией.
- 3. Ответ: А-4; Б-2; В-1; Г-5; Д-3.
- 4. Химические свойства - это совокупность химических реакций в которые вступает вещество
- 5. Химические свойства кислорода2. Сера, S1. Фосфор, РПорошок
- 6. Химические свойства кислородаГорение фосфораГорение серыГорение угляГорение железаГорение метана
- 7. Реакции окисления - - реакции взаимодействия веществ с кислородом с выделением тепла и света (реакции горения)
- 8. Оксиды – сложные вещества состоящие из атомов двух химических элементов, один из которых кислород
- 9. 1. В ряду формул веществ выберите
- 10. ВзаимопроверкаMgO CO2 NOSO2 Al2O3 ZnO2Mg + O2
- 11. Для кислорода верны следующие утверждения:а) Кислород –
- 12. Ответ: а; в; е.
- 13. Домашнее задание§
- 14. Спасибо за внимание
Слайд 2 Установите соответствие между способом получения кислорода и уравнением химической реакцией.
Слайд 5Химические свойства кислорода
2. Сера, S
1. Фосфор, Р
Порошок красного цвета
P + O2
4
5
2
P2O5 – оксид фосфора (V)
Белый дым
Порошок желтого цвета
S+ O2 = SO2
SO2 - Оксид серы (IV)
Бесцветный газ с резким запахом, ядовит.
3. Уголь, С
Твердое, темно-серого цвета
C+ O2 = CO2
CO2 - Оксид углерода (IV)
Бесцветный газ, не ядовит
4. Железо
3
Твердое с металлическим блеском
Fe + O2 = Fe3O4
2
железная окалина
FeO·Fe2O3
Оксид железа (II)
Оксид железа (III)
Твердое, хрупкое
Слайд 6Химические свойства кислорода
Горение фосфора
Горение серы
Горение угля
Горение железа
Горение метана
Слайд 7Реакции окисления - - реакции взаимодействия веществ с кислородом с выделением
Слайд 8Оксиды – сложные вещества состоящие из атомов двух химических элементов, один
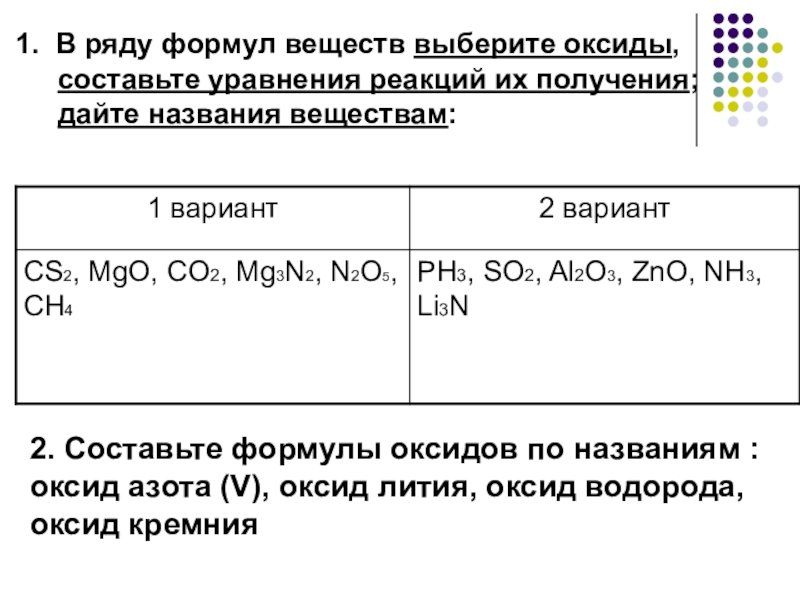
Слайд 9 1. В ряду формул веществ выберите оксиды, составьте уравнения реакций
2. Составьте формулы оксидов по названиям : оксид азота (V), оксид лития, оксид водорода, оксид кремния
Слайд 10Взаимопроверка
MgO CO2 NO
SO2 Al2O3 ZnO
2Mg + O2 = 2MgO
C + O2
N2 + O2 = 2NO
S + O2 = SO2
4Al + 3O2 = 2Al2O3
2Zn + O2 = 2ZnO
Оксид магния
Оксид углерода (IV)
Оксид азота (II)
Оксид серы (IV)
Оксид алюминия
Оксид цинка
2. N2O5, Li2O, H2O, SiO2
Слайд 11Для кислорода верны следующие утверждения:
а) Кислород – бесцветный газ, без вкуса
б) Кислород немного легче воздуха.
в) В кислороде горят и такие вещества, которые обычно считают негорючими, например железо.
г) Известны химические элементы, которые непосредственно с кислородом соединяются. К ним относятся золото Au и некоторые другие.
д) Применение кислорода основано на его физических свойствах.
е) Непрерывный круговорот кислорода непосредственно связан с таким процессом, как фотосинтез.