- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Фенол
Содержание
- 1. Фенол
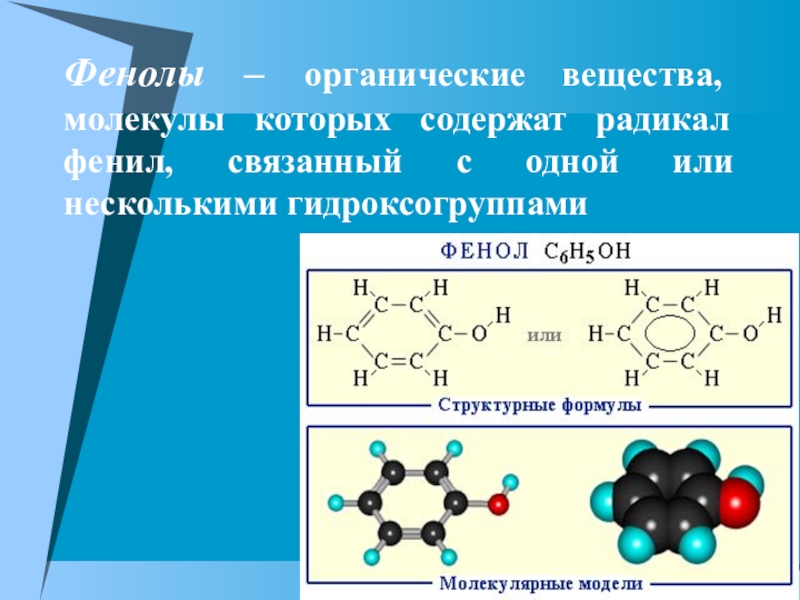
- 2. Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксогруппами
- 3. Фенолы классифицируют по атомности, т.е. по количеству
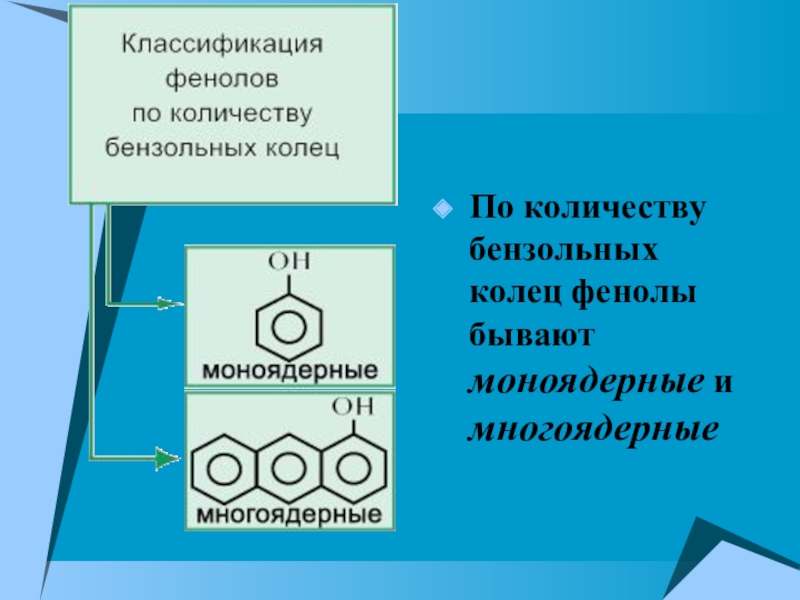
- 4. По количеству бензольных колец фенолы бывают моноядерные и многоядерные
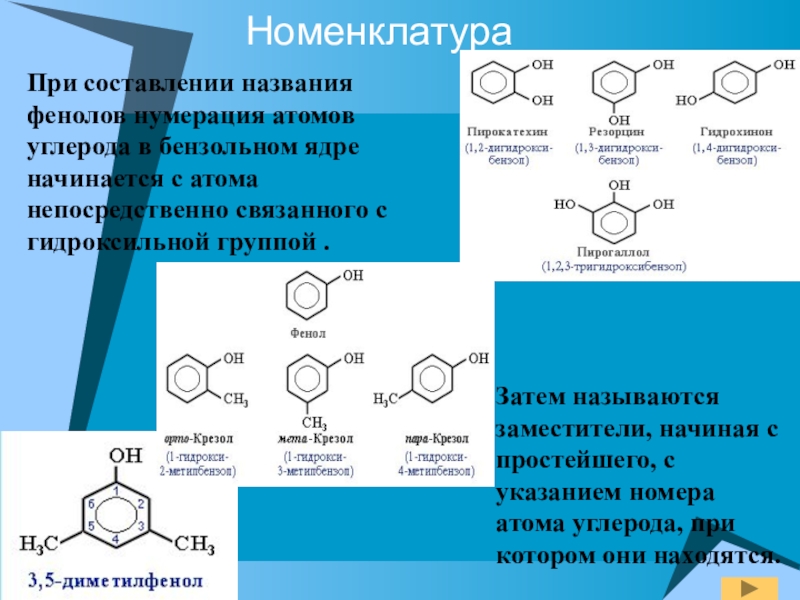
- 5. НоменклатураПри составлении названия фенолов нумерация атомов углерода
- 6. Дайте название веществам4 - метилфенол1,4 - дигидрофенол3,4- диметил – 6 - этилфенол4 - хлорфенол3 - нитрофенол
- 7. Строение молекулы фенолаГидроксогруппа и бензольное кольцо оказывают
- 8. Физические свойства фенолаФенол - твёрдое бесцветное кристаллическое
- 9. Слайд 9
- 10. Химические свойства фенолаХимические свойства фенола обусловлены наличием в его молекулегидроксильной группы –ОНбензольного ядра
- 11. Химические свойства, обусловленные наличием гидроксильной группы1. Диссоциация
- 12. 2.Взаимодействие с натриемФенол, как и спирты, взаимодействует
- 13. 3. Взаимодействие со щелочами Влияние
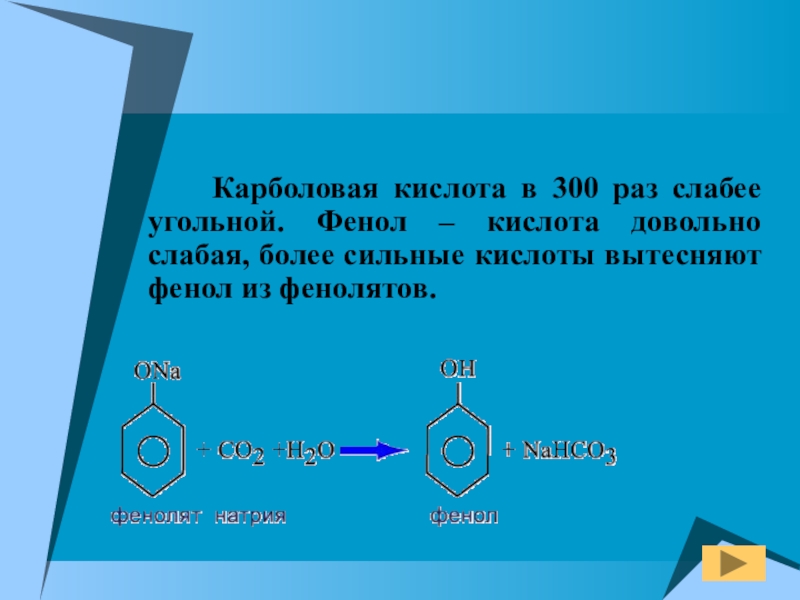
- 14. Карболовая кислота в
- 15. Химические свойства, обусловленные наличием бензольного ядра
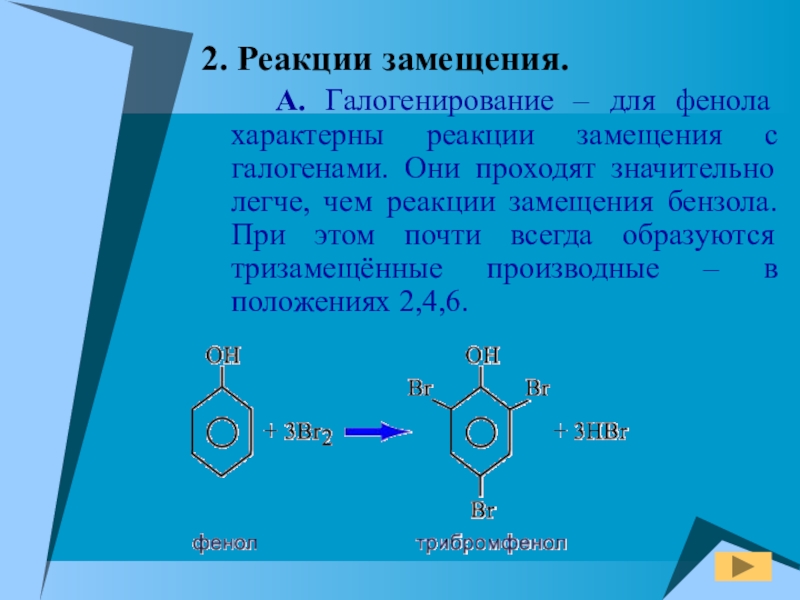
- 16. 2. Реакции замещения. А. Галогенирование –
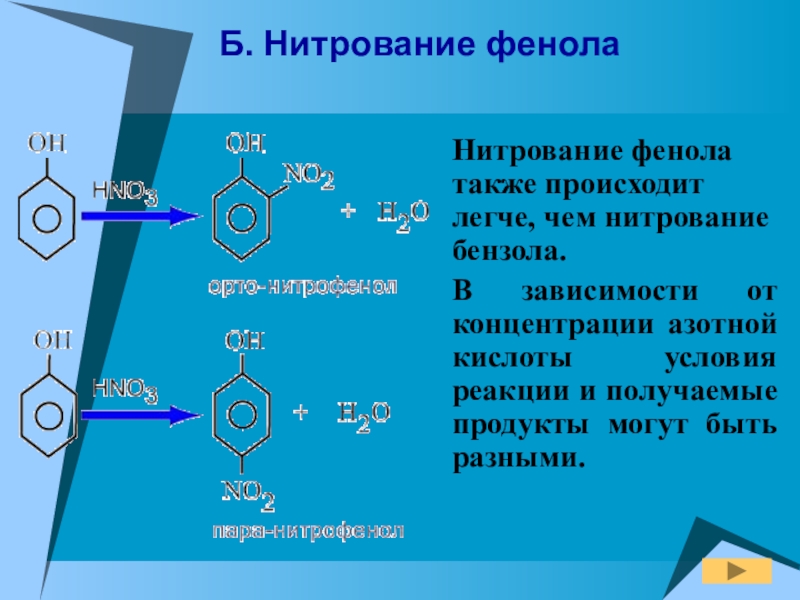
- 17. Б. Нитрование фенола Нитрование фенола также происходит
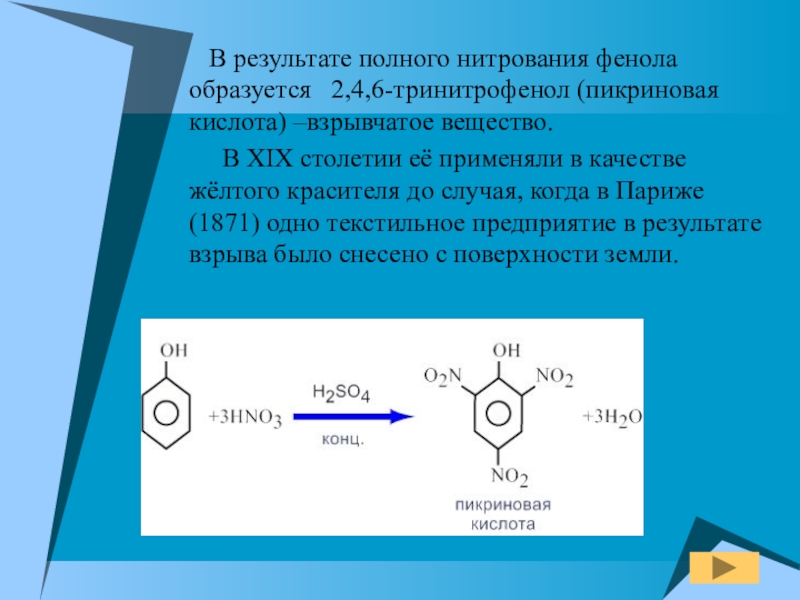
- 18. В результате полного нитрования фенола
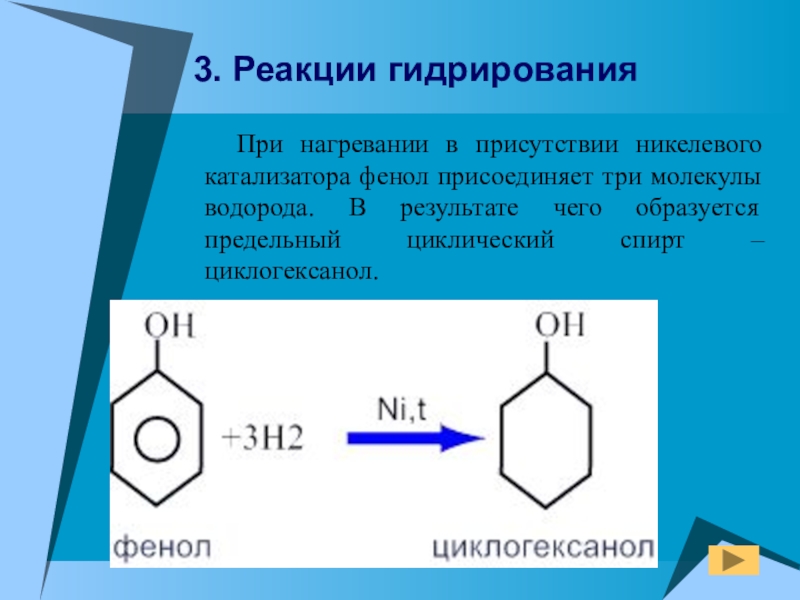
- 19. При нагревании в присутствии никелевого
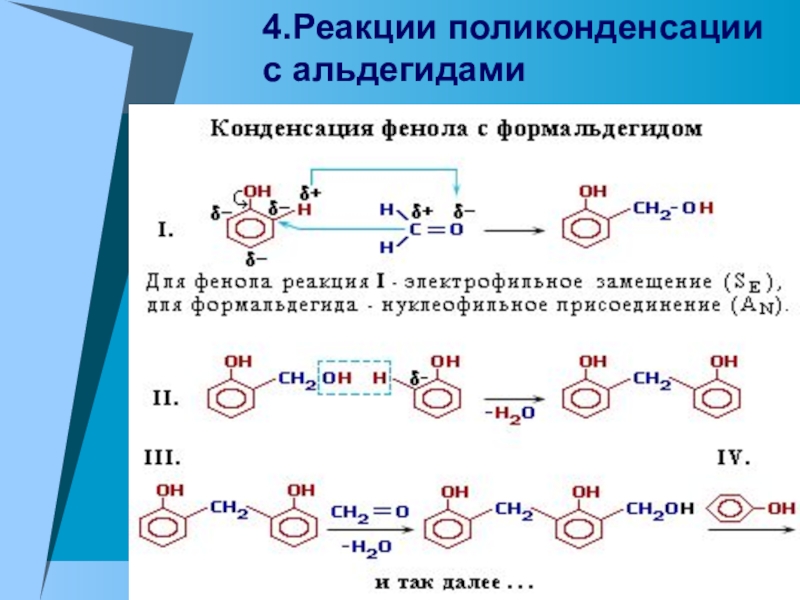
- 20. 4.Реакции поликонденсации с альдегидами
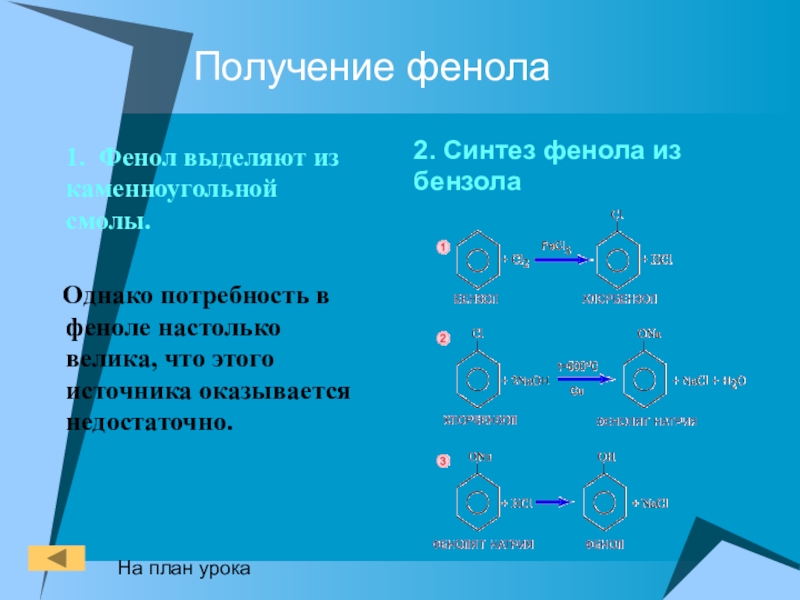
- 21. Получение фенола1. Фенол выделяют из каменноугольной смолы.
- 22. Применение фенола.ФЕНОЛ
- 23. Слайд 23
- 24. Домашнее задание§ 21, вопр. 1-3, упр. 5
Слайд 2Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный с
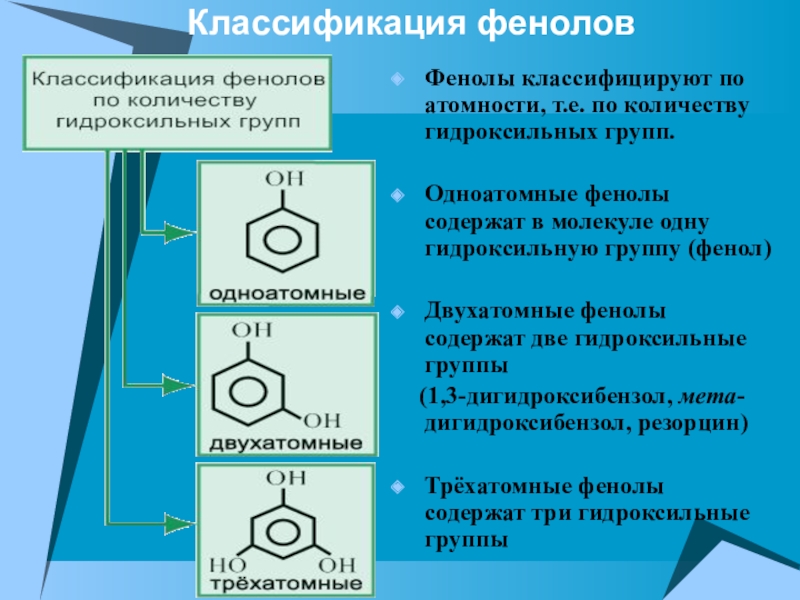
Слайд 3Фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп.
Одноатомные фенолы
Двухатомные фенолы содержат две гидроксильные группы
(1,3-дигидроксибензол, мета-дигидроксибензол, резорцин)
Трёхатомные фенолы содержат три гидроксильные группы
Классификация фенолов
Слайд 5Номенклатура
При составлении названия фенолов нумерация атомов углерода в бензольном ядре начинается
Затем называются заместители, начиная с простейшего, с указанием номера атома углерода, при котором они находятся.
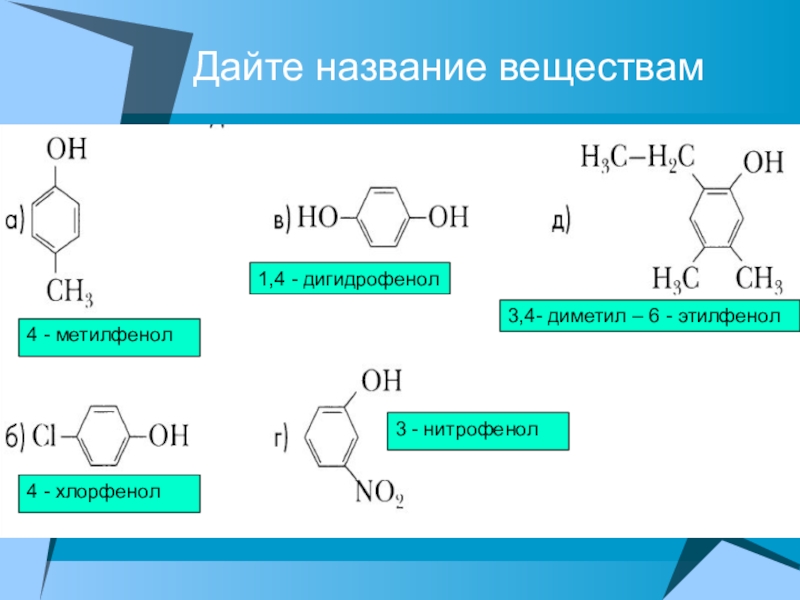
Слайд 6Дайте название веществам
4 - метилфенол
1,4 - дигидрофенол
3,4- диметил – 6 -
4 - хлорфенол
3 - нитрофенол
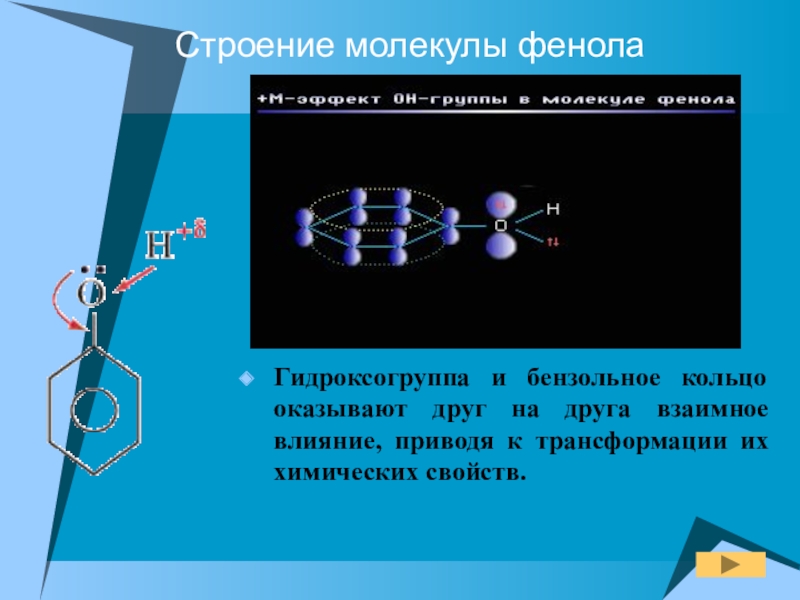
Слайд 7Строение молекулы фенола
Гидроксогруппа и бензольное кольцо оказывают друг на друга взаимное
Слайд 8Физические свойства фенола
Фенол - твёрдое бесцветное кристаллическое вещество. Вследствие частичного окисления
Фенол ядовит! При попадании на кожу вызывает ожоги поэтому с фенолом необходимо обращаться осторожно!
Слайд 10Химические свойства фенола
Химические свойства фенола обусловлены наличием в его молекуле
гидроксильной группы
бензольного ядра
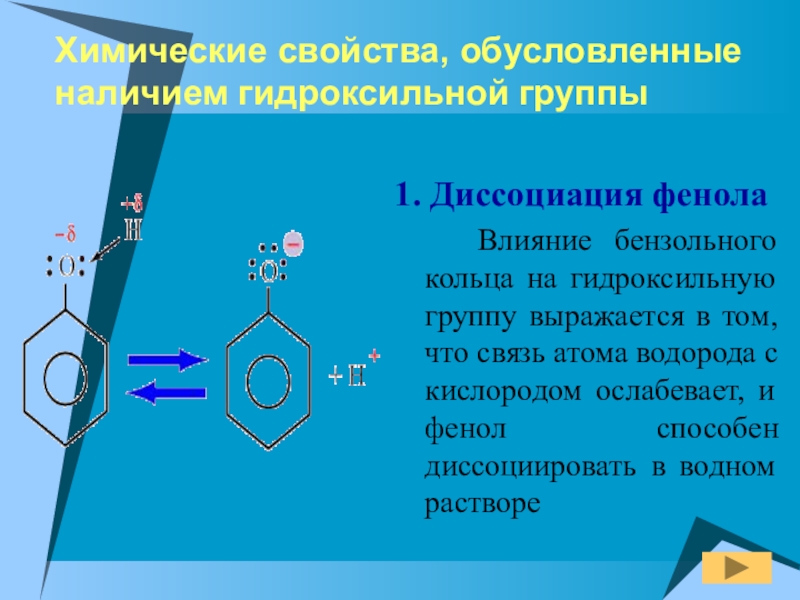
Слайд 11Химические свойства, обусловленные наличием гидроксильной группы
1. Диссоциация фенола
Влияние бензольного
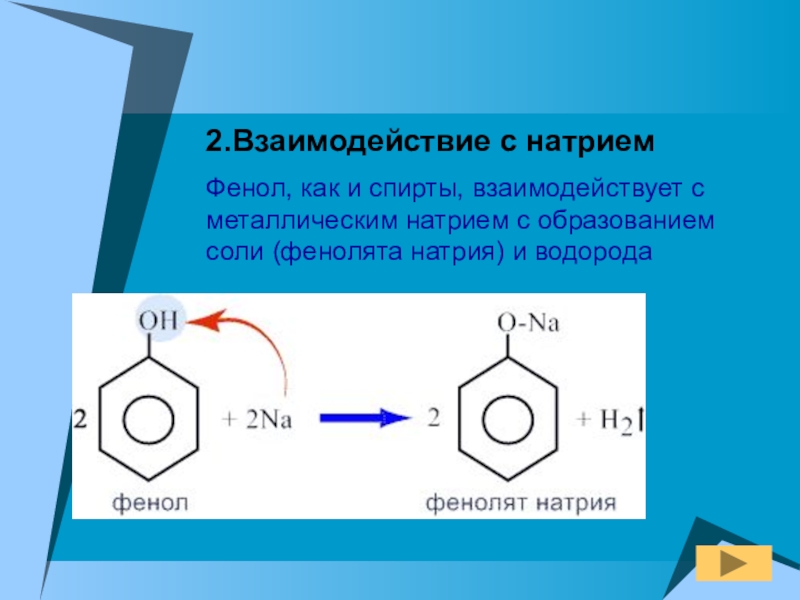
Слайд 122.Взаимодействие с натрием
Фенол, как и спирты, взаимодействует с металлическим натрием с
Слайд 133. Взаимодействие со щелочами
Влияние бензольного ядра обуславливает свойство,
Слайд 14
Карболовая кислота в 300 раз слабее угольной.
Слайд 15Химические свойства, обусловленные наличием бензольного ядра
Отличия от ароматических
1. Реакции окисления
Фенол окисляется кислородом воздуха, приобретая фиолетовую окраску.
Слайд 162. Реакции замещения.
А. Галогенирование – для фенола характерны реакции
Слайд 17Б. Нитрование фенола
Нитрование фенола также происходит легче, чем нитрование бензола.
В зависимости
Слайд 18 В результате полного нитрования фенола образуется 2,4,6-тринитрофенол (пикриновая
В XIX столетии её применяли в качестве жёлтого красителя до случая, когда в Париже (1871) одно текстильное предприятие в результате взрыва было снесено с поверхности земли.
Слайд 19 При нагревании в присутствии никелевого катализатора фенол присоединяет три
3. Реакции гидрирования
Слайд 21Получение фенола
1. Фенол выделяют из каменноугольной смолы.
Однако потребность
2. Синтез фенола из бензола
На план урока
Слайд 23
Практически сразу после получения фенола ученые установили, что это химическое вещество обладает не только полезными свойствами, что позволяет его использовать в различных сферах науки и производства, но и является сильнодействующим ядом. Так, вдыхание паров фенола в течение непродолжительного времени может привести к раздражению носоглотки, ожогам дыхательных путей и последующему отеку легких с летальным исходом. При соприкосновении раствора фенола с кожей образуются химические ожоги, которые впоследствии трансформируются в язвы.