Выполнила:
учитель химии МАОУ «СПШ №33 Пушкарева Т.П.
г. Старый Оскол
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Электронный образовательный ресурс Железо и ртуть. Их влияние на здоровье человека
Содержание
- 1. Электронный образовательный ресурс Железо и ртуть. Их влияние на здоровье человека
- 2. Содержание железа в организме человека (масса тела
- 3. Небольшая часть железа расходуется на рост покровных
- 4. Чтобы железо было усвоено, оно подвергается сложнейшим
- 5. Если человек плохо пережевывает пищу или ест
- 6. Слайд 6
- 7. Когда железа начинает не хватать и организм
- 8. Для работы мозга требуется огромное количество кислорода,
- 9. Реакция организма на избыток железаЕсли же в
- 10. Знаете ли вы, что... Граф А.П.Бестужев-Рюмин (1693–1766)
- 11. Тест «Порядок ли у вас с железом?»На
- 12. Ртуть – яд кумулятивного действия, способна накапливаться
- 13. Токсические свойства ртутиВ отличие от многих веществ,
- 14. Так или иначе, каждый из нас имеет
- 15. Опасность хронического отравления ртутью заключается в том,
- 16. Слайд 16
- 17. Возникает вопрос: как объяснить то обстоятельство, что
- 18. При приеме препаратов ртути внутрь возникает острое
- 19. Помощь при острых отравлениях препаратами ртути1. Предпринять
- 20. Знаете ли вы, что... В
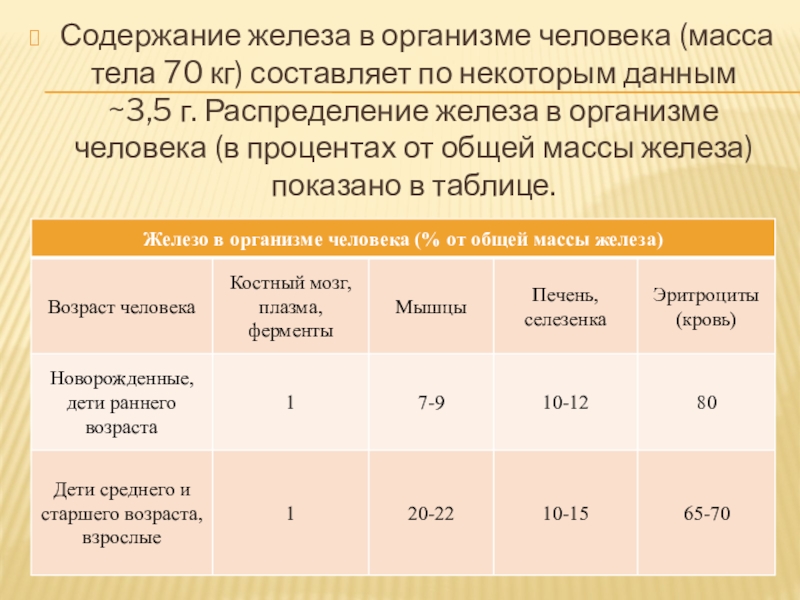
Содержание железа в организме человека (масса тела 70 кг) составляет по некоторым данным ~3,5 г. Распределение железа в организме человека (в процентах от общей массы железа) показано в таблице.
Слайд 1Валеология на уроках
неорганической химии
Железо и ртуть.
Их влияние на здоровье
человека
Слайд 2Содержание железа в организме человека (масса тела 70 кг) составляет по
некоторым данным ~3,5 г. Распределение железа в организме человека (в процентах от общей массы железа) показано в таблице.
Слайд 3Небольшая часть железа расходуется на рост покровных тканей организма – кожи
и ногтей. Железо входит в состав пигмента, окрашивающего волосы (рыжие волосы содержат в 5 раз больше железа, чем любые другие). Как видно из приведенных выше данных, основная масса железа находится в крови – эритроцитах. Это стало известно благодаря открытию француза Мери в ХIХ в. Эритроциты – красные кровяные клетки, главная функция которых заключается в осуществлении газообмена организма с окружающей средой, т. е. эритроциты переносят в организме кислород, поступающий при дыхании.
Входя в состав железосодержащего пигмента – гемоглобина, железо определяет красную окраску этого вещества, а также цвет крови. Молекула гемоглобина состоит из двух частей: из белка – глобина (основная часть молекулы, которая у разных живых организмов имеет разное строение) и железосодержащей группы – гема, который у всех организмов один и тот же. В составе молекулы гемоглобина четыре гема и в каждом – по одному атому железа, на их долю приходится всего лишь 0,35% массы огромной молекулы.
Входя в состав железосодержащего пигмента – гемоглобина, железо определяет красную окраску этого вещества, а также цвет крови. Молекула гемоглобина состоит из двух частей: из белка – глобина (основная часть молекулы, которая у разных живых организмов имеет разное строение) и железосодержащей группы – гема, который у всех организмов один и тот же. В составе молекулы гемоглобина четыре гема и в каждом – по одному атому железа, на их долю приходится всего лишь 0,35% массы огромной молекулы.
Слайд 4Чтобы железо было усвоено, оно подвергается сложнейшим превращениям. В пищевых продуктах
железо находится в трехвалентной форме. Клетки же слизистой оболочки кишечника пропускают железо в двухвалентной форме – в виде соли хлорида железа(II) FeCl2 или сульфата железа(II) FeSO4. Двухвалентным оно бывает только в составе специальных лекарственных препаратов (см. далее табл. 3). Миновав пищевод и попав в желудок, трехвалентное железо под действием желудочного сока восстанавливается в двухвалентное. Важнейшую роль в этом процессе играют соляная кислота и другие вещества, входящие в состав желудочного сока. Поэтому при пониженной кислотности назначают препараты железа вместе с соляной кислотой или желудочным соком. Из всего железа, которое находится в пище, усваивается 2–20%, причем немаловажно и то, что из продуктов растительного происхождения усваивается только от 2–8% железа. В продуктах животного происхождения атомы железа входят в состав белковых молекул, что облегчает его усвоение.
Слайд 5Если человек плохо пережевывает пищу или ест редко, но помногу, железо
из трехвалентной формы не восстанавливается в двухвалентную и остается недоступным для усвоения, т. к. соляная кислота, пепсин и другие реагенты просто не успевают добраться до железа, заключенного в массе съеденной пищи.
Всасывание железа заметно снижается при заболеваниях, связанных с поражением слизистой оболочки кишечника (особенно паразитарных).
Влияет на усвоение железа и состав пищи. Витамин С и фруктоза (содержится в овощах, фруктах, соках, меде) создают благоприятные условия для усвоения железа, т. к. образуют с ним хорошо растворимые соединения. Большую роль играют витамины группы В. Однако у железа кроме «друзей» имеются и «враги». «Враги» железа – это чай, кофе, молочные продукты и яичные желтки. Чашка чая, выпитая во время еды, сократит усвоение железа почти на 2/3, поскольку при этом образуются труднорастворимые соединения. Если кофе выпит после приема пищи, то организм недосчитается 40% железа, а если – за 1 ч до еды, он оставит железо в неприкосновенности. Если с железом у вас все в порядке, то можно спокойно есть продукты, которые числятся во «врагах» железа. Если же нет, то необходимо изменить свой образ жизни.
Всасывание железа заметно снижается при заболеваниях, связанных с поражением слизистой оболочки кишечника (особенно паразитарных).
Влияет на усвоение железа и состав пищи. Витамин С и фруктоза (содержится в овощах, фруктах, соках, меде) создают благоприятные условия для усвоения железа, т. к. образуют с ним хорошо растворимые соединения. Большую роль играют витамины группы В. Однако у железа кроме «друзей» имеются и «враги». «Враги» железа – это чай, кофе, молочные продукты и яичные желтки. Чашка чая, выпитая во время еды, сократит усвоение железа почти на 2/3, поскольку при этом образуются труднорастворимые соединения. Если кофе выпит после приема пищи, то организм недосчитается 40% железа, а если – за 1 ч до еды, он оставит железо в неприкосновенности. Если с железом у вас все в порядке, то можно спокойно есть продукты, которые числятся во «врагах» железа. Если же нет, то необходимо изменить свой образ жизни.
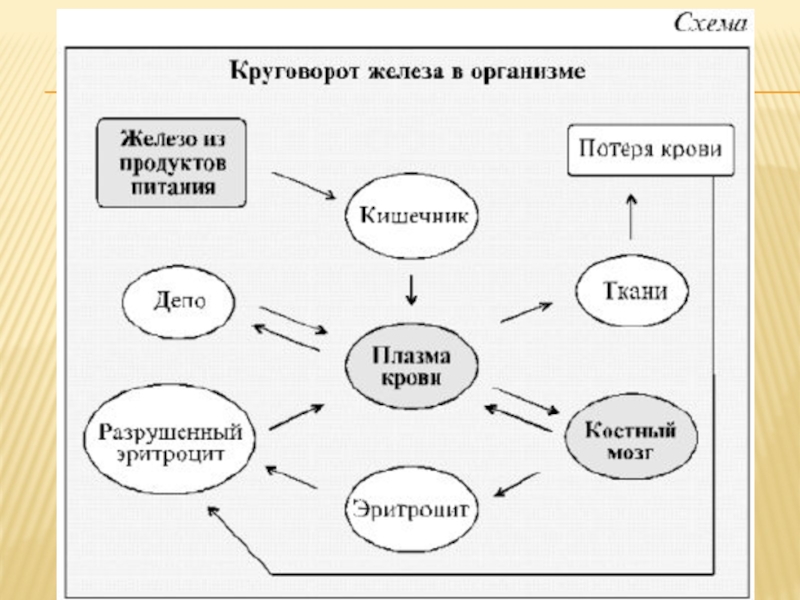
Слайд 7Когда железа начинает не хватать и организм приступает к расходованию его
запасов, хранящихся в печени, печень отвечает на это резким увеличением производства «проводников» железа – апоферритина и трансферрина. Всасывание железа через слизистую оболочку кишечника тут же увеличивается: организм стремится за каждым атомом железа и из тех же пищевых продуктов усваивает в 1,5–4 раза больше железа, чем обычно.
И все же эти резервы могут оказаться недостаточными, если с пищей поступает слишком мало железа или слишком велики его потери: возникает заболевание железодефицитная анемия, или малокровие.
И все же эти резервы могут оказаться недостаточными, если с пищей поступает слишком мало железа или слишком велики его потери: возникает заболевание железодефицитная анемия, или малокровие.
Слайд 8Для работы мозга требуется огромное количество кислорода, а при анемии мозг
не получает его в нужном количестве. Чаще анемия развивается в подростковом возрасте, когда происходит период полового созревания. В этот период особенно нужно следить за питанием, чтобы оно было богато железом. При сильной степени анемии назначают лекарственные препараты, содержащие железо (табл. 3). После приема этих препаратов необходимо тщательно полоскать рот, т. к. может произойти потемнение эмали зубов. Препараты железа могут вызвать раздражение слизистой оболочки желудочно-кишечного тракта, тошноту, рвоту. Поскольку такие препараты связывают сероводород кишечника (естественный стимулятор перистальтики), они могут вызывать запоры.
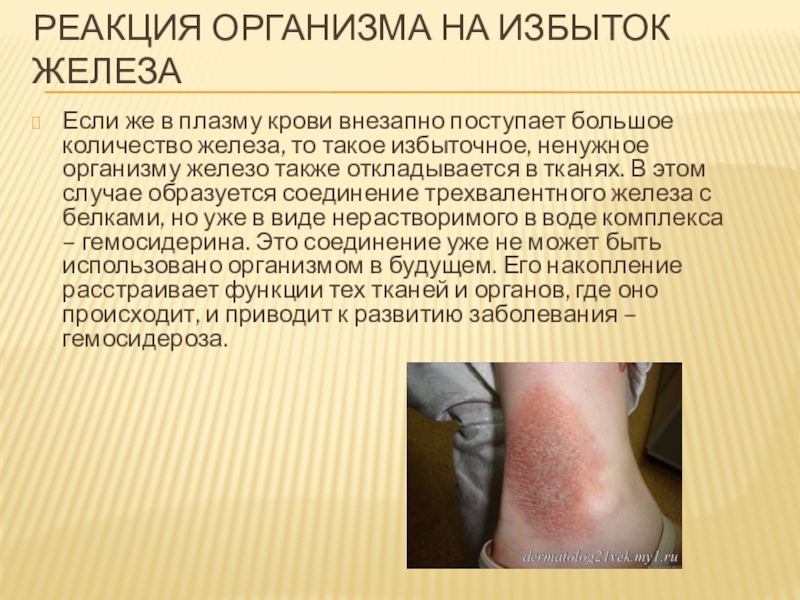
Слайд 9Реакция организма на избыток железа
Если же в плазму крови внезапно поступает
большое количество железа, то такое избыточное, ненужное организму железо также откладывается в тканях. В этом случае образуется соединение трехвалентного железа с белками, но уже в виде нерастворимого в воде комплекса – гемосидерина. Это соединение уже не может быть использовано организмом в будущем. Его накопление расстраивает функции тех тканей и органов, где оно происходит, и приводит к развитию заболевания – гемосидероза.
Слайд 10Знаете ли вы, что...
Граф А.П.Бестужев-Рюмин (1693–1766) – канцлер императрицы Елизаветы
и генерал-фельдмаршал императрицы Екатерины II – предложил капли, получившие название «бестужевские», как укрепляющее и возбуждающее средство. Капли представляли собой раствор хлорида железа(III) в смеси этилового спирта и этилового эфира. Екатерина их часто употребляла.
Гематоген производится из бычьей крови и применяется для профилактики анемии.
Экспериментально показано, что у здоровых мужчин и женщин однократный прием умеренной дозы алкоголя вызывает усиленное выведение через кишечник железа, алюминия, цинка, что создает предпосылки для дефицита этих металлов в организме.
Чай содержит дубильную кислоту. Если смешать светлый настой чая с раствором соли железа, то он почернеет, т. к. дубильная кислота, содержащаяся в чае, в соединении с железом образует чернила. Вот почему нельзя заваривать чай в металлическом чайнике.
Гематоген производится из бычьей крови и применяется для профилактики анемии.
Экспериментально показано, что у здоровых мужчин и женщин однократный прием умеренной дозы алкоголя вызывает усиленное выведение через кишечник железа, алюминия, цинка, что создает предпосылки для дефицита этих металлов в организме.
Чай содержит дубильную кислоту. Если смешать светлый настой чая с раствором соли железа, то он почернеет, т. к. дубильная кислота, содержащаяся в чае, в соединении с железом образует чернила. Вот почему нельзя заваривать чай в металлическом чайнике.
Слайд 11Тест «Порядок ли у вас с железом?»
На вопросы отвечайте либо «да»,
либо «нет».
1. Часто ли вы чувствуете усталость и подавленность?
2. Произошли ли у вас в последнее время изменения кожи, волос и ногтей (например, нетипичная бледность и шероховатость кожи, ломкие волосы, вмятины на ногтях)?
3. Теряли ли вы в последнее время много крови?
4. Обильны ли ваши менструации?
5. Занимаетесь ли вы профессиональным спортом?
6. Редко ли вы употребляете или вовсе не едите мясо?
7. Выпиваете ли вы более трех чашек черного чая или кофе в день?
8. Вы едите мало овощей?
Если на большинство вопросов вы ответили «нет», то ваш организм в достаточной степени обеспечен железом.
1. Часто ли вы чувствуете усталость и подавленность?
2. Произошли ли у вас в последнее время изменения кожи, волос и ногтей (например, нетипичная бледность и шероховатость кожи, ломкие волосы, вмятины на ногтях)?
3. Теряли ли вы в последнее время много крови?
4. Обильны ли ваши менструации?
5. Занимаетесь ли вы профессиональным спортом?
6. Редко ли вы употребляете или вовсе не едите мясо?
7. Выпиваете ли вы более трех чашек черного чая или кофе в день?
8. Вы едите мало овощей?
Если на большинство вопросов вы ответили «нет», то ваш организм в достаточной степени обеспечен железом.
Слайд 12Ртуть – яд кумулятивного действия, способна накапливаться в организме, главным образом
в жировых тканях, вызывает уродства у детей. Токсическая доза составляет 0,4 мг, летальная – 150–300 мг.
Слайд 13Токсические свойства ртути
В отличие от многих веществ, которые в газовой фазе
находятся в форме двух-, трех- и четырехатомных молекул, ртуть существует в виде атомов Нg. Попадая в легкие, пары ртути проникают в кровеносную систему и вступают в химическое взаимодействие с белками-ферментами, биокатализаторами, которые осуществляют в нашем организме тысячи химических процессов. Одни ферменты, связавшись атомами ртути, теряют свои каталитические свойства, а другие – начинают ускорять реакции, продуктами которых являются вещества, отравляющие организм.
Слайд 14Так или иначе, каждый из нас имеет дело c ртутью. Всем
нам приходится измерять температуру тела. Возможна такая ситуация, когда при измерении температуры градусник выпадает у вас из рук и... разбивается. Мельчайшие капельки ртути рассыпаются по полу. Обстоятельства осложняются, если это происходит в помещении, где паркетный пол: тогда капельки попадают в щели между планками. Концентрация ртути становится больше ПДК примерно в 100 раз. В этом случае необходимо выполнить ряд действий для предотвращения хронического отравления обитателей комнаты:
1. Собрать с помощью медной (латунной) проволоки (пластинки) или листочков фольги («серебряной», оловянной бумажки от конфет) вытекшую ртуть. К медной и оловянной поверхности жидкая ртуть, смачивая ее, прилипнет. Для этого также можно воспользоваться обыкновенной медицинской грушей. После сбора капель места, где могла задержаться ртуть, надо засыпать порошком серы или алюминиевой пылью или же залить раствором хлорида железа (III).
2. Поместить в стеклянную баночку все собранные шарики и отвезти на ближайшую санитарно-эпидемиологическую станцию.
3. Место, где находилась ртуть, протереть влажной тряпкой, после чего тщательно вымыть руки (а тряпку выбросить).
1. Собрать с помощью медной (латунной) проволоки (пластинки) или листочков фольги («серебряной», оловянной бумажки от конфет) вытекшую ртуть. К медной и оловянной поверхности жидкая ртуть, смачивая ее, прилипнет. Для этого также можно воспользоваться обыкновенной медицинской грушей. После сбора капель места, где могла задержаться ртуть, надо засыпать порошком серы или алюминиевой пылью или же залить раствором хлорида железа (III).
2. Поместить в стеклянную баночку все собранные шарики и отвезти на ближайшую санитарно-эпидемиологическую станцию.
3. Место, где находилась ртуть, протереть влажной тряпкой, после чего тщательно вымыть руки (а тряпку выбросить).
Слайд 15Опасность хронического отравления ртутью заключается в том, что человек в течение
длительного времени не обнаруживает признаков расстройства здоровья. В это время и происходит развитие тех биологических изменений, результатом которых становятся тяжелые последствия, а именно: повышенная возбудимость, острые головные боли, общая слабость, повышенная утомляемость, прогрессирующее ослабление памяти, обмороки. Позже начинают дрожать руки, веки, в тяжелых случаях – ноги. Эти признаки хронического отравления ртутью могут сопровождаться разрыхлением десен, выпадением зубов и волос, расстройством пищеварительного тракта.
Организм детей и женщин более чувствителен к воздействию ртути, чем организм мужчин.
Арабские алхимики и врачи, не знавшие о пагубных последствиях нахождения в помещении со ртутью, заметили, что скорпионы покидают жилище, в котором разлита ртуть. Это происходит потому, что ферментные белки скорпиона отличаются от человеческих. Молекулы тканей скорпиона немедленно «ощущают» действие атомов ртути, например, на ферменты, обеспечивающие процесс дыхания. Было бы неплохо иметь и человеку такую «сигнальную систему раннего реагирования» на наличие в воздухе паров ртути. А пока ничтожное содержание ртути в воздухе лабораторий и промышленных предприятий химики определяют на основе чувствительных цветовых реакций.
Ртуть – единственный (в природных условиях) жидкий металл, который испаряется даже при комнатной температуре. Ее пары имеют свойство равномерно распространяться по всему объему, сорбируясь тканями, деревянными изделиями и материалами различных конструкций. При температуре выше 28 °С ртуть начинает испаряться и ее пары снова попадают в воздух. Поэтому ее действие всеобъемлюще: она загрязняет почву, воздух и воду.
Если металлическая ртуть по разным причинам попадает в организм человека, отравляющего эффекта не наблюдается. В литературе описывается случай, когда в кровь человека попало несколько миллилитров ртути. Жидкая ртуть в течение девяти лет обнаруживалась при рентгеноскопии в желудочке сердца и на поверхности легких. Но признаков ртутного отравления не наблюдалось.
Организм детей и женщин более чувствителен к воздействию ртути, чем организм мужчин.
Арабские алхимики и врачи, не знавшие о пагубных последствиях нахождения в помещении со ртутью, заметили, что скорпионы покидают жилище, в котором разлита ртуть. Это происходит потому, что ферментные белки скорпиона отличаются от человеческих. Молекулы тканей скорпиона немедленно «ощущают» действие атомов ртути, например, на ферменты, обеспечивающие процесс дыхания. Было бы неплохо иметь и человеку такую «сигнальную систему раннего реагирования» на наличие в воздухе паров ртути. А пока ничтожное содержание ртути в воздухе лабораторий и промышленных предприятий химики определяют на основе чувствительных цветовых реакций.
Ртуть – единственный (в природных условиях) жидкий металл, который испаряется даже при комнатной температуре. Ее пары имеют свойство равномерно распространяться по всему объему, сорбируясь тканями, деревянными изделиями и материалами различных конструкций. При температуре выше 28 °С ртуть начинает испаряться и ее пары снова попадают в воздух. Поэтому ее действие всеобъемлюще: она загрязняет почву, воздух и воду.
Если металлическая ртуть по разным причинам попадает в организм человека, отравляющего эффекта не наблюдается. В литературе описывается случай, когда в кровь человека попало несколько миллилитров ртути. Жидкая ртуть в течение девяти лет обнаруживалась при рентгеноскопии в желудочке сердца и на поверхности легких. Но признаков ртутного отравления не наблюдалось.
Слайд 17Возникает вопрос: как объяснить то обстоятельство, что инертный металл, встречающийся в
природе в самородном виде, который в обычных условиях не окисляется кислородом, не взаимодействует с водой и щелочами, не растворяется в большинстве кислот (растворяется только в царской водке, горячей концентрированной H2SO4 и HNO3), вдруг проявляет ядовитые свойства?
Необходимо различать действия металлической ртути, ее паров и солей.
Наиболее токсичны соли Hg2+, например сулема HgCl2. Если в организм попадают соли Hg2+, то немедленно возникает рвота и наступает упадок сердечной деятельности, резкое понижение температуры тела и обморок.
Металлическая ртуть практически безвредна для живых существ, т. к. в организме процесс образования иона двухвалентной ртути Hg – 2e = Hg2+, который и может вызвать отравление, не происходит.
Токсичность паров ртути объясняется изменением химических свойств вещества при его измельчении, в предельном случае – атомизации вещества, которая является очень эффективным способом повышения его химической активности.
Соединения одновалентной ртути менее токсичны, чем соединения двухвалентной ртути.
Необходимо различать действия металлической ртути, ее паров и солей.
Наиболее токсичны соли Hg2+, например сулема HgCl2. Если в организм попадают соли Hg2+, то немедленно возникает рвота и наступает упадок сердечной деятельности, резкое понижение температуры тела и обморок.
Металлическая ртуть практически безвредна для живых существ, т. к. в организме процесс образования иона двухвалентной ртути Hg – 2e = Hg2+, который и может вызвать отравление, не происходит.
Токсичность паров ртути объясняется изменением химических свойств вещества при его измельчении, в предельном случае – атомизации вещества, которая является очень эффективным способом повышения его химической активности.
Соединения одновалентной ртути менее токсичны, чем соединения двухвалентной ртути.
Слайд 18При приеме препаратов ртути внутрь возникает острое отравление. Симптомы отравления обусловлены:
а)
раздражающим и прижигающим действием соединений ртути на желудочно-кишечный тракт;
б) всасыванием (резорбцией) ионов ртути;
в) действием ртути на органы выделения.
Раздражающее и прижигающее действия препаратов ртути на слизистые оболочки желудочно-кишечного тракта развиваются вскоре после приема препаратов внутрь. При этом появляются металлический вкус и чувство жжения во рту, боли в животе, тошнота и рвота (нередко с примесью крови), усиливается слюноотделение. В первые часы отравления в связи с резким раздражением желудочно-кишечного тракта и возникновением в нем острых болей может развиться шок.
Всасывание ионов ртути происходит уже в первые часы отравления и влияет на центральную нервную систему (вначале происходит ее возбуждение, судороги, затем ее угнетение), наблюдается нарушение деятельности сердечно-сосудистой системы (сердечная слабость, падение артериального давления, слабый и частый пульс) и функции почек (вначале усиление, затем уменьшение мочеотделения). Ионы ртути всасываются преимущественно слизистыми оболочками пищеварительного тракта и почками, в связи с чем у пострадавших развиваются стоматит, язвенный колит и поражение почек.
Действие ионов ртути на органы выделения развивается на 2-е–3-и сутки от момента приема яда.
б) всасыванием (резорбцией) ионов ртути;
в) действием ртути на органы выделения.
Раздражающее и прижигающее действия препаратов ртути на слизистые оболочки желудочно-кишечного тракта развиваются вскоре после приема препаратов внутрь. При этом появляются металлический вкус и чувство жжения во рту, боли в животе, тошнота и рвота (нередко с примесью крови), усиливается слюноотделение. В первые часы отравления в связи с резким раздражением желудочно-кишечного тракта и возникновением в нем острых болей может развиться шок.
Всасывание ионов ртути происходит уже в первые часы отравления и влияет на центральную нервную систему (вначале происходит ее возбуждение, судороги, затем ее угнетение), наблюдается нарушение деятельности сердечно-сосудистой системы (сердечная слабость, падение артериального давления, слабый и частый пульс) и функции почек (вначале усиление, затем уменьшение мочеотделения). Ионы ртути всасываются преимущественно слизистыми оболочками пищеварительного тракта и почками, в связи с чем у пострадавших развиваются стоматит, язвенный колит и поражение почек.
Действие ионов ртути на органы выделения развивается на 2-е–3-и сутки от момента приема яда.
Слайд 19Помощь при острых отравлениях препаратами ртути
1. Предпринять меры к удалению яда
и предупреждению его всасывания из желудочно-кишечного тракта. Для этого пострадавшему необходимо дать внутрь молоко, яичный белок (для связывания ртути с белком).
2. Осторожно промыть желудок водой с активированным углем.
3. Принять внутрь активированный уголь и солевое слабительное (сульфат магния).
4. Для предупреждения всасывающего действия ионов ртути рекомендуется как можно раньше начать парентеральное (например, посредством инъекции) введение антидотов (противоядие). В качестве антидотов при отравлении ртутью используют унитиол и тиосульфат натрия. Принцип действия унитиола заключается в том, что этот антидот, являясь веществом, содержащим SH-группы (сульфгидрильные группы), связывает ионы ртути. Тем самым предупреждают блокирование ртутью SH-групп белков и ферментов организма. Действие тиосульфата натрия сводится к тому, что ионы ртути образуют с этим веществом неядовитые соли.
2. Осторожно промыть желудок водой с активированным углем.
3. Принять внутрь активированный уголь и солевое слабительное (сульфат магния).
4. Для предупреждения всасывающего действия ионов ртути рекомендуется как можно раньше начать парентеральное (например, посредством инъекции) введение антидотов (противоядие). В качестве антидотов при отравлении ртутью используют унитиол и тиосульфат натрия. Принцип действия унитиола заключается в том, что этот антидот, являясь веществом, содержащим SH-группы (сульфгидрильные группы), связывает ионы ртути. Тем самым предупреждают блокирование ртутью SH-групп белков и ферментов организма. Действие тиосульфата натрия сводится к тому, что ионы ртути образуют с этим веществом неядовитые соли.
Слайд 20 Знаете ли вы, что...
В прошлом веке около 120
человек, производивших золочение Исаакиевского собора в Петербурге, получили смертельные отравления. Купола золотили, натирая металлическую кровлю амальгамой золота – раствором золота в ртути. Смертельное отравление было вызвано парами ртути, которыми ежедневно дышали рабочие. Это произошло потому, что рабочие и руководство плохо знали токсические свойства ртути и не обратили внимание на симптомы начавшегося отравления: отсутствие аппетита, головные боли и желудочные расстройства.
В средние века отравление ртутью получило название «болезнь сумасшедшего шляпочника», т. к. заболевали мастера, применявшие ртутные препараты при изготовлении фетровых шляп.
В 140 г. н. э. китайский алхимик Вый Поян занимался изготовлением «пилюль бессмертия». Их состав – сульфид ртути. Эти пилюли он принимал сам, давал их ученикам и своей любимой собаке. Все они, конечно, умерли.
С увеличением кислотности воды в озере на 1 единицу рН концентрация ртути в тканях рыб повышается в среднем на 0,14 мг/кг. В Швеции и США рыболовам рекомендовано возвращать в озеро пойманную рыбу, если ее возраст более трех лет.
Одним из широко распространенных источников ртути являются всем известные люминесцентные лампы. Одна такая лампа дневного света содержит ~150 мг ртути и, выброшенная на свалку и лишившаяся герметичности, способна загрязнить ртутью 500 тыс. м3 воздуха на уровне ПДК. Только московский завод ЗИЛ ежегодно отправлял на свалки 200 тыс. отработанных ртутных ламп.
В средние века отравление ртутью получило название «болезнь сумасшедшего шляпочника», т. к. заболевали мастера, применявшие ртутные препараты при изготовлении фетровых шляп.
В 140 г. н. э. китайский алхимик Вый Поян занимался изготовлением «пилюль бессмертия». Их состав – сульфид ртути. Эти пилюли он принимал сам, давал их ученикам и своей любимой собаке. Все они, конечно, умерли.
С увеличением кислотности воды в озере на 1 единицу рН концентрация ртути в тканях рыб повышается в среднем на 0,14 мг/кг. В Швеции и США рыболовам рекомендовано возвращать в озеро пойманную рыбу, если ее возраст более трех лет.
Одним из широко распространенных источников ртути являются всем известные люминесцентные лампы. Одна такая лампа дневного света содержит ~150 мг ртути и, выброшенная на свалку и лишившаяся герметичности, способна загрязнить ртутью 500 тыс. м3 воздуха на уровне ПДК. Только московский завод ЗИЛ ежегодно отправлял на свалки 200 тыс. отработанных ртутных ламп.