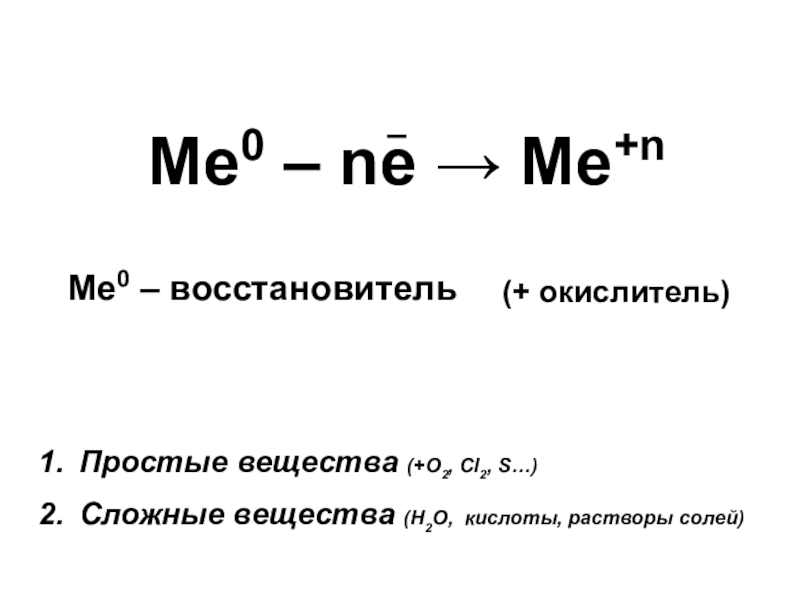- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему электрохимический ряд напряжений металлов химия 10 класс
Содержание
- 1. электрохимический ряд напряжений металлов химия 10 класс
- 2. Верите ли Вы,что...
- 3. Металлы занимают верхний левый угол в ПСХЭ.В
- 4. Ме0 – ne → Me+nМе0 – восстановительПростые
- 5. От каких факторов зависят восстановительные свойства металлов?Природы
- 6. KLi
- 7. Химическая активностьИзменение Rатома и Еионизации.Определяет
- 8. Ме(тв) → Ме+n(гидр)А(работа) =ЕатомизацииЕионизации ЕгидратацииЗатрачивается на разрушение
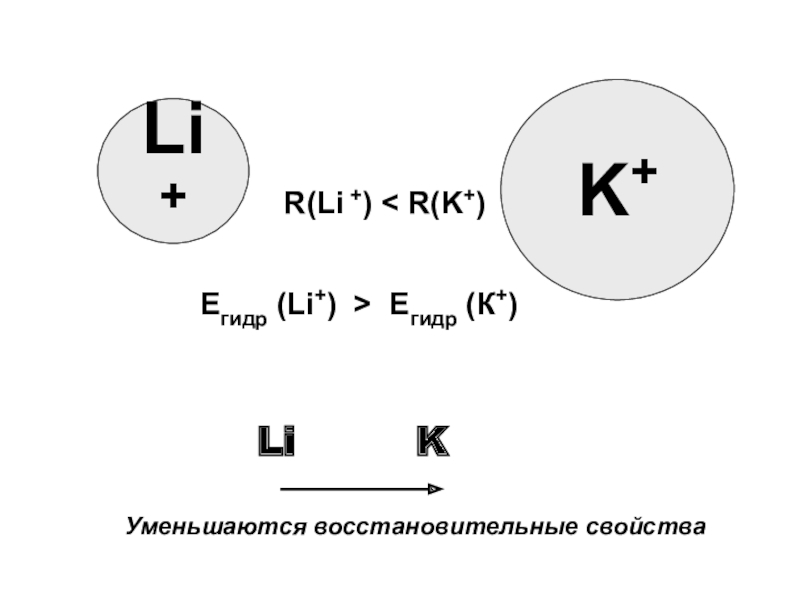
- 9. K+Li+ R(Li +) < R(K+)Eгидр (Li+) > Eгидр (К+)KУменьшаются восстановительные свойстваLi
- 10. БЕКЕТОВ НИКОЛАЙ НИКОЛАЕВИЧ (1827–1911),
- 11. ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЙ МЕТАЛЛОВ Li K Ba Sr
- 12. Практическая работа.«Взаимодействие металлов с растворами солей.»1. СuSO4
- 13. Периодическая таблица Д.И.МенделееваЭлектрохимический ряд напряжения металловХимические элементыКристаллические
- 14. 6. Чтобы оценить реакционную способность металла в
- 15. Блеф – игра: «Верите ли Вы,
- 16. Домашнее задание.Повторить из курса физики понятие «ПОТЕНЦИАЛ»;Закончить
- 17. Даны вещества: металлический Na, p-p
- 18. CПАСИБО ЗА ВНИМАНИЕ!Персональная карточка № 229-436-478
Слайд 3Металлы занимают верхний левый угол в ПСХЭ.
В кристаллах атомы металла связаны
Валентные электроны металлов прочно связаны с ядром.
У металлов, стоящих в главных подгруппах (А), на внешнем уровне обычно 2 электрона.
В группе сверху вниз происходит увеличение восстановительных свойств металлов.
Чтобы оценить реакционную способность металла в растворах солей и кислот, достаточно посмотреть в электрохимический ряд напряжения металлов.
7. Чтобы оценить реакционную способность металла в растворах солей и кислот, достаточно посмотреть в периодическую таблицу Д.И.Менделеева.
Слайд 4Ме0 – ne → Me+n
Ме0 – восстановитель
Простые вещества (+О2, Сl2, S…)
Сложные
(+ окислитель)
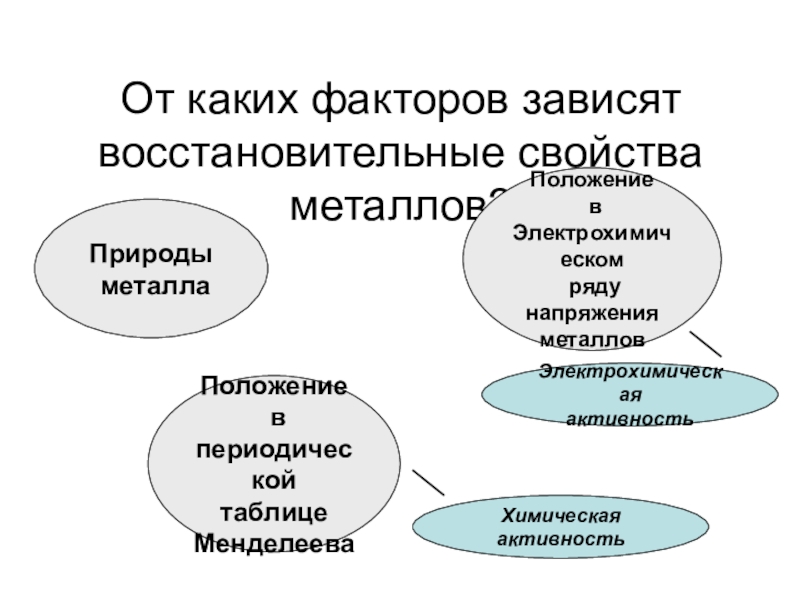
Слайд 5От каких факторов зависят восстановительные свойства металлов?
Природы
металла
Положение
в
Электрохимическом
ряду
напряжения
металлов
Положение
в периодической
таблице
Менделеева
Химическая активность
Электрохимическая
активность
Слайд 7Химическая активность
Изменение
Rатома и Еионизации.
Определяет восстановительную активность металлов в
водных растворах.
Электрохимическая активность
Таблица
Менделеева
Электрохимический
ряд
напряжения
Ме
Ме Rат (нм) Еион (кДж/ моль)
Li 0,155 513,3
Na 0,190 495,8
К 0,235 418,8
Rb 0,248 403,0
Cs 0,267 375,7
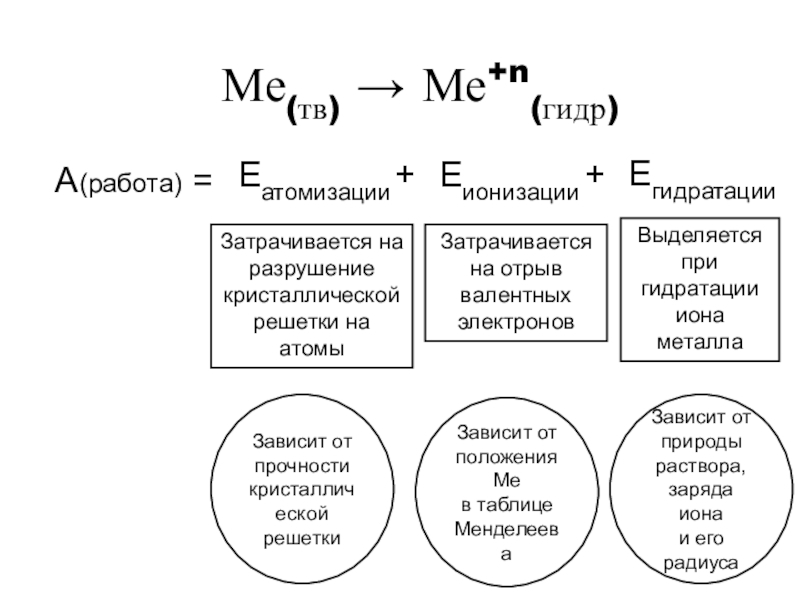
Слайд 8Ме(тв) → Ме+n(гидр)
А(работа) =
Еатомизации
Еионизации
Егидратации
Затрачивается на разрушение кристаллической решетки на атомы
+
+
Затрачивается
Выделяется при гидратации иона металла
Зависит от
прочности
кристаллической
решетки
Зависит от
положения Ме
в таблице
Менделеева
Зависит от
природы раствора,
заряда иона
и его радиуса
Слайд 10БЕКЕТОВ
НИКОЛАЙ НИКОЛАЕВИЧ
(1827–1911),
русский физикохимик.
1863 год
Вытеснительный ряд металлов
Применим только для растворов электролитов (кислот, растворов солей)
Слайд 11ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЙ МЕТАЛЛОВ
Li K Ba Sr Ca Na Mg Al Zn Cr Fe
Вывод:
1. Уменьшается восстановительные свойства металлов при реакциях в водных растворах в стандартных условиях (250С, 1атм.);
2. Металл, стоящий левее, вытесняет металл, стоящий правее из их солей в растворе;
3. Металлы, стоящие до водорода, вытесняют его из кислот в растворе (искл.: HNO3);
4. Ме (до Al) + Н2О → щелочь + Н2
Ме (до Н2) + Н2О → оксид + Н2 (жесткие условия)
Ме (после Н2) + Н2О → не реагируют
Слайд 12Практическая работа.
«Взаимодействие металлов
с растворами солей.»
1. СuSO4 → FeSO4
2. СuSO4 →
“Единственный путь, ведущий к знанию, - это деятельность”. (Б. Шоу)
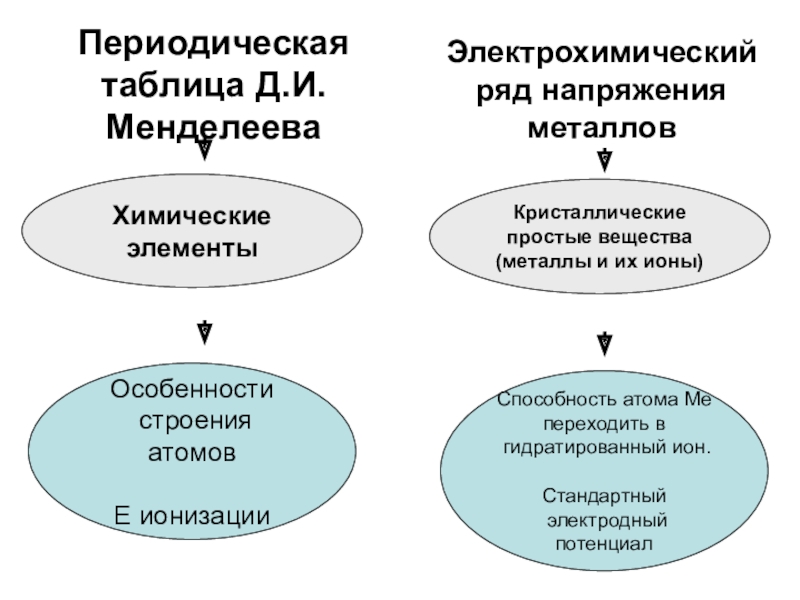
Слайд 13Периодическая таблица Д.И.Менделеева
Электрохимический ряд напряжения металлов
Химические
элементы
Кристаллические
простые вещества
(металлы и их
Особенности
строения атомов
Е ионизации
Способность атома Ме
переходить в
гидратированный ион.
Стандартный
электродный потенциал
Слайд 146. Чтобы оценить реакционную способность металла в растворах солей достаточно посмотреть
7. Чтобы оценить реакционную способность металла в растворах солей достаточно посмотреть в периодическую таблицу Д.И.Менделеева.
Слайд 16Домашнее задание.
Повторить из курса физики понятие «ПОТЕНЦИАЛ»;
Закончить уравнение реакции, написать уравнения
3. Даны металлы(Fe, Mg, Pb, Cu) – предложите опыты, подтверждающие положение данных металлов в электрохимическом ряду напряжения.;