- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему движение электронов
Содержание
- 1. движение электронов
- 2. Электрон бұлты болатын кеңістікті орбиталь деп атаймыз.
- 3. Электрондық қауыз:Атомның барлық электрондары жиналып электрондық қауызын
- 4. Кейбір электрондар ядро маңында гантель тәрізді бұлт
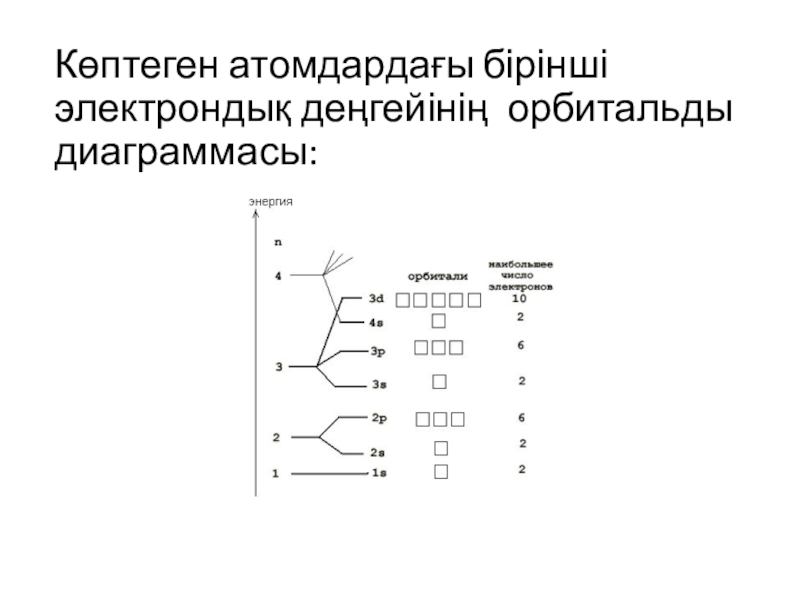
- 5. Көптеген атомдардағы бірінші электрондық деңгейінің орбитальды диаграммасы:
- 6. Электрондық бұлттарды толтыру ережесі келесі:1. Ең алдымен
- 7. Слайд 7
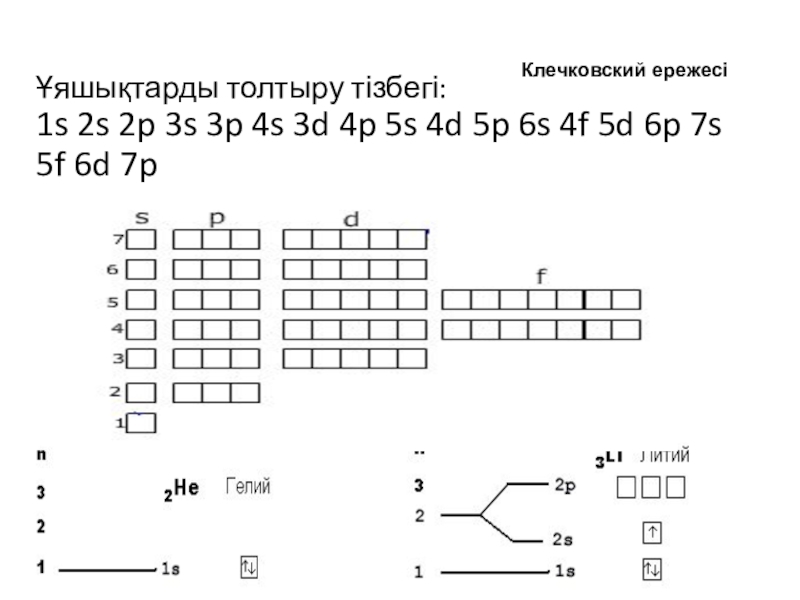
- 8. Ұяшықтарды толтыру тізбегі: 1s 2s 2p 3s
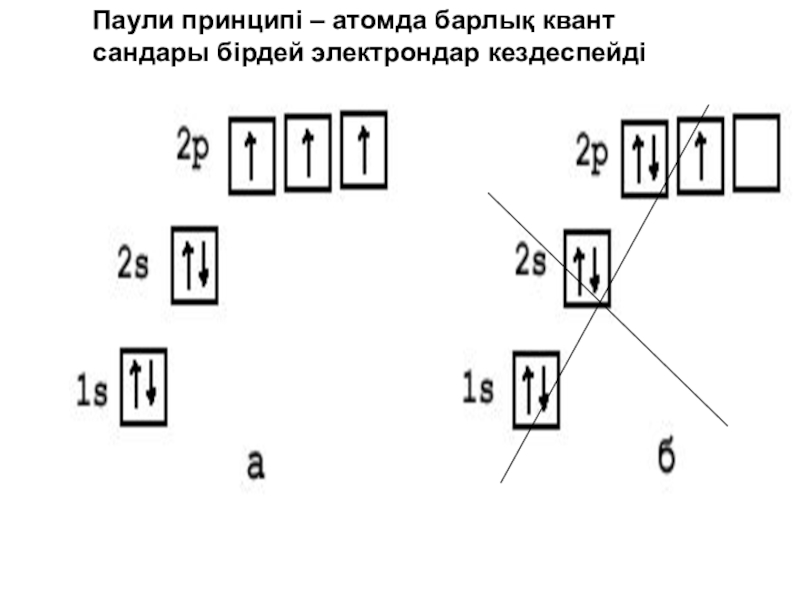
- 9. Паули принципі – атомда барлық квант сандары бірдей электрондар кездеспейді
- 10. Үйге:§ 57 Атомдардағы электрондардың қозғалысы. Есептер мен
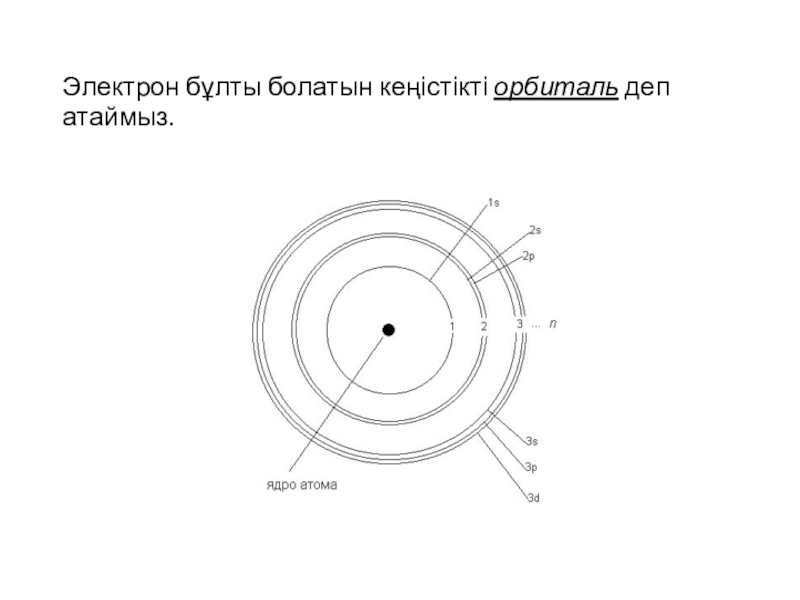
Электрон бұлты болатын кеңістікті орбиталь деп атаймыз.
Слайд 3Электрондық қауыз:
Атомның барлық электрондары жиналып электрондық қауызын құрайды. (n+L+ m +
s) n=1,2,3...; L= n -1; m =2(n+1); s =+-1/2 h/2
n- бас квант саны; L- орбиталь квант саны ; m магнит квант саны; s – спин.
Өзара энергиясы жуық электрондар атомның электрондық қабатын түзеді.
Электрондық қабаттар рет нөміріне қарай 1,2,3,4… деп белгіленеді. Np=
электрондық қабаттар саны
Әр қабаттағы орбитальдардың өзіндік энергиясы мен пішіндері болады.
Шар тәрізді электрон бұлтын s-электрондар деп, ал орбитальдарды s-орбиталь д.с.а.
n- бас квант саны; L- орбиталь квант саны ; m магнит квант саны; s – спин.
Өзара энергиясы жуық электрондар атомның электрондық қабатын түзеді.
Электрондық қабаттар рет нөміріне қарай 1,2,3,4… деп белгіленеді. Np=
электрондық қабаттар саны
Әр қабаттағы орбитальдардың өзіндік энергиясы мен пішіндері болады.
Шар тәрізді электрон бұлтын s-электрондар деп, ал орбитальдарды s-орбиталь д.с.а.
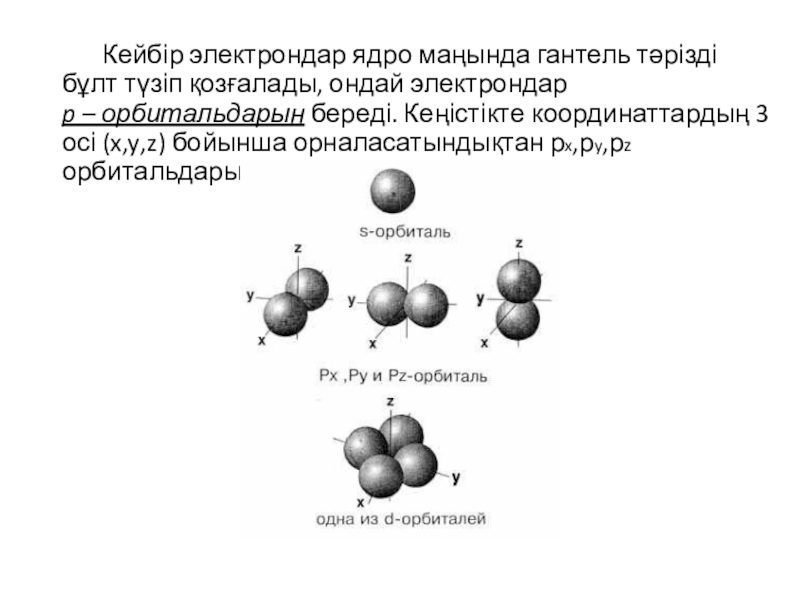
Слайд 4 Кейбір электрондар ядро маңында гантель тәрізді бұлт түзіп қозғалады, ондай электрондар
p – орбитальдарын береді. Кеңістікте координаттардың 3 осі (x,y,z) бойынша орналасатындықтан рx,рy,рz орбитальдары деп бөлінеді
Слайд 6Электрондық бұлттарды толтыру ережесі келесі:
1. Ең алдымен элемент атомында қанша электрон
бар екендігін анықтап алу. Ол үшін сол элементтің ядро зарядын білсек болғаны, ол Д.И. Менделеевтің периодтық жүйедегі элементтің реттік нөміріне тең. Реттік нөмірі (ядродағы протон саны) барлық атомдағы электрон санына тең.
2. Бар электронмен 1s – орбитальдан бастап ұяшықтарды толтырамыз. Әрбір ұяшықта 1 не 2 электрон бола алады. Бір ұяшықта орналасқан
екі электронды қарама – қарсы бағдаршамен
белгілейді. (Хунд ережесі)
3. Элементтің электрондық формуласын жазамыз.
2. Бар электронмен 1s – орбитальдан бастап ұяшықтарды толтырамыз. Әрбір ұяшықта 1 не 2 электрон бола алады. Бір ұяшықта орналасқан
екі электронды қарама – қарсы бағдаршамен
белгілейді. (Хунд ережесі)
3. Элементтің электрондық формуласын жазамыз.
Слайд 8Ұяшықтарды толтыру тізбегі: 1s 2s 2p 3s 3p 4s 3d 4p 5s
4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
Клечковский ережесі
Слайд 10Үйге:
§ 57 Атомдардағы электрондардың қозғалысы.
Есептер мен жаттығулар жинағы: 104-105 бет
5-56, 5-57, 5-67, 5-68 жаттығуларды орындау