Н2 + F2 = 2HF
H2 + Cl2 = 2HCl
H2 + Br2 = 2HBr
H2 + I2 = 2HI
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему 23. Урок по теме Соединения галогенов
Содержание
- 1. 23. Урок по теме Соединения галогенов
- 2. Галогеноводородные кислоты
- 3. Слайд 3
- 4. Получение хлороводородаВ промышленности:H2 + Cl2 = 2HClВ лаборатории:NaCl + H2SO4 = NaHSO4 + HCl
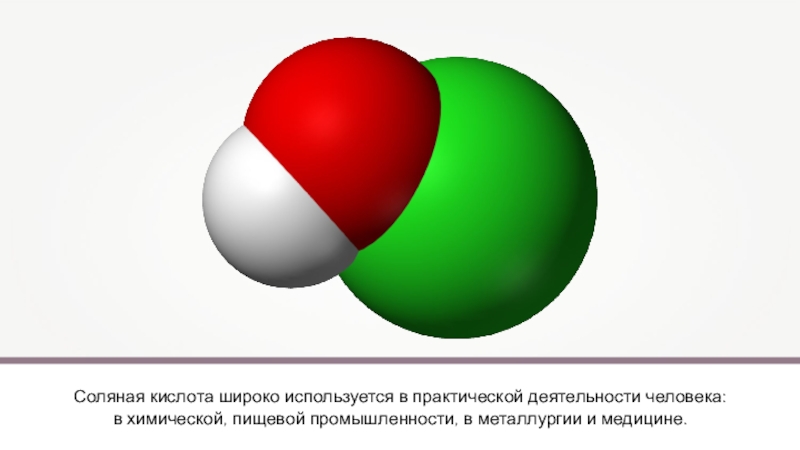
- 5. Соляная кислота — это бесцветная жидкость, которая дымится на воздухе. Соляная кислота тяжелее воды.
- 6. Химические свойства соляной кислотыВзаимодействие с металлами:6HCl +
- 7. Слайд 7
- 8. Галогеноводородные кислоты образуют соли: фториды, хлориды, бромиды и йодиды. Большинство таких солей хорошо растворимы в воде.
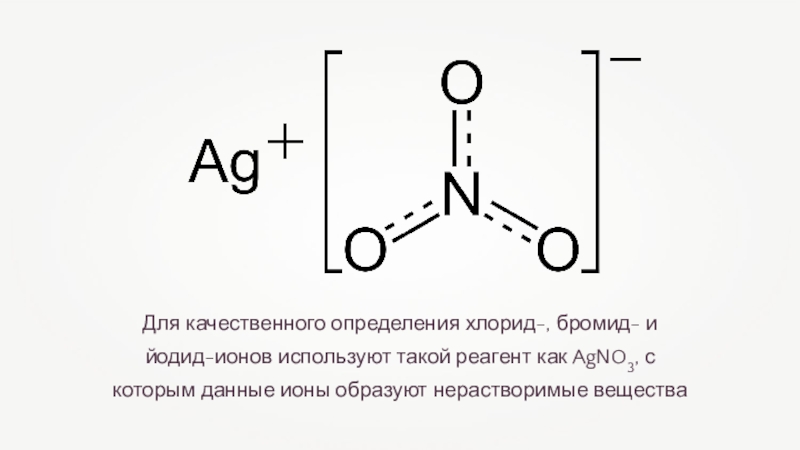
- 9. Для качественного определения хлорид-, бромид- и йодид-ионов
- 10. При взаимодействии хлоридов (и самой соляной кислоты)
- 11. Для определения ионов фтора чаще всего используют
- 12. Ввиду большой реакционной способности галогенов в природе они встречаются исключительно в виде соединений.
- 13. Слайд 13
- 14. Слайд 14
- 15. Слайд 15
- 16. Слайд 16
Слайд 1
Взаимодействие галогенов с водородом
Галогеноводороды — бесцветные газы, с резким запахом, токсичны.
Слайд 4
Получение хлороводорода
В промышленности:
H2 + Cl2 = 2HCl
В лаборатории:
NaCl + H2SO4 =
Слайд 5Соляная кислота — это бесцветная жидкость, которая дымится на воздухе. Соляная
Слайд 6
Химические свойства соляной кислоты
Взаимодействие с металлами:
6HCl + 2Al = 2AlCl3 +
Взаимодействие с основными оксидами:
2HCl + CaO = CaCl2 + H2O
Взаимодействие с основаниями:
HCl + NaOH = NaCl + H2O
Взаимодействие с солями:
2HCl + K2CO3 = 2KCl + H2O + CO2↑
Слайд 8Галогеноводородные кислоты образуют соли: фториды, хлориды, бромиды и йодиды. Большинство таких
в воде.
Слайд 9Для качественного определения хлорид-, бромид- и йодид-ионов используют такой реагент как
Слайд 10При взаимодействии хлоридов (и самой соляной кислоты)
с нитратом серебра образуется
Ag+ + Cl- = AgCl↓
При взаимодействии бромоводородной кислоты и её солями и йодоводородной кислоты и её солями с нитратом серебра также образуются осадки, но только жёлтого цвета, которые различаются оттенками.
Ag+ + Br- = AgBr↓
Слайд 11Для определения ионов фтора чаще всего используют растворимые соли кальция, в
Ca2+ + 2F- = CaF2↓
Взаимодействие фтороводородной кислоты с оксидом кремния:
SiO2+4HF = SiF4↑ + 2H2O