- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Уравнение состояния идеального газа -тест
Содержание
- 1. Уравнение состояния идеального газа -тест
- 2. 1.Назови макроскопические параметры:Масса, давление, объем, температурадавление, объем, температура
- 3. К макроскопическим параметрам идеального газа относятся: давление, объем и температура! P, V, T
- 4. Молодец! Переходи к следующему вопросу
- 5. Неправильно!Вспомни теорию!
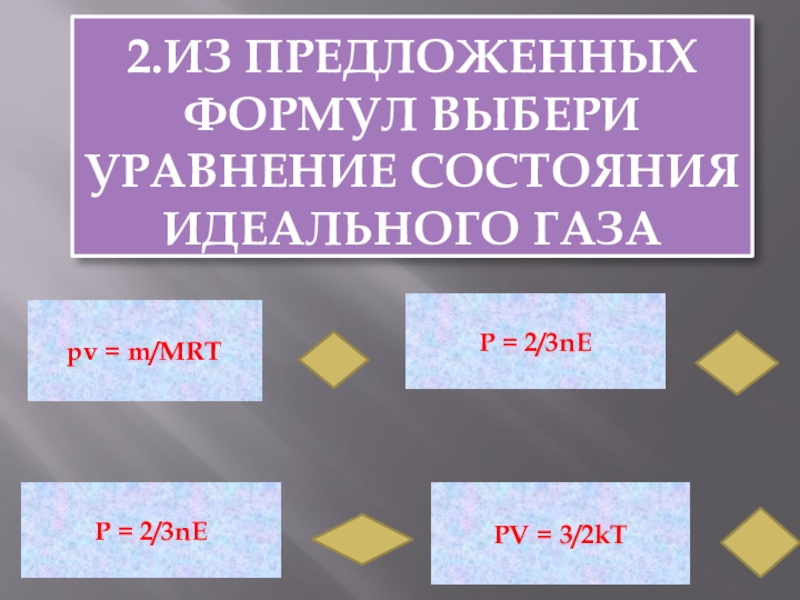
- 6. 2.Из предложенных формул выбери уравнение состояния идеального газаpv = m/MRTP = 2/3nEP = 2/3nEPV = 3/2kT
- 7. pv = m/MRT!Уравнением состояния идеального газа называется зависимость между макроскопическими параметрами: давлением, объемом и температурой!
- 8. Переходи к следующему вопросу Молодец!
- 9. Повтори теорию! Неправильно!
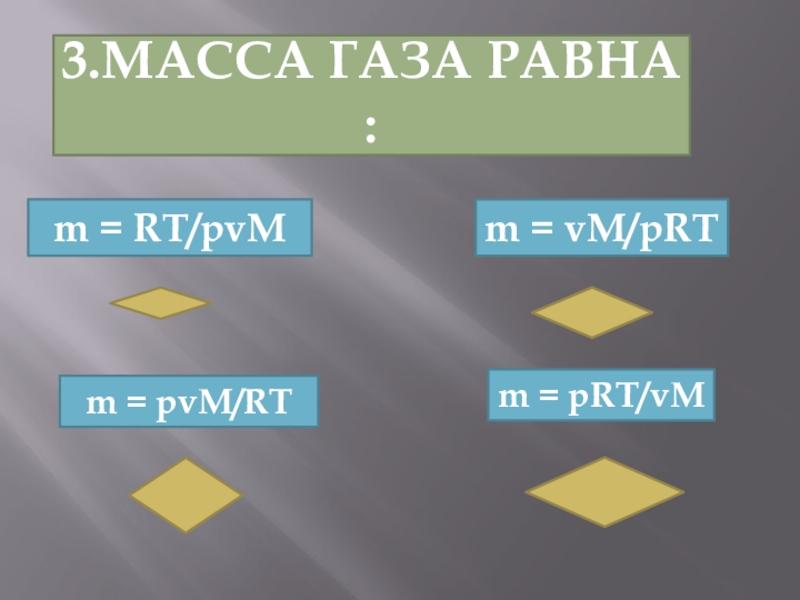
- 10. 3.Масса газа равна :m = RT/pvMm = vM/pRTm = pvM/RTm = pRT/vM
- 11. m = pRT/vMЧтобы выразить неизвестную величину из
- 12. переходи к следующему вопросуМолодец!
- 13. Повтори теорию! Неправильно!
- 14. 4.Универсальная газовая постоянная равна:6,022 *10 23 моль-11,38 * 10 – 23Дж/К 8,31 Дж/ (моль*К)
- 15. k NA = RУниверсальной газовой постоянной называется
- 16. переходи к следующему вопросуМолодец!
- 17. Повтори теорию! Неправильно!
- 18. 5.Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называется… изобарныйизохорныйизотермический
- 19. pv = constСогласно уравнению состояния газа в
- 20. переходи к следующему вопросуМолодец!
- 21. Повтори теорию! Неправильно!
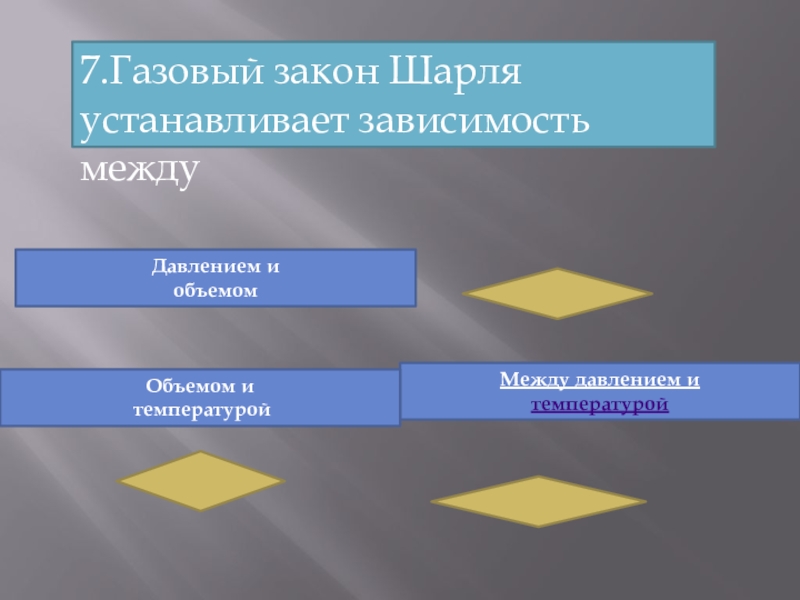
- 22. 7.Газовый закон Шарля устанавливает зависимость междуДавлением и объемомМежду давлением и температуройОбъемом и температурой
- 23. p/T = constПроцесс изменения состояния термодинамической системы при постоянном объеме называют изохорным.Газовый закон Шарля.V = const.
- 24. Повтори теорию! Неправильно!
- 25. Тест окончен , спасибо !
1.Назови макроскопические параметры:Масса, давление, объем, температурадавление, объем, температура
Слайд 21.Назови макроскопические параметры:
Масса, давление, объем, температура
давление, объем, температура
Слайд 3К макроскопическим параметрам идеального газа относятся: давление, объем и температура! P, V,
T
Слайд 62.Из предложенных формул выбери уравнение состояния идеального газа
pv = m/MRT
P =
2/3nE
P = 2/3nE
PV = 3/2kT
Слайд 7pv = m/MRT
!
Уравнением состояния идеального газа называется зависимость между макроскопическими параметрами:
давлением, объемом и температурой!
Слайд 11m = pRT/vM
Чтобы выразить неизвестную величину из уравнения Менделеева – Клапейрона,
умножь левую и правую часть уравнения на знаменатель (М), получишь: рvM = mRT, найди неизвестный множитель, разделив произведение на известные множители.
Слайд 144.Универсальная газовая постоянная равна:
6,022 *10 23 моль-1
1,38 * 10 – 23Дж/К
8,31 Дж/ (моль*К)
Слайд 15k NA = R
Универсальной газовой постоянной называется произведение числа Авогадро и
постоянной Больцмана: 6,02 * 1023 * 1,38 * 10 -23
Слайд 185.Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называется…
изобарный
изохорный
изотермический
Слайд 19pv = const
Согласно уравнению состояния газа в любом состоянии с неизменной
температурой произведение давления газа на его объем остается постоянным. Процесс изотермический.
T = const
T = const
Слайд 227.Газовый закон Шарля устанавливает зависимость между
Давлением и
объемом
Между давлением и
температурой
Объемом
и
температурой
температурой
Слайд 23p/T = const
Процесс изменения состояния термодинамической системы при постоянном объеме называют
изохорным.
Газовый закон Шарля.
V = const.
Газовый закон Шарля.
V = const.