- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по физике на тему Решение задач повышенной трудности по молекулярной физике
Содержание
- 1. Презентация по физике на тему Решение задач повышенной трудности по молекулярной физике
- 2. Система знаний по разделу «Молекулярная физика и термодинамика»
- 3. Слайд 3
- 4. Группы задач части 1 и части 21.Задачи на воспроизведение теоретического материала;2.Графические задачи;3.Расчетные задачи.
- 5. Задача 1.1.Учительница вошла в класс. Ученик,сидящий за
- 6. РешениеЗапах духов появляется за счет испарения эфирных
- 7. Задача 1.2.Используя первый закон термодинамики, установите соответствие
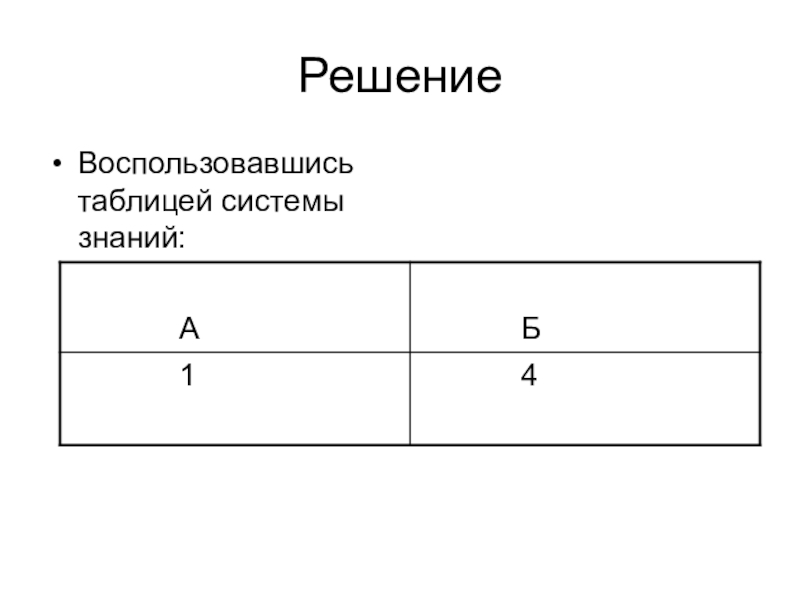
- 8. РешениеВоспользовавшись таблицей системы знаний:
- 9. Графические задачи Задача 1.3.Как изменится давление идеального
- 10. РешениеЕсли через начало координат и каждую из
- 11. Задача 1.4.Идеальный газ сначала охлаждается при постоянном
- 12. РешениеПоскольку газ вначале охлаждается при постоянном давлении,
- 13. Расчетные задачи. Задача 1.5.Какое количество теплоты надо
- 14. Задания повышенного уровня части 2.Первая группа: 1
- 15. 2 тип-на первый закон термодинамики -устанавливается вид
- 16. Задачи 1 типа.Задача 2.1.В колбах одинакового объема
- 17. Задача 2.2.На рисунке показан график изотермического расширения
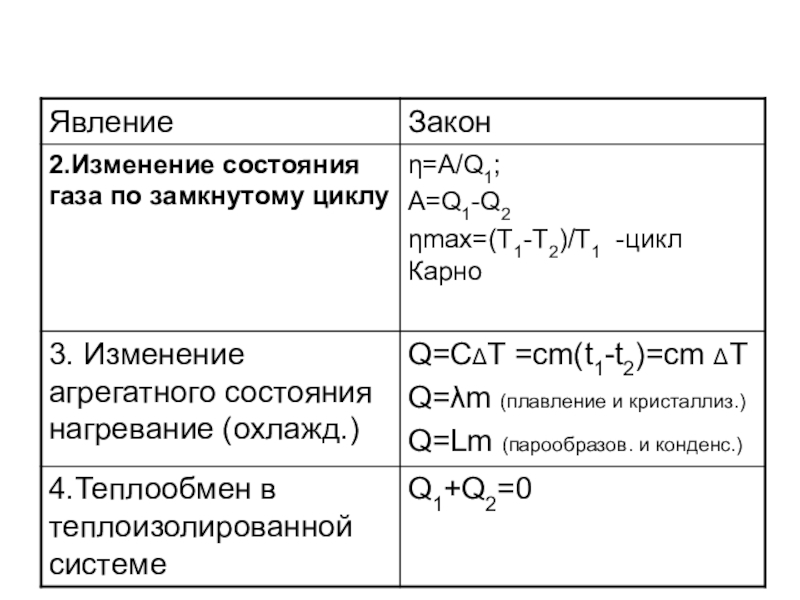
Система знаний по разделу «Молекулярная физика и термодинамика»
Слайд 4Группы задач части 1 и части 2
1.Задачи на воспроизведение теоретического материала;
2.Графические
задачи;
3.Расчетные задачи.
3.Расчетные задачи.
Слайд 5Задача 1.1.
Учительница вошла в класс. Ученик,сидящий за последней партой,почувствовал запах ее
духов через 10 с.Скорость распространения духов в комнате определяется в основном скоростью:
1) испарения; 2)диффузии; 3)броуновского движения;
4) конвекционного переноса воздуха
1) испарения; 2)диффузии; 3)броуновского движения;
4) конвекционного переноса воздуха
Слайд 6Решение
Запах духов появляется за счет испарения эфирных масел с поверхности одежды
и тела, однако ученик находится на последней парте,поэтому это явление не основное. Диффузия -процесс медленный. Броуновское движение здесь не проявляется.Следовательно такая существенная скорость распространения запаха духов связана с явлением конвекционного переноса воздуха. Правильный ответ 4
Слайд 7Задача 1.2.
Используя первый закон термодинамики, установите соответствие между описанными в первом
столбце особенностями изопроцесса в идеальном газе и его названием.
Слайд 9Графические задачи
Задача 1.3.
Как изменится давление идеального газа при переходе из состояния
1 в состояние 2 ?
1.увеличится;
2.уменьшится;
3.останется неизменным;
4.ответ неоднозначен.
1.увеличится;
2.уменьшится;
3.останется неизменным;
4.ответ неоднозначен.
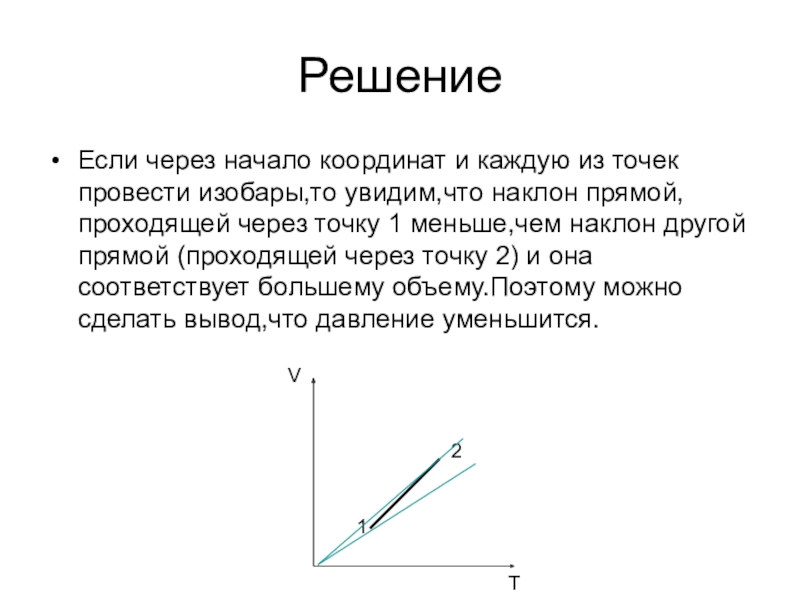
Слайд 10Решение
Если через начало координат и каждую из точек провести изобары,то увидим,что
наклон прямой,проходящей через точку 1 меньше,чем наклон другой прямой (проходящей через точку 2) и она соответствует большему объему.Поэтому можно сделать вывод,что давление уменьшится.
Слайд 11Задача 1.4.
Идеальный газ сначала охлаждается при постоянном давлении,потом его давление увеличивается
при постоянном объеме,затем при постоянной температуре давление уменьшается до первоначального значения. Какой из графиков в координатных осях p-Vсоответствует этим изменениям состояния газа?
1
Слайд 12Решение
Поскольку газ вначале охлаждается при постоянном давлении, то ответ 2) исключаем,
так как на нем участок постоянного давления( линия, параллельная оси V) лежит не в начале и не в конце процесса, а в его середине. На втором этапе давление увеличивалось при постоянном объеме. Этому условию удовлетворяет любая из оставшихся кривых. На третьем этапе давление уменьшается при постоянной температуре до первоначального значения. В ответах 3) и 4) нет участков, соответствующих изотермам, следовательно, варианты 3) и 4) не удовлетворяют условию задачи. Для процесса 1) имеем соответствие с законом Бойля-Мариотта, где при изотермическом процессе с ростом объема давление уменьшается. Эта зависимость описывается спадающей ветвью гиперболы. Таким образом, правильным ответом является график 1).
Слайд 13Расчетные задачи.
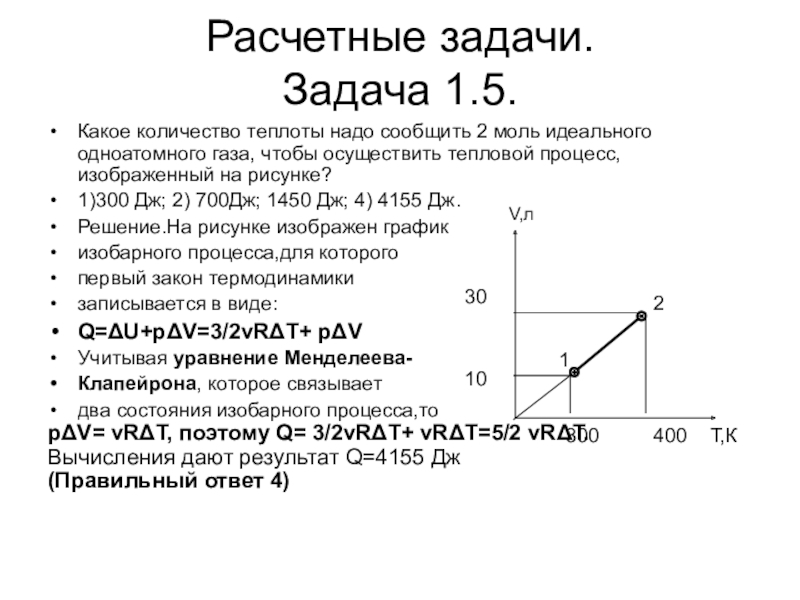
Задача 1.5.
Какое количество теплоты надо сообщить 2 моль идеального одноатомного
газа, чтобы осуществить тепловой процесс, изображенный на рисунке?
1)300 Дж; 2) 700Дж; 1450 Дж; 4) 4155 Дж.
Решение.На рисунке изображен график
изобарного процесса,для которого
первый закон термодинамики
записывается в виде:
Q=ΔU+рΔV=3/2vRΔT+ рΔV
Учитывая уравнение Менделеева-
Клапейрона, которое связывает
два состояния изобарного процесса,то
рΔV= vRΔT, поэтому Q= 3/2vRΔT+ vRΔT=5/2 vRΔT.
Вычисления дают результат Q=4155 Дж
(Правильный ответ 4)
1)300 Дж; 2) 700Дж; 1450 Дж; 4) 4155 Дж.
Решение.На рисунке изображен график
изобарного процесса,для которого
первый закон термодинамики
записывается в виде:
Q=ΔU+рΔV=3/2vRΔT+ рΔV
Учитывая уравнение Менделеева-
Клапейрона, которое связывает
два состояния изобарного процесса,то
рΔV= vRΔT, поэтому Q= 3/2vRΔT+ vRΔT=5/2 vRΔT.
Вычисления дают результат Q=4155 Дж
(Правильный ответ 4)
V,л
T,К
1
2
10
30
300
400
Слайд 14Задания повышенного уровня части 2.
Первая группа:
1 тип-на уравнение состояния
-выделяется газ и его характеристики;
-выделяются начальное и последующее состояния газа с соответствующими характеристиками;
-записывается основное уравнение кинетической теории газов (или закон Менделеева-Клапейрона)
-выделяются начальное и последующее состояния газа с соответствующими характеристиками;
-записывается основное уравнение кинетической теории газов (или закон Менделеева-Клапейрона)
Слайд 152 тип-на первый закон термодинамики
-устанавливается вид процесса перехода газа из начального
состояния в конечное;
-записывается уравнение первого закона термодинамики для изопроцессов.
-записывается уравнение первого закона термодинамики для изопроцессов.
Слайд 16Задачи 1 типа.
Задача 2.1.
В колбах одинакового объема находятся аргон и воздух
при нормальном атмосферном давлении и комнатной температуры. Каково отношение массы аргона в первой колбе к массе воздуха во второй. Ответ округлите до десятых.
Решение. Аргон и воздух различаются молярной массой и,по условию задачи, массой.Массы газов можно выразить из уравнений Менделеева-Клапейрона для каждого газа: m1=pVµ1/RT и m2=pVµ2/RT
Поэтому: m1/ m2 =µ1/ µ2
Вычисления дают результат µ1/ µ2 =0,04/0,029=1,38~1,4
Ответ
Решение. Аргон и воздух различаются молярной массой и,по условию задачи, массой.Массы газов можно выразить из уравнений Менделеева-Клапейрона для каждого газа: m1=pVµ1/RT и m2=pVµ2/RT
Поэтому: m1/ m2 =µ1/ µ2
Вычисления дают результат µ1/ µ2 =0,04/0,029=1,38~1,4
Ответ
1
,
4
Слайд 17Задача 2.2.
На рисунке показан график изотермического расширения водорода. Масса водорода 0,04
кг. Определите его температуру. Ответ округлите до целого числа.
Решение. Температуру газа можно определить из уравнения состояния:
pV=mRT/ µ => T=pVµ/mR
При изотермическом процессе
температура во всех состояниях
одна и та же, поэтому на графике
можем выбрать любую точку, например,
объем 0,1 м3 и давление 50*104 Па.
Учитывая,что молярная масса водорода
0,002 кг/моль,
находим Т=300,8~301 К
Ответ
Решение. Температуру газа можно определить из уравнения состояния:
pV=mRT/ µ => T=pVµ/mR
При изотермическом процессе
температура во всех состояниях
одна и та же, поэтому на графике
можем выбрать любую точку, например,
объем 0,1 м3 и давление 50*104 Па.
Учитывая,что молярная масса водорода
0,002 кг/моль,
находим Т=300,8~301 К
Ответ
p, 104 Па
V,м3
0
0,2
0,4
0,6
20
40
60
3
0
1
К