- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Газовые законы
Содержание
- 1. Газовые законы
- 2. Цели урока:Усвоение и понимание учащимися понятий: изопроцесс,
- 3. ИзопроцессыИзопроцессы–процессы, протекающие при неизменном значении одного из
- 4. Уравнение Менделеева - Клапейрона
- 5. Газовые законыИзотермический процессИзобарный процессИзохорный процесс
- 6. Изотермический процессПроцесс изменения состояния термодинамической системы макроскопических
- 7. Для поддержания температуры газа постоянной необходимо, чтобы
- 8. Роберт БОЙЛЬ (1627-1691), английский химик
- 9. Эдм Мариотт (1620-1684) Французский физик, член
- 10. Закон Бойля-МариоттаРоберт Бойль (англ.) – 1662гЭ. Мариотт
- 11. Изотермический процесс.pV=
- 12. Закон справедлив для любых газов и их
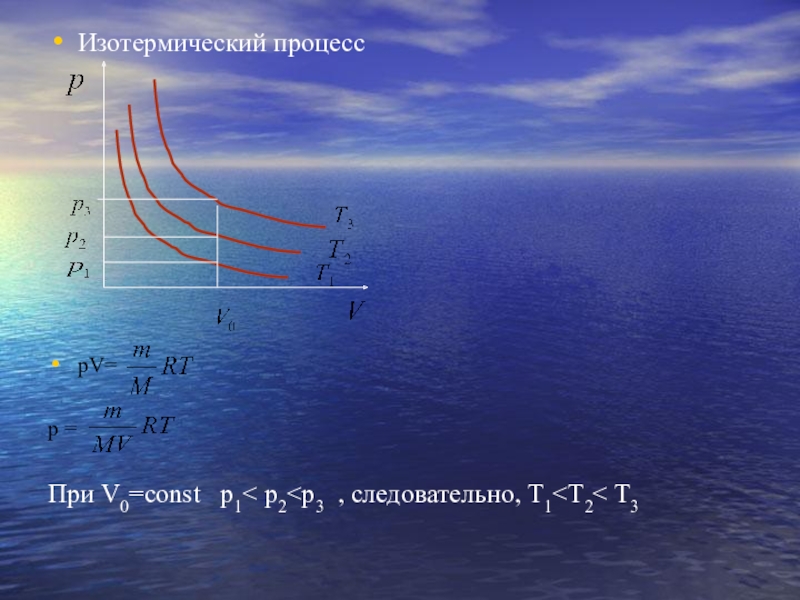
- 13. Изотермический процессpV=р =При V0=const p1< p2
- 14. Давление газа зависит от числа ударов молекул
- 15. Изохорный процесс.Процесс изменения состояния термодинамической системы макроскопических
- 16. Шарль, Жак Александр Сезар ШАРЛЬ
- 17. Закон ШарляДля данной массы газа отношение давления
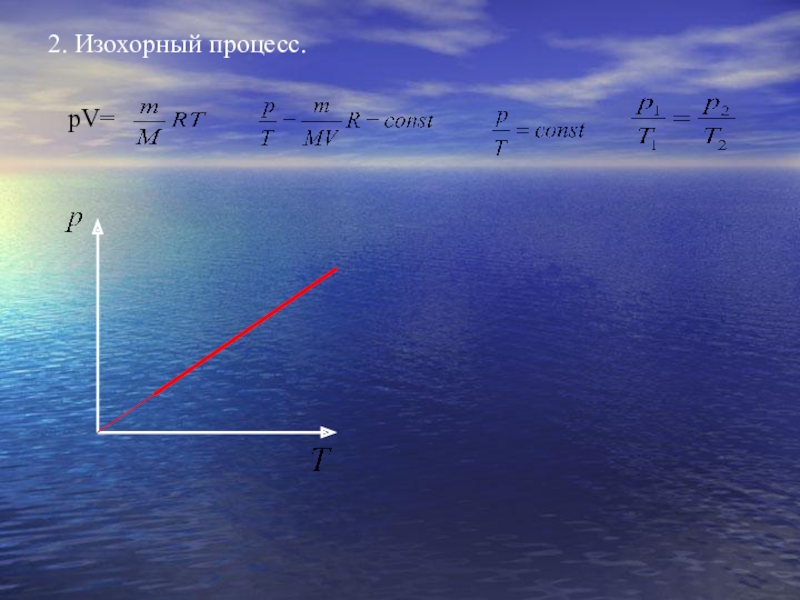
- 18. 2. Изохорный процесс. pV=
- 19. Давление газа зависит от числа
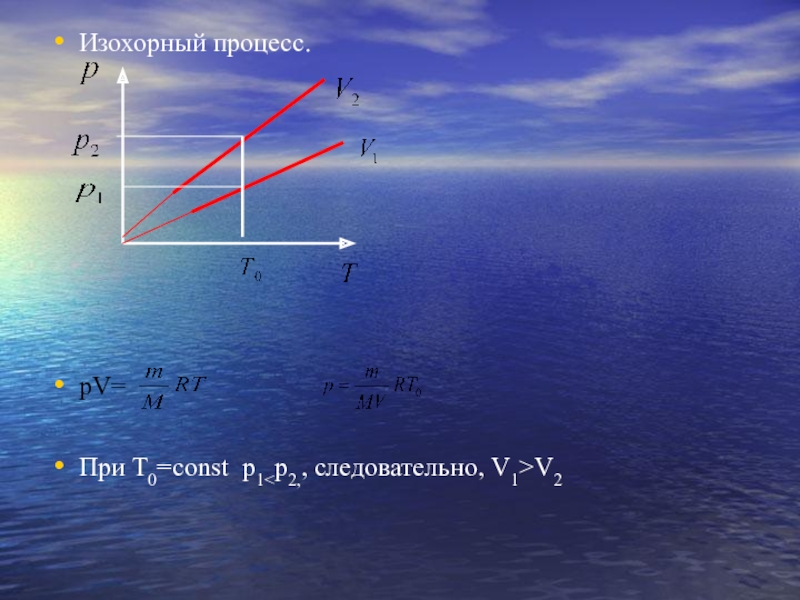
- 20. Изохорный процесс.рV=При Т0=const p1V2
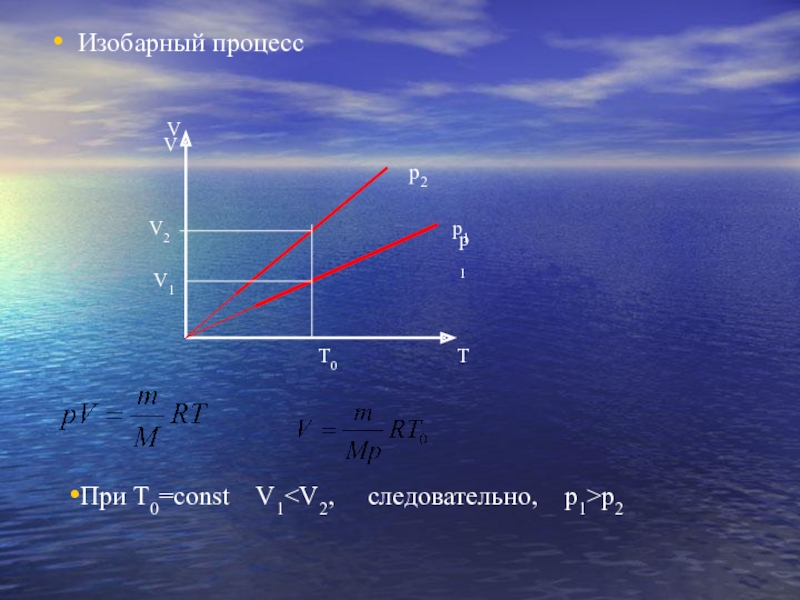
- 21. Изобарный процессИзобарный процесс – процесс изменения состояния
- 22. Гей –Люсак Жозеф Луи Французский
- 23. Закон Гей – Люссака Ж. Гей –
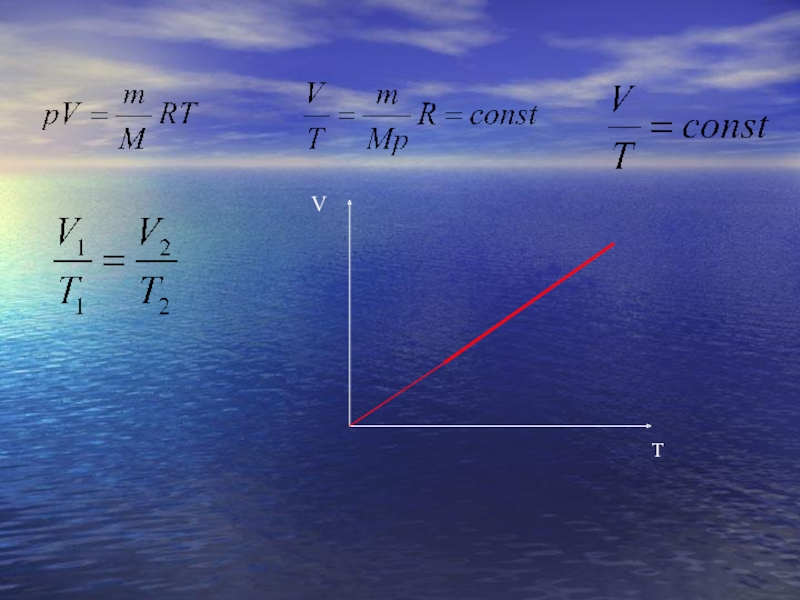
- 24. VT
- 25. Изобарный процессVVTT0V2V1p1p1p2При Т0=const V1p2
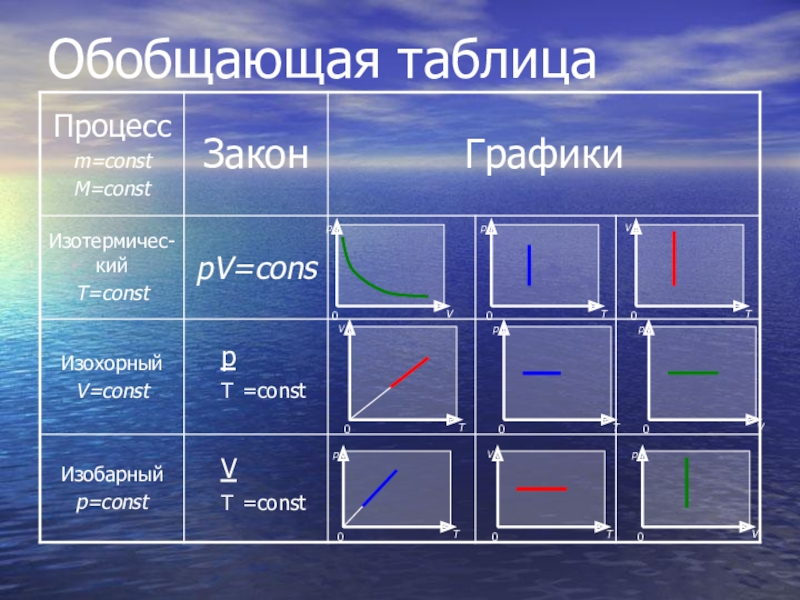
- 26. Обобщающая таблица
- 27. Проверь полученные знания.
- 28. Задание 1 Вариант 1изотермическом процессе?Вариант 2 изобарном процессе?Какой из макроскопических параметров остается постоянным при …
- 29. Задание 2Вариант 1Какая из формул описывает законВариант 2Бойля-Мариотта?Гей-Люссака?
- 30. Слайд 30
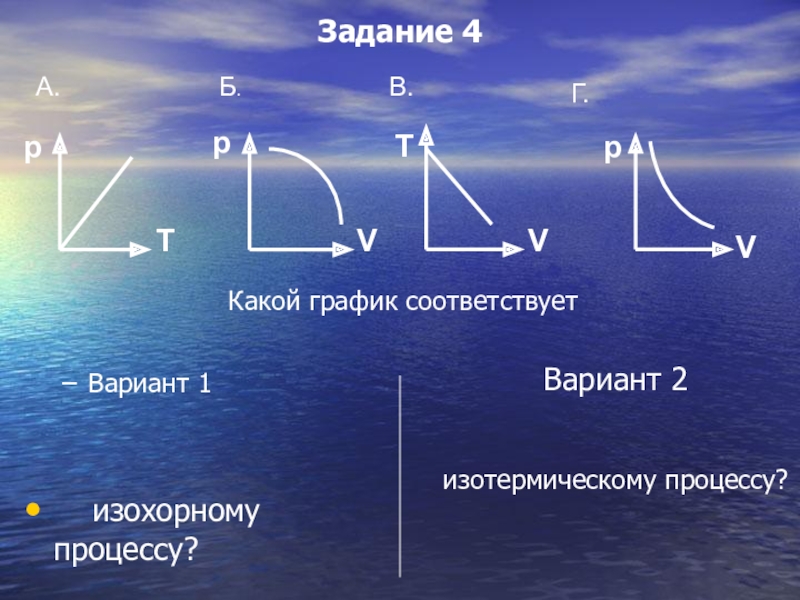
- 31. Вариант 1 изохорному процессу?Вариант 2изотермическому процессу?Задание 4Какой график соответствует
- 32. Задание 5 Вариант 1Вариант 2В.p На каком из
- 33. Проверь правильность своих ответов
- 34. Оцени свои результаты
Цели урока:Усвоение и понимание учащимися понятий: изопроцесс, изотермический, изобарный, изохорный, закон Бойля-Мариотта, Гей-Люссака, Шарля, изотерма, изохора, изобара. 2. Развитие умений анализировать, выделять главное, сравнивать, строить аналогии.Воспитание умения самоорганизации, самоанализа, чувства коллективизма.
Слайд 2Цели урока:
Усвоение и понимание учащимися понятий: изопроцесс, изотермический, изобарный, изохорный, закон
Бойля-Мариотта, Гей-Люссака, Шарля, изотерма, изохора, изобара.
2. Развитие умений анализировать, выделять главное, сравнивать, строить аналогии.
Воспитание умения самоорганизации, самоанализа, чувства коллективизма.
2. Развитие умений анализировать, выделять главное, сравнивать, строить аналогии.
Воспитание умения самоорганизации, самоанализа, чувства коллективизма.
Слайд 3Изопроцессы
Изопроцессы–процессы, протекающие при неизменном значении одного из параметров
“изо” - постоянство
Слайд 6Изотермический процесс
Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре
называют изотермическим.
«термо» - (греч.) температура
«термо» - (греч.) температура
Слайд 7Для поддержания температуры газа постоянной необходимо, чтобы он мог обмениваться теплотой
с большой системой – термостатом. Иначе температура газа будет меняться. Термостатом может служить атмосферный воздух, если температура его заметно не меняется на протяжении всего процесса. Для поддержания теплообмена процесс должен протекать медленно.
Слайд 8 Роберт БОЙЛЬ (1627-1691), английский химик и физик, один из
учредителей Лондонского королевского общества. Сформулировал (1661) первое научное определение химического элемента, ввел в химию экспериментальный метод, положил начало химическому анализу. Способствовал становлению химии как науки. Установил (1662) один из газовых законов (закон Бойля — Мариотта).
Слайд 9 Эдм Мариотт (1620-1684) Французский физик, член Парижской академии наук со
дня ее основания (1666). Был настоятелем монастыря в окрестностях Дижона. Впервые описал слепое пятно в глазу (1668), в 1676 – опыты о зависимости упругости воздуха от давления, вторично дал формулировку закона, открытого и опубликованного Р. Бойлем в 1662 (закон Бойля–Мариотта). Впервые использовал этот закон для определения высоты места по показаниям барометра. Описал многочисленные опыты о течении жидкостей по трубам и действие фонтанов (1686). Изучал также явление удара тел.
Слайд 10Закон Бойля-Мариотта
Роберт Бойль (англ.) – 1662г
Э. Мариотт (франц.) – 1676г
Для газа
данной массы произведение давления газа на его объем постоянно, если температура газа не меняется.
PV = const.
PV = const.
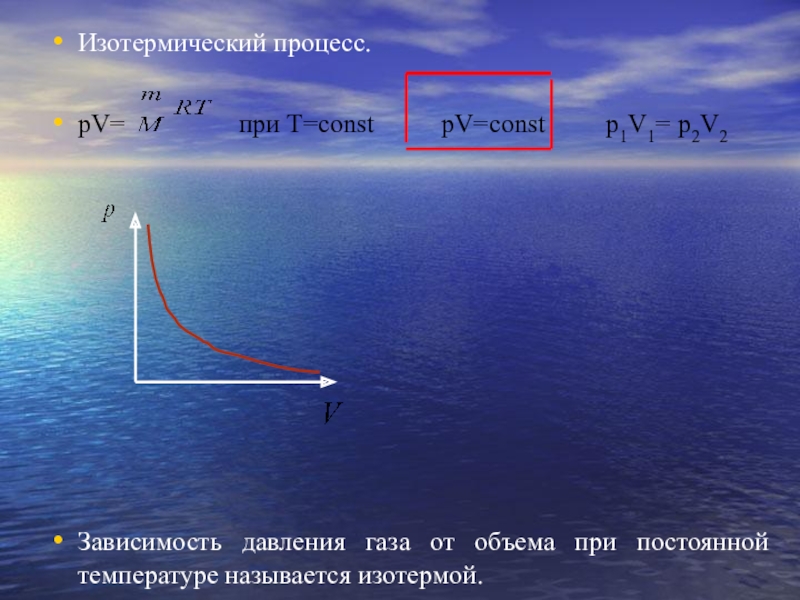
Слайд 11Изотермический процесс.
pV= при
T=const pV=const p1V1= p2V2
Зависимость давления газа от объема при постоянной температуре называется изотермой.
Зависимость давления газа от объема при постоянной температуре называется изотермой.
Слайд 12Закон справедлив для любых газов и их смесей.
Отклонения от этого
закона становятся существенными при давлениях очень высоких (в несколько сот раз больше атмосферного) и при очень низких температурах.
Слайд 14Давление газа зависит от числа ударов молекул о стенки сосуда.
При
сжатии газа объем уменьшается, число ударов увеличивается и, следовательно, давление газа увеличивается.
При расширении газа объем увеличивается, число ударов молекул о стенки сосуда уменьшается и, следовательно, давление газа уменьшается.
При расширении газа объем увеличивается, число ударов молекул о стенки сосуда уменьшается и, следовательно, давление газа уменьшается.
Слайд 15Изохорный процесс.
Процесс изменения состояния термодинамической системы макроскопических тел при постоянном объеме
называют изотермическим.
“хорос”(греч.) - объем
“хорос”(греч.) - объем
Слайд 16Шарль, Жак Александр Сезар
ШАРЛЬ Жак Александр Сезар (1746-1823),
французский физик. Труды связаны с изучением расширения газов. Установил (1787) зависимость давления идеального газа от температуры (Шарля закон). Сразу же после братьев Ж. и Э. Монгольфье построил воздушный шар из прорезиненной ткани и для его наполнения впервые использовал водород. В 1783 совершил полет на этом шаре. Изобрел ряд приборов.
Слайд 17Закон Шарля
Для данной массы газа отношение давления к температуре постоянно, если
объем не меняется.
при V = const
при V = const
Слайд 19 Давление газа зависит от числа ударов молекул о стенки
сосуда.
При повышении температуры скорость
движения молекул увеличивается, число ударов молекул о стенки сосуда увеличивается, и, следовательно, давление повышается.
При понижении температуры скорость
движения молекул уменьшается, число ударов молекул о стенки сосуда уменьшается, и, следовательно, давление понижается.
При повышении температуры скорость
движения молекул увеличивается, число ударов молекул о стенки сосуда увеличивается, и, следовательно, давление повышается.
При понижении температуры скорость
движения молекул уменьшается, число ударов молекул о стенки сосуда уменьшается, и, следовательно, давление понижается.
Слайд 21Изобарный процесс
Изобарный процесс – процесс изменения состояния определенной массы газа при
постоянном давлении.
“барос”(греч.) - давление
Слайд 22Гей –Люсак Жозеф Луи
Французский химик и физик,
член Парижской академии наук (с 1806), её президент в 1822 и 1834. родился в Сен-Леонаре. Окончил Политехническую школу в Париже (1800), где учился К.Л. Бертолле. Работал там же (в 1800-1802 ассистент Бертолле). В 1805-1806 совершал путешествие по Европе вместе со знаменитым немецким естествоиспытателем А. Гумбольдтом. С 1809 проф. химии в Политехнической школе и физики в Сорбонне. С 1832 проф. химии в Ботаническом саду в Париже. Работы относятся к различным областям химии. Изобрёл (1816) термограф и ртутный сифонный переносной барометр. Совместно с Т.Ж. Пелузом получил (1833) нагреванием молочной кислоты лактид. Иностранный почетный чл. Петербургской академии наук (с 1829).
Слайд 23Закон Гей – Люссака
Ж. Гей – Люссак (франц.) 1802
Для данной массы
газа при постоянном давлении отношение объема газа к его температуре постоянно.
Слайд 28Задание 1
Вариант 1
изотермическом процессе?
Вариант 2
изобарном процессе?
Какой из макроскопических параметров
остается постоянным при …
Слайд 31Вариант 1
изохорному процессу?
Вариант 2
изотермическому процессу?
Задание 4
Какой график соответствует
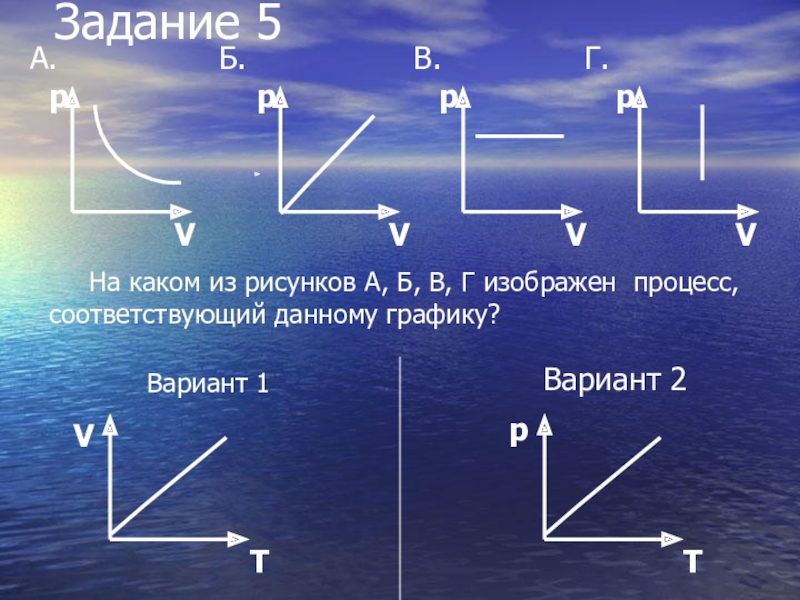
Слайд 32Задание 5
Вариант 1
Вариант 2
В.
p
На каком из рисунков А, Б, В, Г
изображен процесс, соответствующий данному графику?