- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Алканы
Содержание
- 1. Алканы
- 2. Предельные углеводороды (Алканы)Состав алкановвыражается общей формулой СnH2n+2 где n – количество атомов углерода.
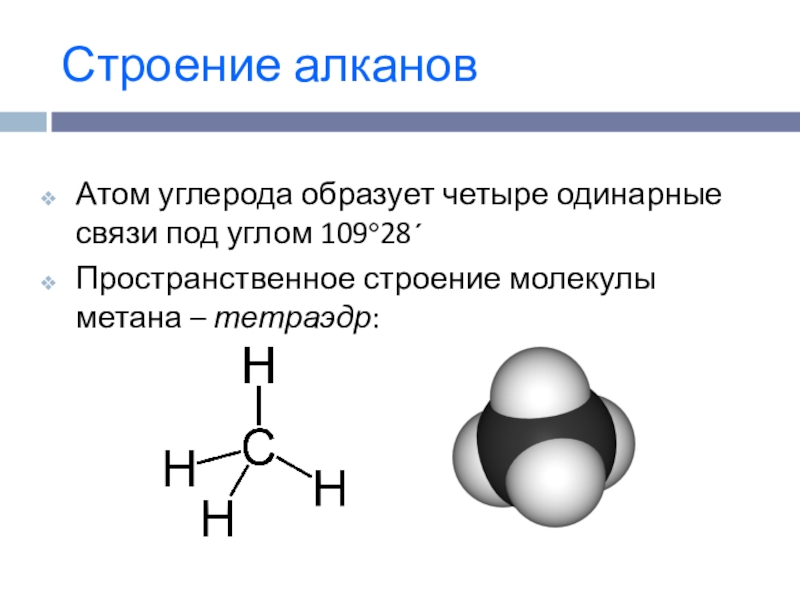
- 3. Строение алкановАтом углерода образует четыре одинарные связи под углом 109º28´Пространственное строение молекулы метана – тетраэдр:
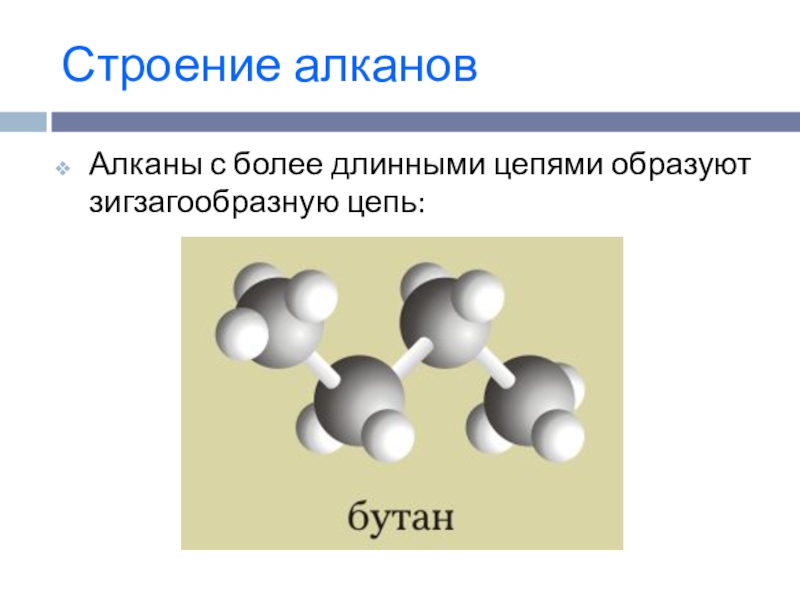
- 4. Строение алкановАлканы с более длинными цепями образуют зигзагообразную цепь:
- 5. Гомологические ряды Гомологи – вещества, имеющие сходное
- 6. Гомологический ряд метана
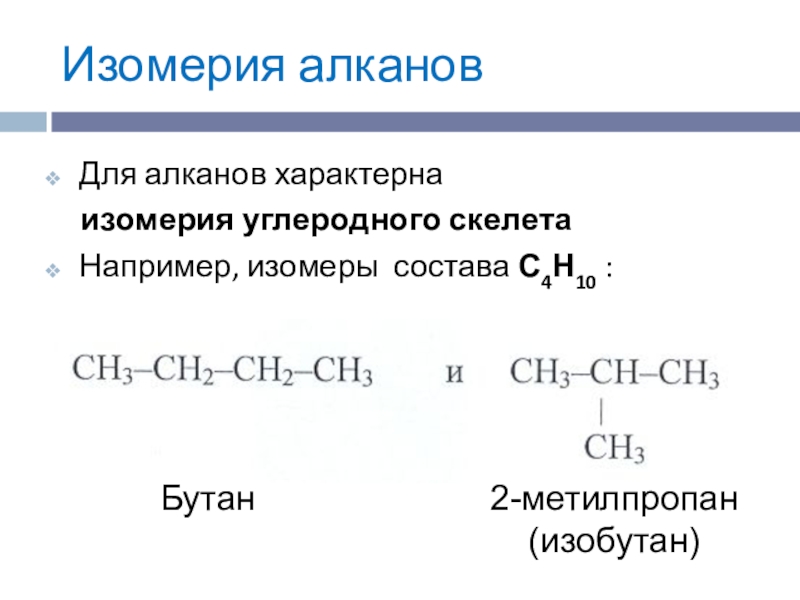
- 7. Изомерия алкановДля алканов характерна изомерия углеродного скелетаНапример, изомеры состава С4Н10 :Бутан 2-метилпропан(изобутан)
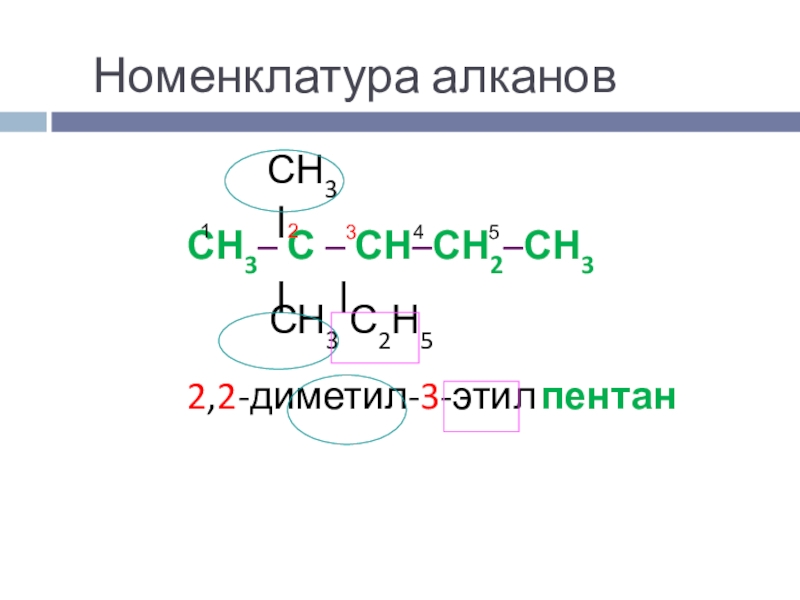
- 8. Номенклатура алканов
- 9. Физические свойства алкановМетан, этан, пропан, бутан –
- 10. Химические свойства алкановРеакция горения:
- 11. Химические свойства алкановРеакция разложения при нагревании без
- 12. Химические свойства алкановРазложение алканов может быть неполным:
- 13. Химические свойства алкановАлканы вступают в реакции замещения:
- 14. Химические свойства алкановАлканы НЕ вступают в реакции присоединения и НЕ окисляются перманганатом калия
- 15. Получение алкановВ промышленности различные предельные углеводороды получают путем термического разделения природных углеводородов – ректификации
- 16. Получение алканов
- 17. Применение алкановГорючееСырьё для получения сажи и водородаСырьё
- 18. Предельные углеводороды (Алканы)Спасибо за внимание, теперь вы знаете об алканах:СоставСтроениеГомологиИзомерыСвойстваПолучениеПрименениеПроверим ?
Предельные углеводороды (Алканы)Состав алкановвыражается общей формулой СnH2n+2 где n – количество атомов углерода.
Слайд 2Предельные углеводороды
(Алканы)
Состав алканов
выражается общей формулой
СnH2n+2
где n
– количество атомов углерода.
Слайд 3Строение алканов
Атом углерода образует четыре одинарные связи под углом 109º28´
Пространственное строение
молекулы метана – тетраэдр:
Слайд 5Гомологические ряды
Гомологи – вещества, имеющие сходное строение, но отличающиеся по
составу
Ближайшие гомологи отличаются друг от друга на группу ( – СН2 – )
Гомологический ряд – ряд последовательных гомологов
Ближайшие гомологи отличаются друг от друга на группу ( – СН2 – )
Гомологический ряд – ряд последовательных гомологов
Слайд 7Изомерия алканов
Для алканов характерна
изомерия углеродного скелета
Например, изомеры состава
С4Н10 :
Бутан
2-метилпропан
(изобутан)
Слайд 9Физические свойства алканов
Метан, этан, пропан, бутан – газы; последующие (до С15Н32)
– жидкости; более тяжёлые углеводороды – твёрдые вещества
В воде практически не растворяются
Электрический ток не проводят
В воде практически не растворяются
Электрический ток не проводят
Слайд 10Химические свойства алканов
Реакция горения:
СН4 + 2О2 →
СО2 + 2Н2О
С3Н8 + 5О2 → 3СО2 + 4Н2О
Смесь метана
с воздухом
взрывоопасна!
С3Н8 + 5О2 → 3СО2 + 4Н2О
Смесь метана
с воздухом
взрывоопасна!
Слайд 11Химические свойства алканов
Реакция разложения при нагревании без доступа воздуха :
СН4
→ С(сажа) + 2Н2
С2Н6 → 2С(сажа)+ 3Н2
С2Н6 → 2С(сажа)+ 3Н2
t
t
Слайд 12Химические свойства алканов
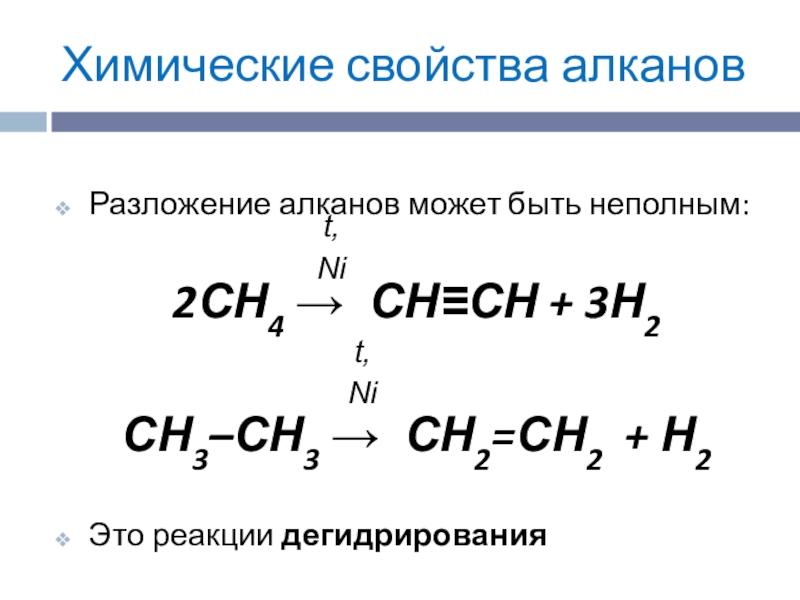
Разложение алканов может быть неполным:
2СН4 → СН≡СН +
3Н2
СН3–СН3 → СН2=СН2 + Н2
Это реакции дегидрирования
СН3–СН3 → СН2=СН2 + Н2
Это реакции дегидрирования
t, Ni
t, Ni
Слайд 13Химические свойства алканов
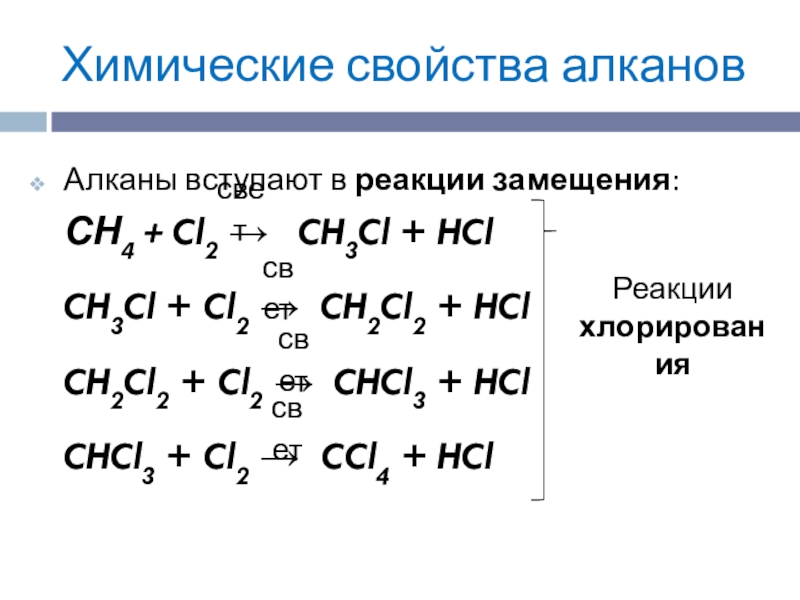
Алканы вступают в реакции замещения:
СН4 + Cl2
→ CH3Cl + HCl
CH3Cl + Cl2 → CH2Cl2 + HCl
CH2Cl2 + Cl2 → CHCl3 + HCl
CHCl3 + Cl2 → CCl4 + HCl
CH3Cl + Cl2 → CH2Cl2 + HCl
CH2Cl2 + Cl2 → CHCl3 + HCl
CHCl3 + Cl2 → CCl4 + HCl
Реакции
хлорирования
свет
свет
свет
свет
Слайд 14Химические свойства алканов
Алканы НЕ вступают в реакции присоединения и НЕ окисляются
перманганатом калия
Слайд 15Получение алканов
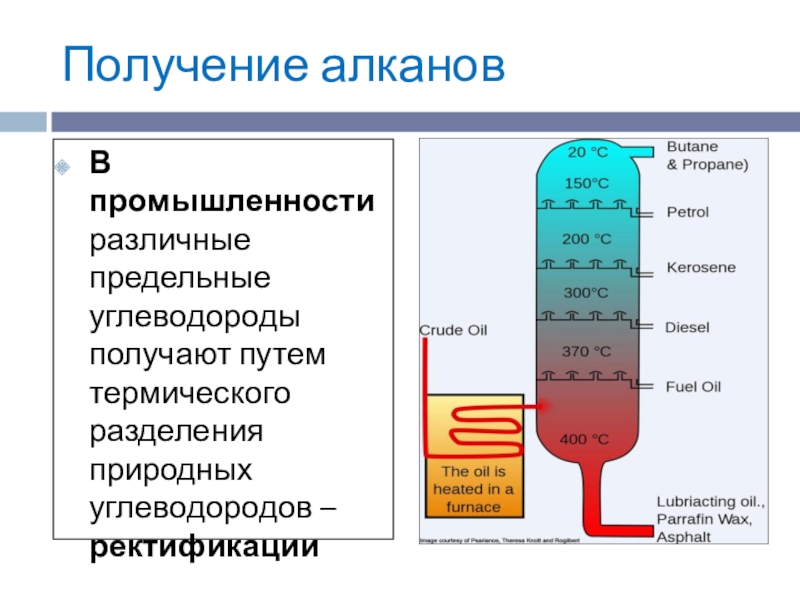
В промышленности различные предельные углеводороды получают путем термического разделения природных
углеводородов – ректификации
Слайд 16Получение алканов
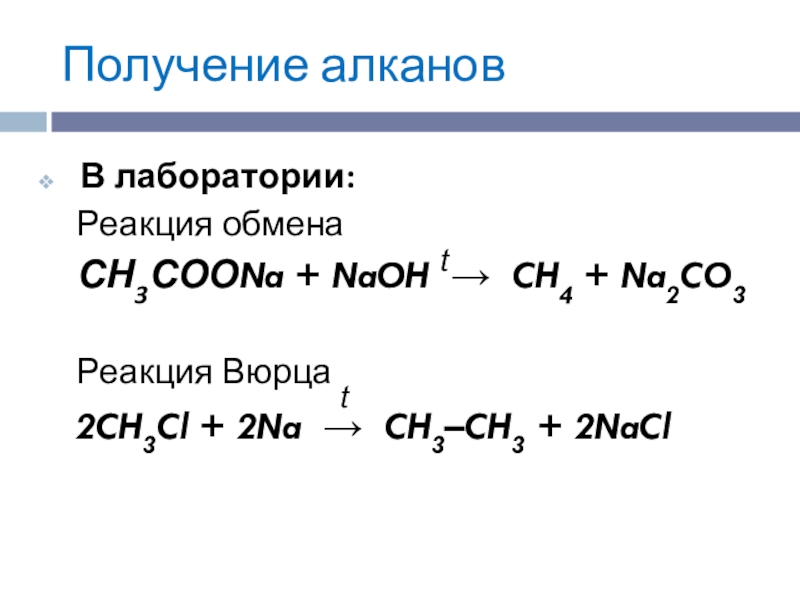
В лаборатории:
Реакция обмена
СН3СООNa + NaOH → CH4 + Na2CO3
Реакция Вюрца
2CH3Cl + 2Na → CH3–CH3 + 2NaCl
t
t
Слайд 17Применение алканов
Горючее
Сырьё для получения сажи и водорода
Сырьё для получения непредельных углеводородов
Сырьё
для получения растворителей, хладагентов и лекарственных препаратов