- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по биологии на тему: Строение и функции белков. (10 класс)
Содержание
- 1. Презентация по биологии на тему: Строение и функции белков. (10 класс)
- 2. Цель урока.Изучить строение белков.Ознакомиться с уровнями организации
- 3. Слайд 3
- 4. Слайд 4
- 5. Химический составОсновные химические элементы, входящие в состав
- 6. Строение аминокислотОбщая формула:
- 7. В нейтральной среде аминокислоты существуют в виде биполярных ионов – цвиттер-ионов.
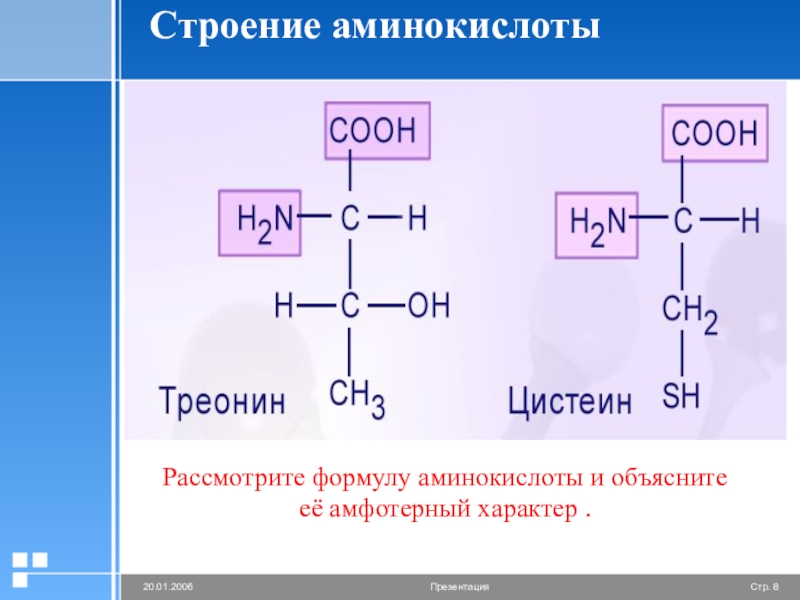
- 8. Строение аминокислотыРассмотрите формулу аминокислоты и объяснитееё амфотерный характер .
- 9. Данилевский Александр Яковлевич.Предположение о том, что белки
- 10. Фишер Эмиль Герман.
- 11. Пептидная связьСоединение молекул аминокислот:Рассмотрите схему образования дипептида.Какие атомы образовали молекулу воды в результате соединения двух аминокислот?
- 12. Образование пептидной связи
- 13. Реакции получения полимеров, которые сопровождаются образованием побочного
- 14. Биуретовая реакция.Приливаем в пробирку 2 мл. раствора
- 15. Полимер, состоящий из аминокислот
- 16. БЕЛКИ. ПРОТЕИНЫ. ПРОТЕИДЫ.Белки – это макромолекулы, биополимеры,
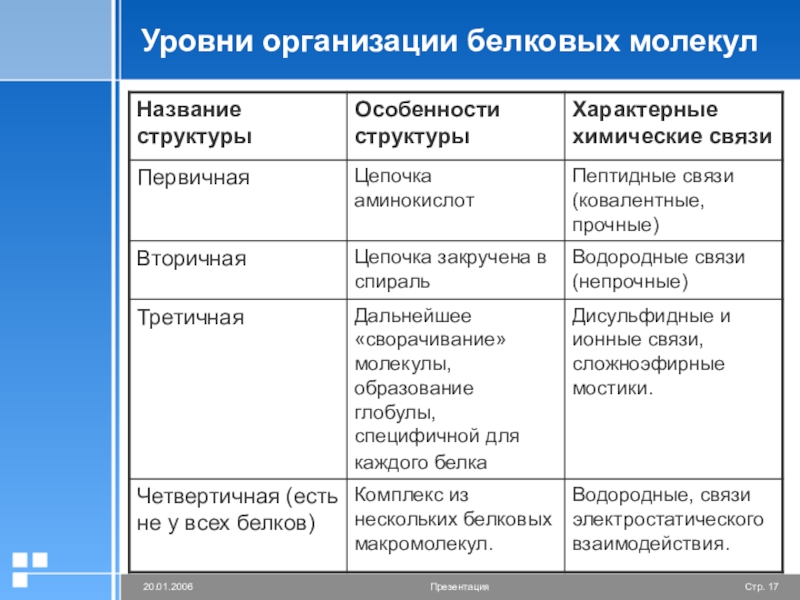
- 17. Уровни организации белковых молекул
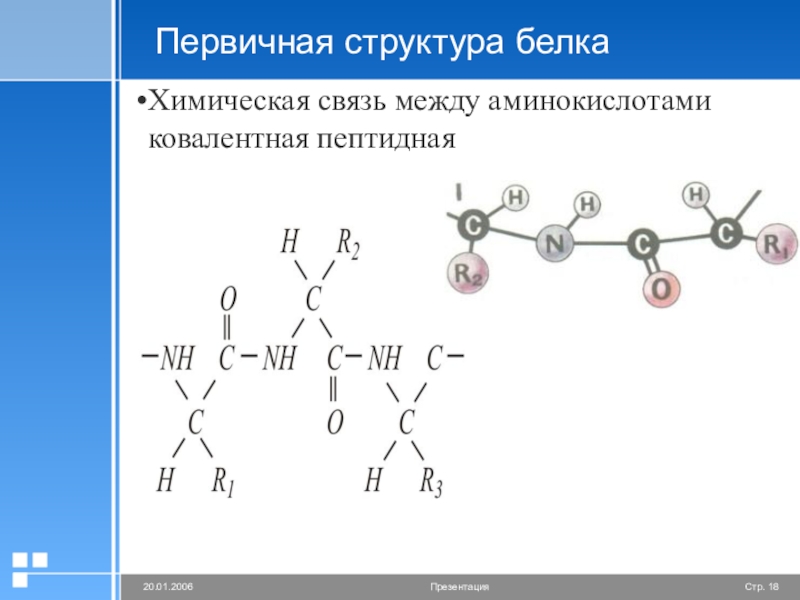
- 18. Первичная структура белкаХимическая связь между аминокислотами ковалентная пептидная
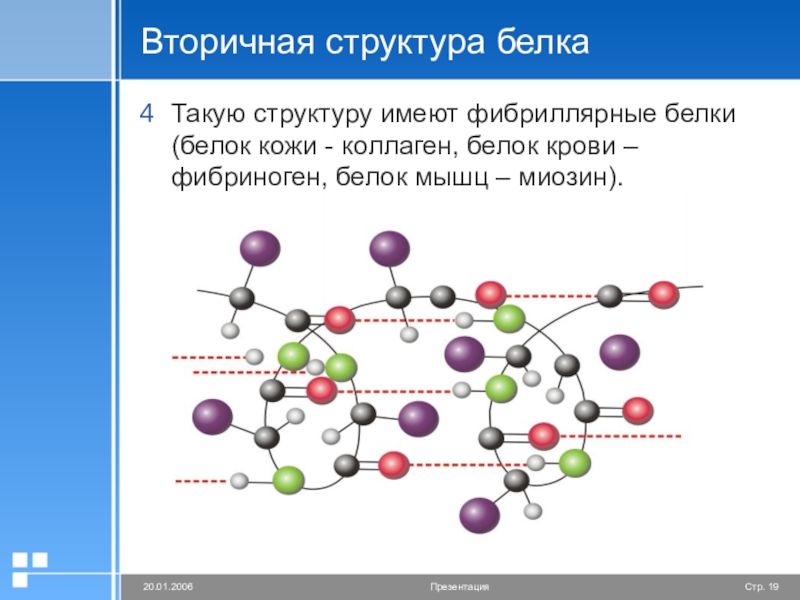
- 19. Вторичная структура белкаТакую структуру имеют фибриллярные белки
- 20. Вторичная структура белка
- 21. В 1951 году Л.Полинг и Р.Кори высказывали
- 22. Типы вторичной структуры белка.Существует 3 типа вторичной
- 23. БЕТА – СКЛАДЧАТОСТЬ.
- 24. Третичная структура белкаЭто многократно скрученная спираль, глобула. Такую структуру имеют глобулярные белки (альбумины, глобулины).
- 25. Четвертичная структура белкаЧетыре глобулы связанные атомом железа имеет белок гемоглобин.
- 26. Моделирование структур белка.
- 27. Свойства белка.
- 28. Денатурация – это изменение вторичной, третичной и
- 29. ГИДРОЛИЗ- ПРОЦЕСС РАЗРУШЕНИЯ ПЕПТИДНЫХ СВЯЗЕЙ БЕЛКОВОЙ МОЛЕКУЛЫ С УЧАСТИЕМ ВОДЫ.
- 30. КИСЛОТНЫЙ ГИДРОЛИЗ ПРОТЕКАЕТ ПРИ ДЕЙСТВИИ 25% РАСТВОРОВ
- 31. Слайд 31
- 32. ГОРЕНИЕ.БЕЛКИ ПРИ СЖИГАНИИ ОБРАЗУЮТ АЗОТ, УГЛЕКИСЛЫЙ ГАЗ,
- 33. КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ.ЭТО ЦВЕТНАЯ РЕАКЦИЯ НА БЕЛКИ,СОДЕРЖАЩИЕ АРОМАТИЧЕСКИЕ
- 34. Свойства белков.Денатурация.Ренатурация.Гидролиз.Горение.Цветные реакции.
- 35. Классификация белков.По растворимости: Водорастворимые
- 36. Функции белков
- 37. Функции белков в клетке
- 38. ПОДВЕДЁМ ИТОГИ УРОКА.
- 39. Какие вещества называются белками?Каковы основные функции белков
- 40. Домашнее задание.Д/З параграф 27. Вопросы 6 – 10.
Слайд 1Биологические полимеры. БЕЛКИ
Жизнь есть способ существования белковых тел, существенным моментом которого
Ф.Энгельс
Слайд 2Цель урока.
Изучить строение белков.
Ознакомиться с уровнями организации белковых молекул.
Рассмотреть свойства белков.
Классифицировать
Показать многообразие функций белков.
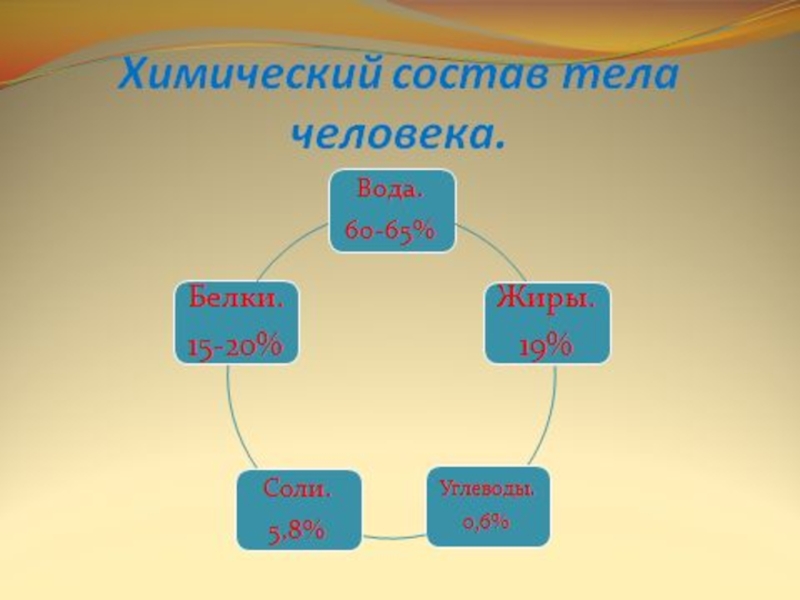
Слайд 5Химический состав
Основные химические элементы, входящие в состав белков
С(углерод) – 50%
O(кислород) –
H(водород) – 6,5-7,3%
N(азот) – 15-18%
S(сера) – 0,2-2,4%
Р(фосфор)
Белки – это полимеры, мономерами которых являются аминокислоты.
Слайд 9
Данилевский Александр Яковлевич.
Предположение о том, что белки состоят из остатков аминокислот,
Слайд 11Пептидная связь
Соединение молекул аминокислот:
Рассмотрите схему образования дипептида.
Какие атомы образовали молекулу воды
результате соединения двух аминокислот?
Слайд 13
Реакции получения полимеров, которые сопровождаются образованием побочного низкомолекулярного продукта, например воды,
Давайте докажем наличие пептидных связей в белке куриного яйца. Проведём биуретовую реакцию.
Слайд 14Биуретовая реакция.
Приливаем в пробирку 2 мл. раствора белка.
Добавляем 2 мл. раствора
Белок окрашивается в красно-фиолетовый цвет.
Слайд 16БЕЛКИ. ПРОТЕИНЫ. ПРОТЕИДЫ.
Белки – это макромолекулы, биополимеры, полипептиды.
Белки – это самые
Протеины – простые белки, состоят только из аминокислот.
Протеиды – сложные белки, кроме аминокислот в состав молекул входит и небелковая часть.
Слайд 19Вторичная структура белка
Такую структуру имеют фибриллярные белки (белок кожи - коллаген,
Слайд 21
В 1951 году Л.Полинг и Р.Кори высказывали предположение, что для белков
Приблизительно через 6 лет предположения подтвердились.
Слайд 22Типы вторичной структуры белка.
Существует 3 типа вторичной структуры.
Альфа- спираль – это
Бета- складчатость – полипептидная цепь собрана в равнозначные складки.
Бета-изгиб – образуется между тремя аминокислотами за счёт водородной связи. Он необходим при образовании третичной структуры белка.
Слайд 24Третичная структура белка
Это многократно скрученная спираль, глобула. Такую структуру имеют глобулярные
Слайд 28
Денатурация – это изменение вторичной, третичной и четвертичной структуры белковой макромолекулы
Если разрушения первичной структуры молекулы не произошло , при наступлении благоприятных условий денатурированный белок может вновь восстановить свою форму. Этот процесс называется ренатурацией.
Слайд 30
КИСЛОТНЫЙ ГИДРОЛИЗ ПРОТЕКАЕТ ПРИ ДЕЙСТВИИ 25% РАСТВОРОВ СЕРНОЙ ИЛИ СОЛЯНОЙ КИСЛОТЫ
ФЕРМЕНТАТИВНЫЙ ГИДРОЛИЗ ПРОИСХОДИТ В ЖИВЫХ ОРГАНИЗМАХ ПОД ДЕЙСТВИЕМ ФЕРМЕНТОВ ПЕПТИДАЗ.
КАРБОКСИПЕПТИДАЗА РАЩЕПЛЯЕТ МОЛЕКУЛУ С ОБРАЗОВАНИЕМ КОНЦЕВОЙ КАРБОКСИДНОЙ ГРУППЫ.
АМИНОПЕПТИДАЗА ГЕНЕРИРУЕТ КОНЦЕВУЮ АМИНОГРУППУ.
Слайд 32ГОРЕНИЕ.
БЕЛКИ ПРИ СЖИГАНИИ ОБРАЗУЮТ АЗОТ, УГЛЕКИСЛЫЙ ГАЗ, ВОДУ И НЕКОТОРЫЕ ДРУГИЕ
ГОРЕНИЕ СОПРОВОЖДАЕТСЯ ХАРАКТЕРНЫМ ЗАПАХОМ ЖЖЁНЫХ ПЕРЬЕВ.
Слайд 33КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ.
ЭТО ЦВЕТНАЯ РЕАКЦИЯ НА БЕЛКИ,СОДЕРЖАЩИЕ АРОМАТИЧЕСКИЕ АМИНОКИСЛОТЫ. ЧАСТЬ ИХ ЯВЛЯЕТСЯ
ОПРЕДЕЛИМ СТЕПЕНЬ ПОЛНОЦЕННОСТИ ДЛЯ ПИТАНИЯ ЯИЧНОГО БЕЛКА.
В ПРОБИРКУ С БЕЛКОМ ДОБАВЛЯЕМ НЕСКОЛЬКО КАПЕЛЬ КОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТЫ. НАГРЕВАЕМ.
ОСАДОК ОКРАШИВАЕТСЯ В ЖЕЛТЫЙ ЦВЕТ И РАСТВОРЯЕТСЯ.
ОХЛАЖДАЕМ И ДОБАВЛЯЕМ РАСТВОР АММИАКА.
ОКРАСКА СТАНОВИТСЯ ОРАНЖЕВОЙ.
Слайд 35Классификация белков.
По растворимости:
Водорастворимые
Солерастворимые
Нерастворимые
По конформационной структуре:
Фибриллярные
Глобулярные
По химическому строению:
Протеины
Протеиды
Слайд 39
Какие вещества называются белками?
Каковы основные функции белков в живых организмах?
Как называются
Каков состав белков?
Что такое первичная структура белка?
Каковы химические свойства белков?
Что такое денатурация белка?
Какие вещества образуются при полном гидролизе белков?
Какие качественные реакции на белки вам известны?