- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Органические вещества. Белки
Содержание
- 1. Органические вещества. Белки
- 2. Слайд 2
- 3. “Жизнь есть способ существования белковых тел, существенным
- 4. “Лови ошибку”Белки – сложные органические полимеры, мономерами
- 5. Белки - биологические полимерыБелок – это высокомолекулярное
- 6. Аминокислоты Аминокислоты- азотсодержащие органические вещества, молекулы которых
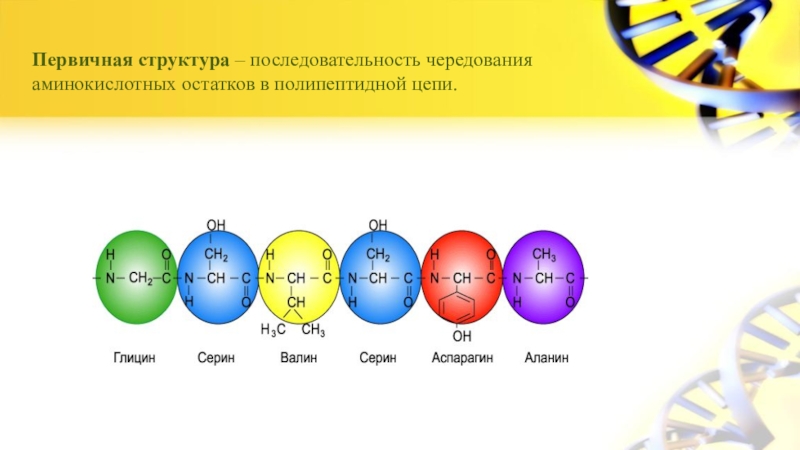
- 7. Первичная структура – последовательность чередования аминокислотных остатков в полипептидной цепи.
- 8. Вторичная структура белка возникает за счет
- 9. Третичная структура белка это глобулярная форма,
- 10. Четвертичная структура белкапредставляет собой объединение нескольких глобул
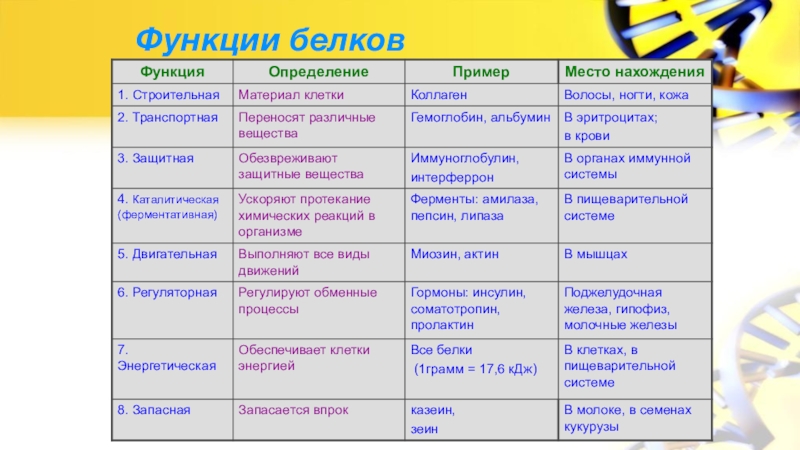
- 11. Функции белков
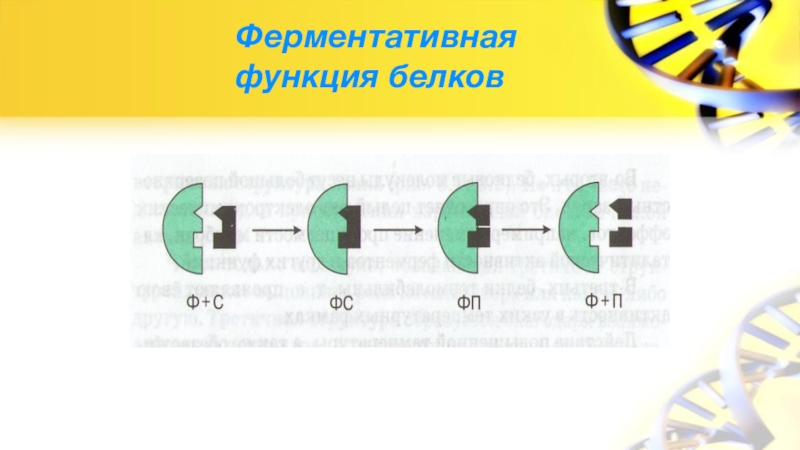
- 12. Ферментативная функция белков
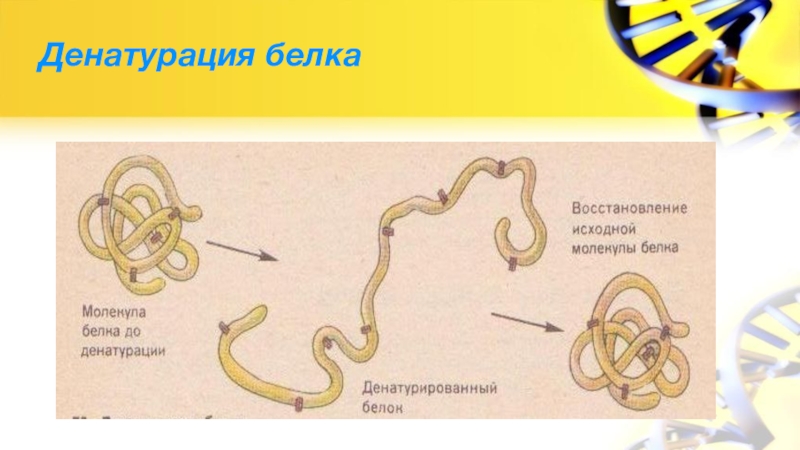
- 13. Денатурация белка
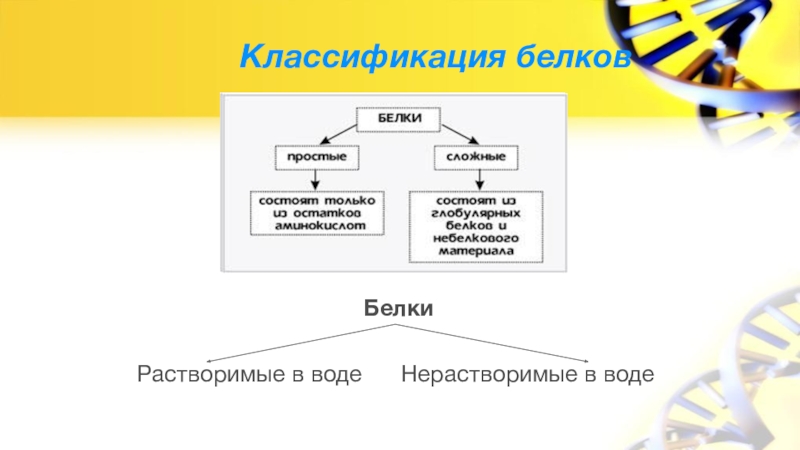
- 14. Классификация белков
- 15. Белки – источник незаменимых аминокислот.
- 16. Продукты, богатые белком:Творог, мясо, рыба, сыры, соя, горох, фасоль, орехи
- 17. Химические свойства белков1. Гидролиз (кислотно-основный, ферментативный), в
- 18. Цветные реакции на белки1. Ксантопротеиновая – взаимодействие
- 19. Рефлексия Рефлексия (ошибки в тексте выделены)Белки –
- 20. Проверь себяГлавными носителями жизни являются … .…
- 21. Ответы 1.Белки.Белки; остатков α –
- 22. Ответьте на вопрос:Почему же Ф.Энгельс определил белки как основу жизни на Земле?
- 23. «Скажи мне, и я забуду. Покажи
- 24. Спасибо за внимание!
“Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, при чём с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка.” Ф.Энгельс
Слайд 3“Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный
обмен веществ с окружающей их внешней природой, при чём с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка.” Ф.Энгельс
Слайд 4“Лови ошибку”
Белки – сложные органические полимеры, мономерами которых являются аминокислоты. В
состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией.
Вторичная структура белков – это чередование аминокислотных остатков в линейной структуре.
Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке яиц белок не меняет свой цвет.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией.
Вторичная структура белков – это чередование аминокислотных остатков в линейной структуре.
Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке яиц белок не меняет свой цвет.
Слайд 5Белки - биологические полимеры
Белок – это высокомолекулярное (103-107)
органическое соединение -
биополимер,
состоящий из мономеров – аминокислот,
соединенных пептидной связью (полипептид).
Мr(белка яйца) = 36000 Мr(С6Н12О6) = 180
Мr(гемоглобина) = 68000 Мr(NaCl) = 58
Мr(белка мышц) = 1500000
Формула белка молока: С1861Н3021О576N468S21
Формула гемоглобина С3032Н4816О872N780S8Fe4
состоящий из мономеров – аминокислот,
соединенных пептидной связью (полипептид).
Мr(белка яйца) = 36000 Мr(С6Н12О6) = 180
Мr(гемоглобина) = 68000 Мr(NaCl) = 58
Мr(белка мышц) = 1500000
Формула белка молока: С1861Н3021О576N468S21
Формула гемоглобина С3032Н4816О872N780S8Fe4
Слайд 6Аминокислоты
Аминокислоты- азотсодержащие органические вещества, молекулы которых содержат две функциональные группы:
1.
аминогруппу (NH2 ),
2. карбоксильную группу (СООН),
связанных с углеводородным радикалом.
Слайд 7Первичная структура – последовательность чередования аминокислотных остатков в полипептидной цепи.
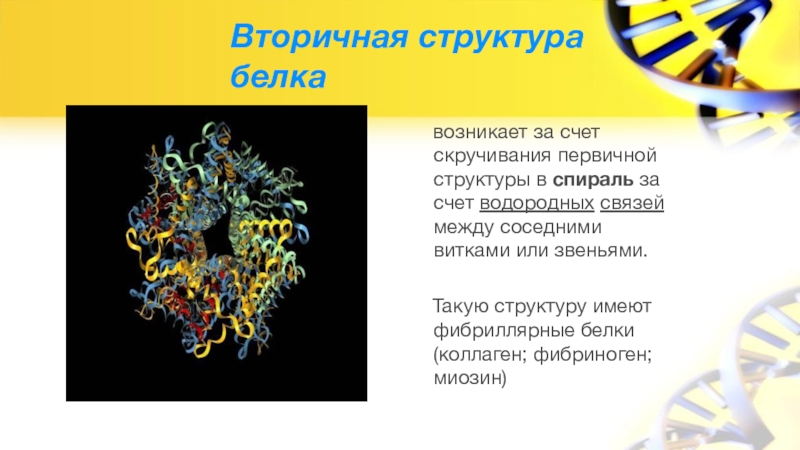
Слайд 8Вторичная структура белка
возникает за счет скручивания первичной структуры в
спираль за счет водородных связей между соседними витками или звеньями.
Такую структуру имеют фибриллярные белки (коллаген; фибриноген; миозин)
Такую структуру имеют фибриллярные белки (коллаген; фибриноген; миозин)
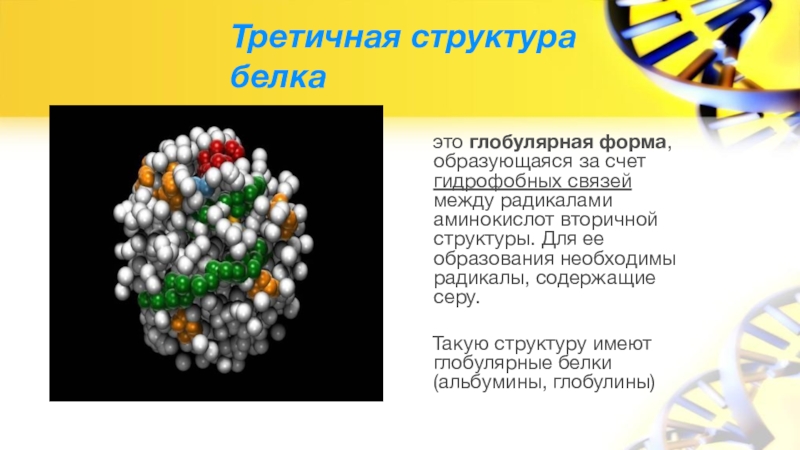
Слайд 9Третичная структура белка
это глобулярная форма, образующаяся за счет гидрофобных
связей между радикалами аминокислот вторичной структуры. Для ее образования необходимы радикалы, содержащие серу.
Такую структуру имеют глобулярные белки (альбумины, глобулины)
Такую структуру имеют глобулярные белки (альбумины, глобулины)
Слайд 10Четвертичная структура белка
представляет собой объединение нескольких глобул с третичной структурой в
единый конгломерат
Четыре глобулы
связанные атомом
железа имеет
белок гемоглобин.
Четыре глобулы
связанные атомом
железа имеет
белок гемоглобин.
Слайд 17Химические свойства белков
1. Гидролиз (кислотно-основный, ферментативный), в результате которого образуются аминокислоты.
2.
Денатурация – нарушение природной структуры белка под действием нагревания или химических реагентов.
Денатурированный белок теряет свои биологические свойства.
3. Ренатурация - полное или частичное восстановление денатурированными биополимерами своих свойств, в т. ч. биологической активности…
Слайд 18Цветные реакции на белки
1. Ксантопротеиновая – взаимодействие с концентрированной азотной кислотой,
которое сопровождается появлением желтой окраски.
2. Биуретовая – взаимодействие слабощелочных растворов белков с раствором сульфата меди (II), в результате которой появляется фиолетово-синяя окраска.
Слайд 19Рефлексия
Рефлексия (ошибки в тексте выделены)
Белки – сложные органические полимеры, мономерами
которых являются аминокислоты. В состав природных белков входят 20 аминокислот, 8 из них незаменимые, т.е. синтезируются в организме и их поступление в организм не обязательно вместе с пищей.
Белки, взаимодействуя с азотной кислотой, дают фиолетовое окрашивание. Данная реакция называется ксантопротеиновой реакцией. Вторичная структура белков – это чередование аминокислот в линейной структуре. Денатурация – процесс изменения цвета белковой молекулы. Содержание белка в яйце меньше, чем в молоке и молочных продуктах. При варке белок не меняет свой цвет.
Слайд 20Проверь себя
Главными носителями жизни являются … .
… - это сложные высокомолекулярные
соединения, построенные из … .
Элементный состав белков: … .
Молекулярная масса белков изменяется от … до … .
Многие белки растворимы в …, почти все растворяются в … .
Нерастворимы белки, из которых построены … .
В структуре белка различают … структуры.
Функции белков в организме … .
Элементный состав белков: … .
Молекулярная масса белков изменяется от … до … .
Многие белки растворимы в …, почти все растворяются в … .
Нерастворимы белки, из которых построены … .
В структуре белка различают … структуры.
Функции белков в организме … .
Слайд 21Ответы
1.Белки.
Белки; остатков α – аминокислот.
С, Н, О, N,
S.
Десяти тысяч, миллионов.
Воде, растворах солей, кислот; щелочах.
Ткани живых организмов: кожа, сухожилия, мышцы, ногти, волосы.
Первичную, вторичную, третичную, четвертичную.
8. Строительная, каталитическая, двигательная, транспортная, защитная, энергетическая
Десяти тысяч, миллионов.
Воде, растворах солей, кислот; щелочах.
Ткани живых организмов: кожа, сухожилия, мышцы, ногти, волосы.
Первичную, вторичную, третичную, четвертичную.
8. Строительная, каталитическая, двигательная, транспортная, защитная, энергетическая
Слайд 23«Скажи мне, и я забуду. Покажи мне, - я смогу запомнить. Позволь
мне это сделать самому, и это станет моим навсегда.»
(древняя мудрость)