- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Картирование ДНК. Программа Геном Человека. Геномная дактилоскопия.
Содержание
- 1. Картирование ДНК. Программа Геном Человека. Геномная дактилоскопия.
- 2. Картирование генов – определение положения данного гена
- 3. Геном человекаГеном - вся совокупностьгенетического материала23 пары
- 4. ПРИНЦИП ГЕНЕТИЧЕСКОГО КАРТИРОВАНИЯ Анализ генетического сцепления гена
- 5. Программа ГЕНОМ ЧЕЛОВЕКАПроект по расшифровке генома человекаThe
- 6. Цель проекта заключается в выяснении последовательности оснований
- 7. РЕЗУЛЬТАТЫ:Расшифрованные геномы.1995 г. - бактерия Hemophilus influenza;.1996
- 8. РЕЗУЛЬТАТЫ:Изученные гены человека. За 1995 г. длина
- 9. ГЕНОМНАЯ ДАКТИЛОСКОПИЯПредставляет собой метод, используемый в судебно-медицинской
- 10. Повреждения генов и наследственные болезни. Из 10
- 11. Общие принципы геномной дактилоскопии Методы молекулярной генетики,
- 12. «Геномный оттиск» ДНК человекаВ качестве гибридизационной пробы
- 13. Молекулярно-генетический идентификационный анализ позволяет исследовать особые участки
- 14. Технологии молекулярно-генетической индивидуализации:В судебно-экспертной практике базовыми молекулярно-генетическими
- 15. Анализ полиморфизма длины рестриктазных фрагментов ДНК
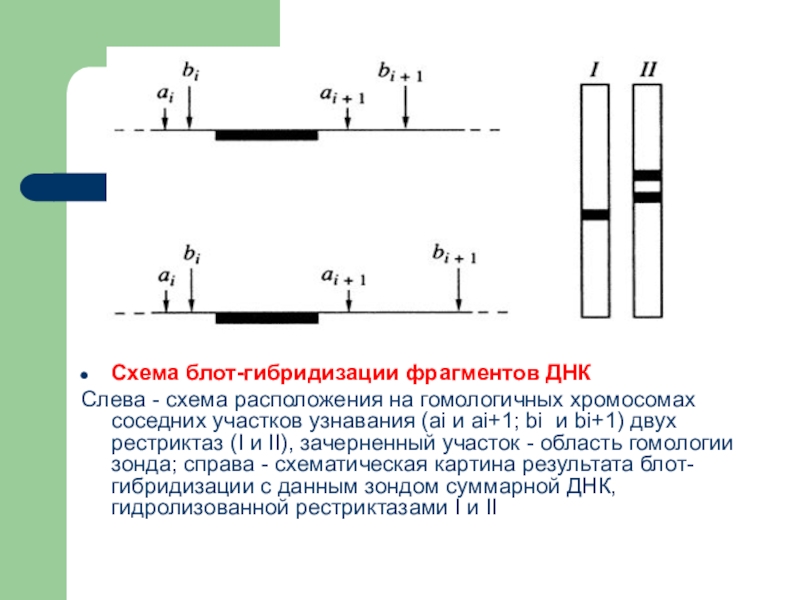
- 16. Схема блот-гибридизации фрагментов ДНКСлева - схема расположения
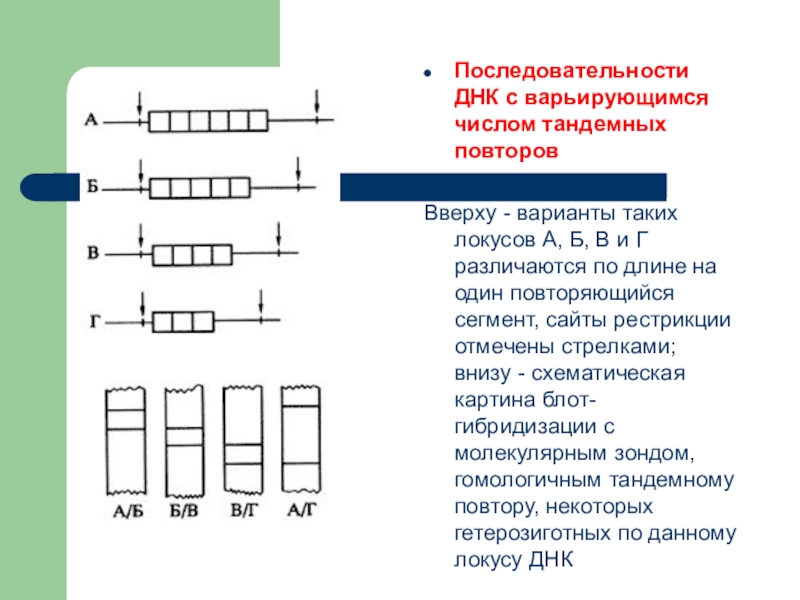
- 17. Последовательности ДНК с варьирующимся числом тандемных повторовВверху
- 18. Результаты идентификационной экспертизы,полученные с помощью меченного дигоксигенином
- 19. Электрофореграмма (окрашивание серебром)амплифицированных фрагментов ДНК – аллелей
- 20. Анализ полиморфизма нуклеотидных последовательностей ДНК
- 21. Карта митохондриального генома человекаОтмечены гены, локализованные на
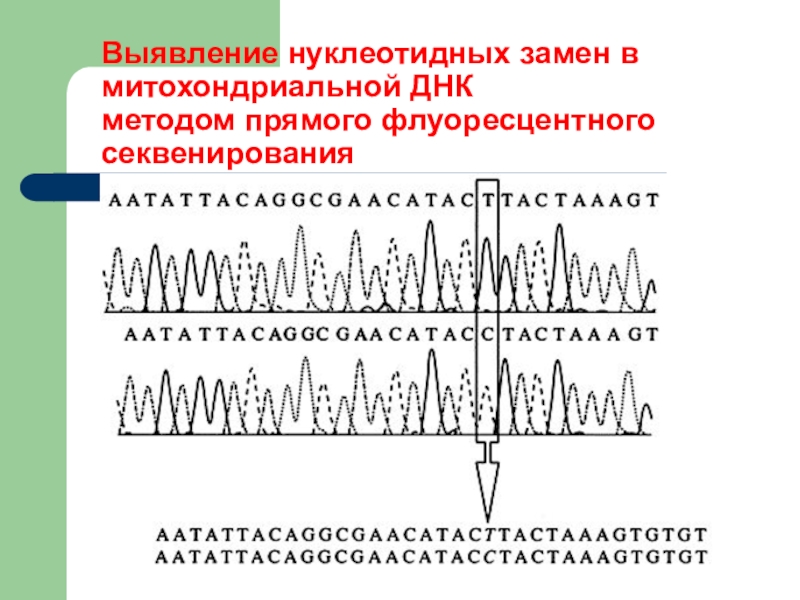
- 22. Выявление нуклеотидных замен в митохондриальной ДНК методом прямого флуоресцентного секвенирования
- 23. Возникшая на базе новейших достижений академической биологической
- 24. Спасибо за внимание.
Слайд 2Картирование генов – определение положения данного гена на какой-либо хромосоме относительно
Используют три основные группы методов картирования генов :
►физическое (определение с помощью рестрикционных карт, электронной микроскопии и некоторых вариантов электрофореза межгенных расстояний – в нуклеотидах),
►генетическое (определение частот рекомбинаций между генами, в частности, в семейном анализе и др.),
►цитогенетическое (гибридизации in situ, получение монохромосомных клеточных гибридов, делеционный метод и др.)
Слайд 3Геном человека
Геном - вся совокупность
генетического материала
23 пары хромосом и мтДНК
все гены
~ 3 млрд пар нуклеотидов
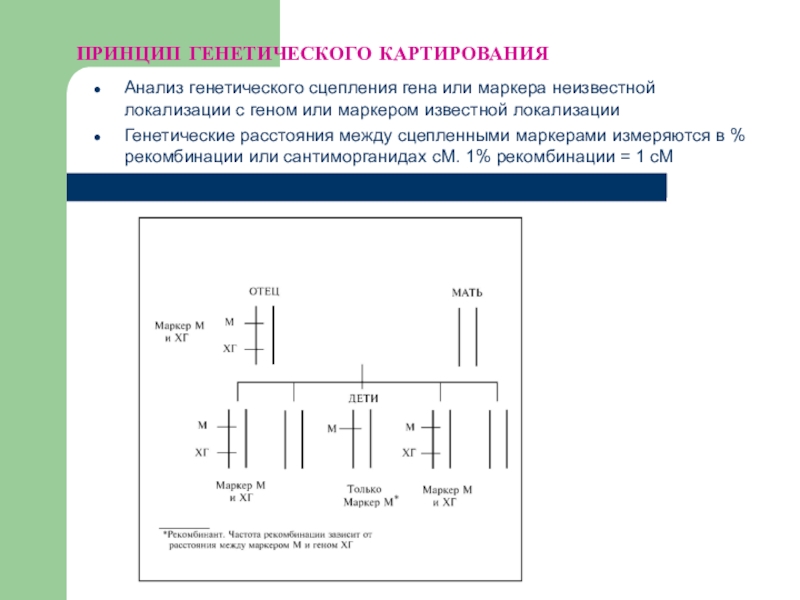
Слайд 4ПРИНЦИП ГЕНЕТИЧЕСКОГО КАРТИРОВАНИЯ
Анализ генетического сцепления гена или маркера неизвестной локализации
Генетические расстояния между сцепленными маркерами измеряются в % рекомбинации или сантиморганидах cМ. 1% рекомбинации = 1 сМ
Слайд 5Программа ГЕНОМ ЧЕЛОВЕКА
Проект по расшифровке генома человека
The Human Genome Project, HGP
Международный
главной целью которого было определить последовательность
нуклеотидов,
которые составляют ДНК и
идентифицировать 20,000-25,000 генов в человеческом геноме.
Проект начался в 1990 году,
под руководством Джеймса Уотсона
под эгидой Национальной организации
здравоохранения США
Слайд 6Цель проекта заключается в выяснении последовательности оснований во всех молекулах ДНК
Чтобы последовательно приближаться к решению проблемы картирования генов человека, было сформулировано пять основных целей: 1) завершить составление детальной генетической карты, на которой были бы помечены гены, отстоящие друг от друга на расстоянии, не превышающем в среднем 2 млн оснований (1 млн оснований принято называть 1 мегабаза, сокращенно Мб, от англ. слова base - основание); 2) составить физические карты каждой хромосомы (разрешение 0,1 Мб); 3) получить карту всего генома в виде охарактеризованных по отдельности клонов (5 тыс. оснований в клоне, или 5 килобаз, Кб); 4) завершить к 2004 году полное секвенирование ДНК (разрешение 1 основание) и 5) нанести на полностью завершенную секвенсовую карту все гены человека (к 2005 году). Ожидалось, что, когда все указанные цели будут достигнуты, исследователи определят все функции генов и разработают методы биологического и медицинского применения полученных данных.
Слайд 7РЕЗУЛЬТАТЫ:
Расшифрованные геномы.
1995 г. - бактерия Hemophilus influenza;.
1996 г. - клетка дрожжей
1998 г. - круглый червь Caenorhabditis elegans (19 тыс. генов, 97 Мб).
Слайд 8РЕЗУЛЬТАТЫ:
Изученные гены человека. За 1995 г. длина участков ДНК человека с
Слайд 9ГЕНОМНАЯ ДАКТИЛОСКОПИЯ
Представляет собой метод, используемый в судебно-медицинской экспертизе для идентификации лиц
Слайд 10Повреждения генов и наследственные болезни. Из 10 тыс. известных заболеваний человека
Слайд 11Общие принципы геномной дактилоскопии
Методы молекулярной генетики, несмотря на свою сложность,
На первом этапе необходимо получить очищенную ДНК из доступных исследователю образцов. А их спектр довольно широк: это может быть и кровь, и волосы, и жевательная резинка, и окурок сигареты, т.е. практически любые объекты, с которыми контактировал человек. Далее необходимо оценить количество полученной ДНК, это делают с помощью метода ПЦР в реальном времени, который кроме количества позволяет определить пригодность образца для использования в полимеразной цепной реакции.
На следующей стадии проводят специфичную амплификацию (наработку необходимого количества копий) вариабельных участков генома – STR-локусов, которые отличаются у разных людей только количеством единиц повтора, т.е. длиной последовательности. ПЦР проводят с праймеров, несущих флюоресцентную метку, что позволяет легко детектировать продукты амплификации.
Заключительным этапом является электрофоретический анализ, который позволяет определить генотипы тестируемых лиц по длине продуктов амплификации STR-локусов. Полученные генетические профили анализируют и в зависимости от задач исследования делают вывод о наличии биологического родства или принадлежности образцов тому или иному человека.
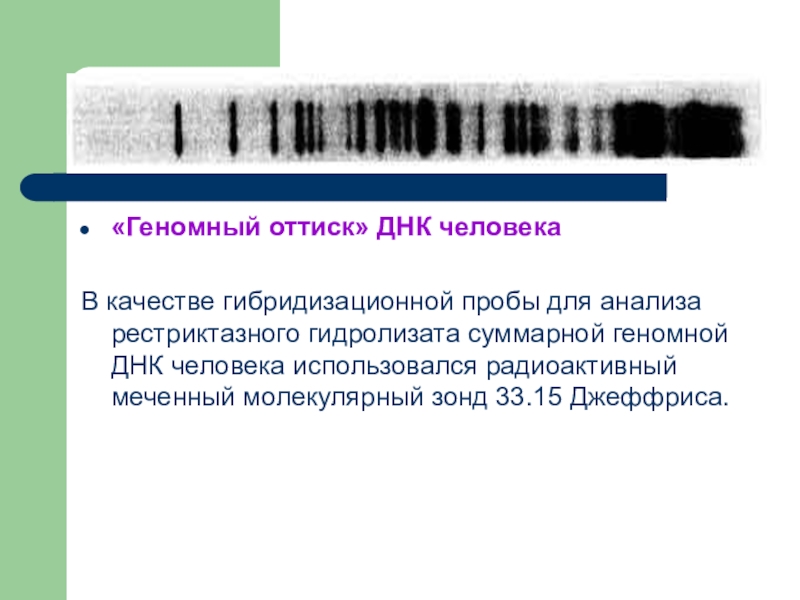
Слайд 12«Геномный оттиск» ДНК человека
В качестве гибридизационной пробы для анализа рестриктазного гидролизата
Слайд 13Молекулярно-генетический идентификационный анализ позволяет исследовать особые участки ДНК, строго специфичные для
Слайд 14Технологии молекулярно-генетической индивидуализации:
В судебно-экспертной практике базовыми молекулярно-генетическими технологиями признаны: анализ полиморфизма
Слайд 16Схема блот-гибридизации фрагментов ДНК
Слева - схема расположения на гомологичных хромосомах соседних
Слайд 17
Последовательности ДНК с варьирующимся числом тандемных повторов
Вверху - варианты таких локусов
Слайд 18
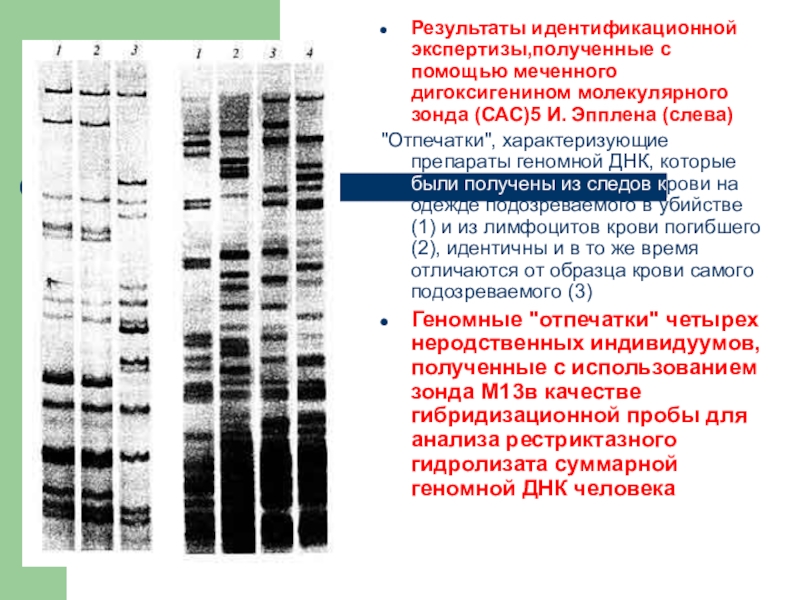
Результаты идентификационной экспертизы,полученные с помощью меченного дигоксигенином молекулярного зонда (САС)5 И.
"Отпечатки", характеризующие препараты геномной ДНК, которые были получены из следов крови на одежде подозреваемого в убийстве (1) и из лимфоцитов крови погибшего (2), идентичны и в то же время отличаются от образца крови самого подозреваемого (3)
Геномные "отпечатки" четырех неродственных индивидуумов,полученные с использованием зонда М13в качестве гибридизационной пробы для анализа рестриктазного гидролизата суммарной геномной ДНК человека
Слайд 19
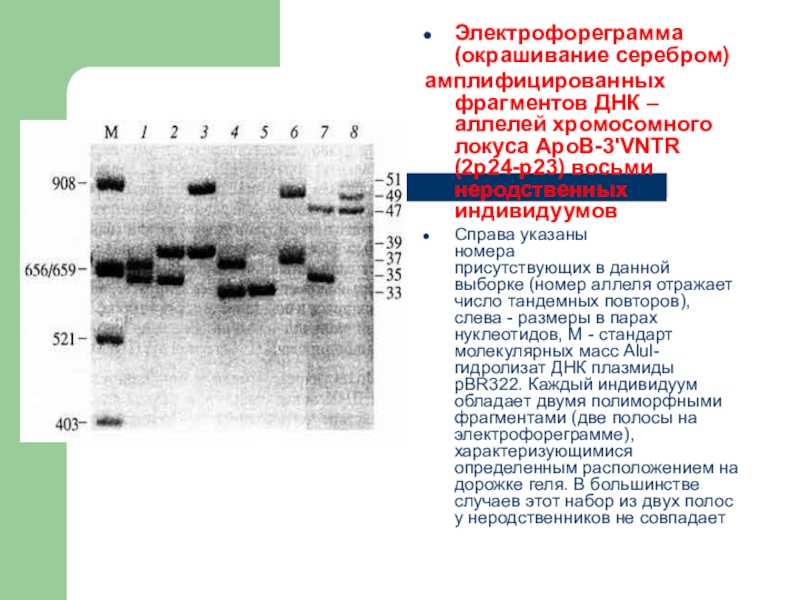
Электрофореграмма (окрашивание серебром)
амплифицированных фрагментов ДНК – аллелей хромосомного локуса ApoB-3'VNTR (2р24-р23)
Справа указаны номерааллельных вариантов, присутствующих в данной выборке (номер аллеля отражает число тандемных повторов), слева - размеры в парах нуклеотидов, М - стандарт молекулярных масс Alul-гидролизат ДНК плазмиды pBR322. Каждый индивидуум обладает двумя полиморфными фрагментами (две полосы на электрофореграмме), характеризующимися определенным расположением на дорожке геля. В большинстве случаев этот набор из двух полос у неродственников не совпадает